2010年,美国FDA批准新药21个,欧洲药品管理局(EMA)批准新药为14个,创近年来新低;跨国制药公司研发的新药在FDA或EMA严格的审核下,只有少部分得到批准,其余未获批准,一些新药因安全性或不良反应遭到撤市,一些被认为很具有潜力的新药在3期临床研究中遭遇失败。
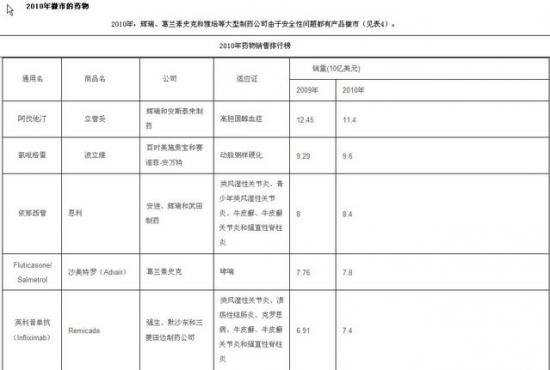
2010年制药公司新药研发高投入及产出依旧是热门话题,在获批新药中,生物制品(单克隆抗体和疫苗)所占份额较高;新研制的减肥药因安全性问题导致推迟批准上市,还有西布曲明、西他生坦(Thelin)和梵帝雅(Avandia,在欧洲退市,在美国使用受限)遭到撤市;辉瑞公司有3个新药获得FDA批准;礼来公司有3个产品在3期临床研究中遭受失败,1个生物制品申请遭拒;罗氏、诺华和阿斯利康公司也分别有2个新药申请遭FDA和其咨询委员会的拒绝;葛兰素史克和默沙东公司分别有4个和3个新药获得EMA批准,没有新分子实体(NME)通过FDA批准。>
颇具潜力在研新药3期临床遭到失败
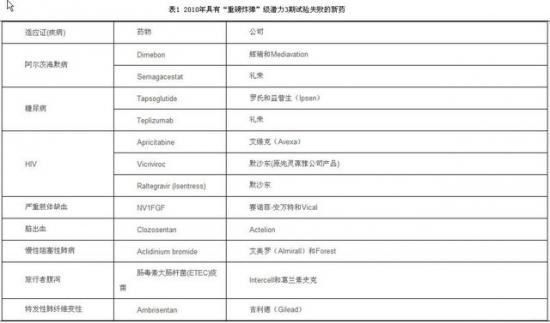
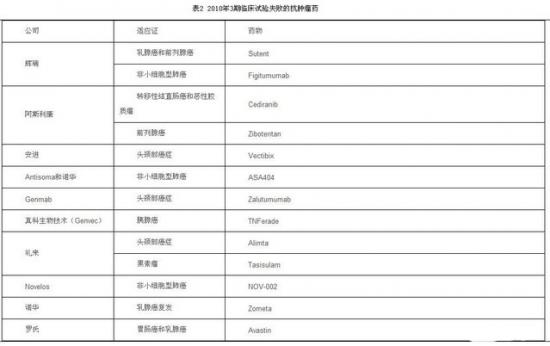
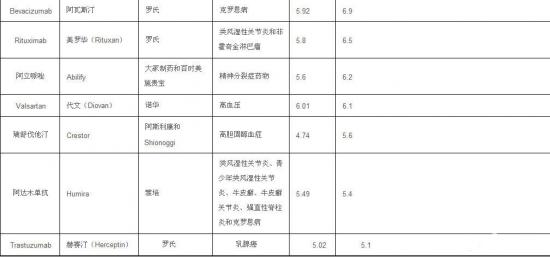
因安全性和疗效原因遭受失败的具有“重磅炸弹”级潜力的3期新药可能导致制药公司损失数十亿美元(见表1)。另外,2010年,作为热门研究领域的抗肿瘤药物研究也纷纷宣告失败(见表2)。
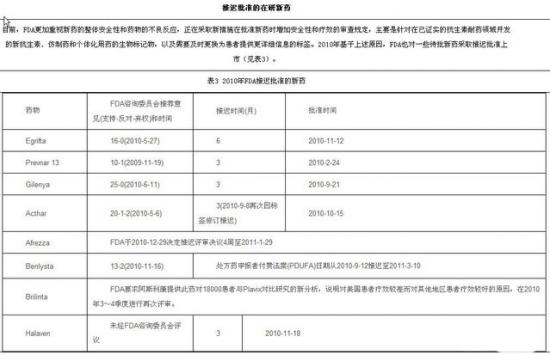
获得批准的新药
2010年,FDA批准的具有数十亿美元销量潜力的药物有达比加群酯(Dabigatran)、芬戈莫德(Fingolimod)、利拉鲁肽(Liraglutide)、普瑞巴林(Pregabalin)、Tesamorelin、妥克利骨(Tocilizumab)、狄诺塞麦(Denosumab)和疫苗Prevnar 13、Provenge、Menveo。辉瑞有3个新药获得FDA批准,成为最大的赢家。生物制品申请/新药上市申请(NDA/BLA)获得批准的机会从2009年的75%降至2010年的60%。下面列出的是部分具有“重磅炸弹”级潜力药物。
Denosumab (狄诺塞麦),安进公司,治疗骨质疏松症。
Fingolimod(芬戈莫德),三菱田边制药公司,复发型的多发性硬化症。
Tocilizumab (妥克利骨),罗氏公司,治疗类风湿性关节炎。
dabigatran (Pradaxa,达比加群酯),勃林格殷格翰公司,治疗房颤患者发生卒中风险的口服凝血酶抑制剂。
2010年,EMA批准 的“重磅炸弹”级的潜力药物有Tocilizumab(妥克利骨)、Denosumab(狄诺塞麦)、单克隆抗体Ofatuzumab和Pazopanib(帕唑帕尼)。葛兰素史克有4个新药获得EMA 批准,成为欧洲R"D的佼佼者,默沙东紧随其后,有3个新药获得批准。不过文迪雅的退市使欧洲药物市场黯然失色。