生物体有性繁殖、发育和内稳态维持的基础是细胞与细胞之间的融合。在生理过程中,细胞融合决定了受精的成功与否。在骨骼肌生长、修复过程中,成肌细胞的融合是形成多核肌纤维细胞的基础。在胎盘的形成过程中,单核的滋养层细胞融合,分化生成合体的滋养层细胞,形成胎盘屏障,避免来自母体血液的免疫细胞攻击胎儿。
细胞融合具有如此重要的作用,但是目前还没有搞清楚其融合机制。近日,杜克大学的杨黄河、张洋团队在Science Advances杂志上发表了题为“MEM16F phospholipid scramblase mediates trophoblast fusion and placental development”的研究文章。文章发现TMEM16F能够使磷脂酰丝氨酸(PS)翻转到细胞外膜上,在胎盘滋养层细胞融合中发挥重要作用。
磷脂酰丝氨酸(PS)主要存在于真核细胞质内膜,一旦转运到细胞膜外暴露时,就会发挥多方面的细胞信号,比如促进血液凝固、招募巨噬细胞以及各种细胞融合。在本研究中发现滋养层细胞融合需要PS转运到细胞外膜表面。而这一过程需要磷脂翻转酶的催化作用。
TMEM16家族是目前所知的磷脂翻转酶。本研究通过检测滋养层细胞系及原代滋养层细胞中的TMEM16家族的mRNA表达水平,结果发现TMEM16F能够高表达。并且在妊娠早期和足月胎盘中,TMEM16F在胎盘绒毛的合体滋养层细胞中显著高表达。说明TMEM16F是人滋养层细胞中PS转运的主要磷脂翻转酶。
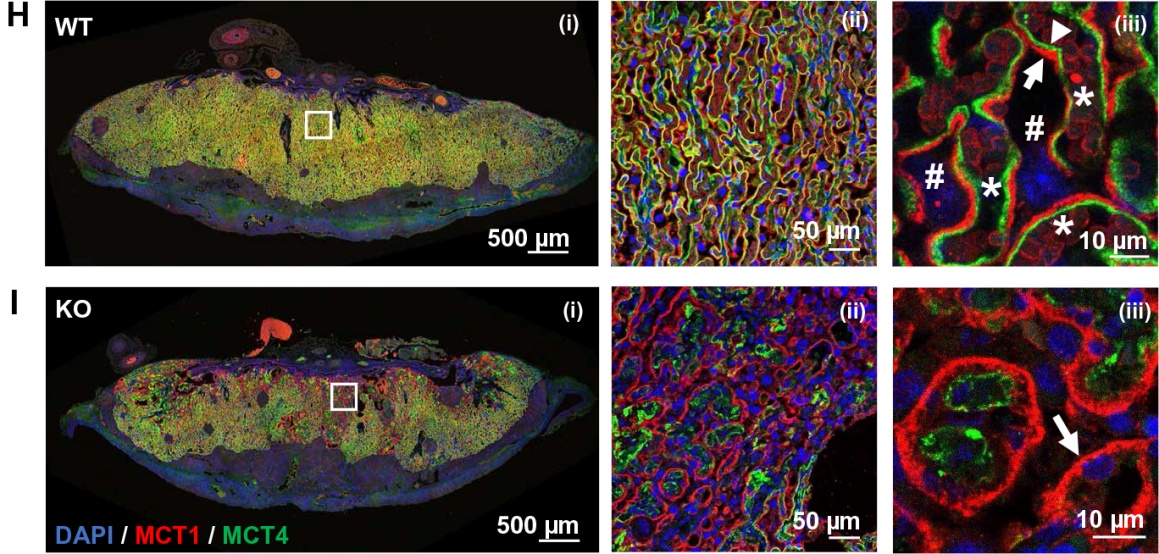
通过TMEM16F基因敲除与野生型的小鼠进行对比,利用免疫组织学技术,证实了TMEM16F敲除小鼠的胎盘发育缺陷。在胎盘中靠近胎儿一侧会出现明显的胎盘滋养层合胞体缺失,直接导致营养交换不充分,造成胎儿血管发育障碍。并且会导致小鼠围产期的死亡。
总之,通过本文可以确定TMEM16F在调控滋养层细胞融合及胎盘发育中具有重要作用。这是一种细胞融合的新机制。并且证明磷脂酰丝氨酸翻转到细胞外膜不仅是一种细胞凋亡信号,也是细胞融合信号。
本次研究通过体外细胞实验以及基因敲除技术,利用免疫组化染色、mRNA分析等,从分子到细胞层面揭示了细胞融合的新机制,为治疗胎盘相关的妊娠疾病及其并发症提供了新思路。TMEM16F介导的细胞融合机制还将有助于理解不同细胞融合相关疾病,如肌肉营养不良、不育症、病毒感染等。
免疫组织化学/荧光技术是研究组织形态和抗原表达表位不可或缺的检测技术,广泛用于生物学的各个研究领域。随着精准化治疗及蛋白质组学的发展,尤其是像病毒检测这类样本较少的情况下,单一染色已经不能满足抗原蛋白互作研究的需求了。因此开发多重免疫免疫组化染色技术已经迫在眉睫。
众所周知,免疫组化实现1-2种染色比较容易,但是要在一个切片上实现7-8种染色就会很困难。抗体的来源、染料的波长、洗脱造成的抗原损失、图像的叠加等多种因素,造成多重免疫组化染色技术难以实现。那么怎样才能突破这些技术难点呢?
5月21日14:00,义翘神州特邀请具有多年IHC实战经验的李天月老师,举办了一场“如何突破多重免疫组化染色技术难点”的在线课堂,扫描下方二维码立即免费报名预约。

温馨提示:本次课程设有直播专用交流群,讲座直播间入口及答疑环节届时都将在群里进行。直播前一小时,工作人员会把直播间入口用短信或邮件的方式发送给大家。添加义翘客服小助手:sinobio2019,回复「多重免疫组化」,即可拉您入群。