牛体内重组牛生长激素 (rbST) 快速高灵敏度检测
Gaud Pinel1 , Sandrine Roulet-Rochereau1 , Marie-Hélène Le Breton1,2 ,
Sylvain Chéreau1 , Fabrice Monteau1 , Paul Silcock3 ,与 Bruno Le Bizec1
1 Laboratoire d’ Etude des Résidus et Contaminants dans les Aliments (LABERCA) , ONIRIS , Nantes , France 法国 LABERCA 化学实验室
2 瑞士洛桑雀巢公司,雀巢研究中心
3 英国曼彻斯特沃特世公司
应用优势
牛注射了重组牛生长激素,过几天后检测药物在牛体内的残留。首次得到了明确的检测结果,可用于此类药物的使用监控。
■ Xevo TQ MS 的高灵敏度可准确检测生物基质中的重组牛生长激素( rbST ),符合 2002/657/EC 要求。
■ 方法的灵敏度高,非常适合用于在给药几天后检测动物血液中痕量的残留激素药物。
■ Xevo TQ MS 提供重复性好的结果,且基质效应很低,这对于药物监控计划实施中的常规分析来说是十分重要的。
沃特世解决方案
■ ACQUITY UPLC , Xevo TQ MS
关键词
■ rbST , reST ,生长激素,食品安全
简介
动物性食品安全控制是政府、国际法规机构与组织的重要任务,应该在食品进入消费环节之前就对食品安全进行有效的检测和控制。因为上市后的食品安全事件可能影响消费者信心与国际贸易。
重组牛生长激素( rbST ),又称为生长激素,在一些国家通常作为猪或牛的生长促进剂,将其用于乳牛可以增加牛奶产量 1,2 。然而,生长激素的使用有严格的法律规范,在欧盟国家是完全禁用的 3,4 。但是,这项法规的执行面临着很大的困难,主要是因为缺乏有效的分析工具来检测是否存在滥用该激素的情况。此分析的困难在于生长激素本身是蛋白质,且在生物基质中浓度较低,而样品基质组成又十分复杂。至今为止,分析方法仅仅局限为酶联免疫检测,这个方法不能将天然存在的激素与重组激素分离开来;尽管也有其它应用报导,但都不能专属性很强地检测生理水平的重组牛生长激素( rbST ) 5,6 。
直到最近才开发出了一项直接检测生物基质中重组牛生长激素( rbST )的方法 7,8 ,这个方法是将重组生长激素用胰蛋白酶进行水解,然后分析生长激素专有的 N- 端肽链。事实上,天然激素的 N- 端氨基酸是丙氨酸,而重组激素的 N- 端氨基酸是甲硫氨酸。
此应用文章展示了使用 Waters® XevoTM TQ MS 分析注射了重组激素的动物血浆样品中的药物。在注射后几天进行检测,可清晰检测出结果,展示了一流水平。
实验部分
重组激素标准品
重组牛生长激素( rbST )标准品与重组马生长激素( reST )分别购自哈勃 UCLA 医学中心国家激素与垂体项目(美国托兰斯)以及 Bresagen 有限公司(澳大利亚 T hebarton )。
样本制备
重组牛生长激素在血浆中的样本提取、纯化步骤依照文献进行。 7,8
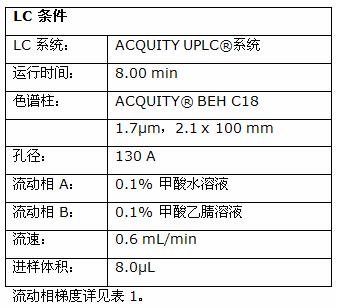
MS 条件
MS 系统: XEVO TQ MS
离子化模式: ESI+
毛细管电压: 3 kV
源温度: 150 ℃
脱溶剂温度: 550 ℃
脱溶剂气速: 800 L / 小时
碰撞气流速: 0.15 mL/ 分
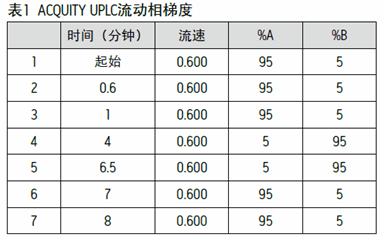
MRM 方法参数
MRM 通道通过 Masslynx 软件中的 IntelliStartTM 行独立的参数优化,详见表 2 。
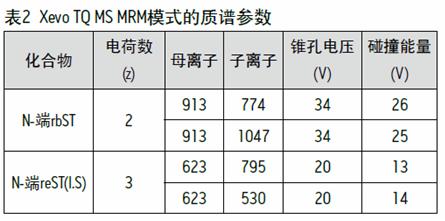
结果与讨论
LC/MS/MS 条件优化
ACQUITY UPLC 系统对胰蛋白酶水解的 N- 端肽片段又很好的保留和分离效果,总运行时间 8 分钟,重组牛生长激素( rbST )与重组马生长激素( reST )的 N- 端保留时间分别为 2.74 和 2.79 分钟(图 1 )。
重组牛生长激素( rbST ) N- 端肽链在电喷雾正离子模式产生双电荷的离子 [M+2H]2+=913 ,将此离子作为母离子。根据 2002/657/EC 欧盟委员会决议 10 , MRM 方法中选择了两个子离子用于确证;重组马生长激素( reST )作内标物,在样品中的浓度为 100 ng/mL ,其 N- 端肽链在电喷雾正离子模式产生三价电荷的离子 [M+3H]3+= 623 ,将其作为母离子。
动物注射生长激素后体内 rbST 的检测
此方法用于检测注射生长激素后的动物样品。对奶牛一次性皮下注射 500mg Lactatropin® 药物,然后取样分析。

图 1 对 10 ng/mL 的 rbST 和 reST 标准品进样, UPLC(ESI+)/MS/MS 的 MRM 特征离子信号分别为 rbST 的 N- 端碎片离子为 913<774 和 913<1047 ; reST 的 N- 端碎片离子为 623 <795 和 623 <530
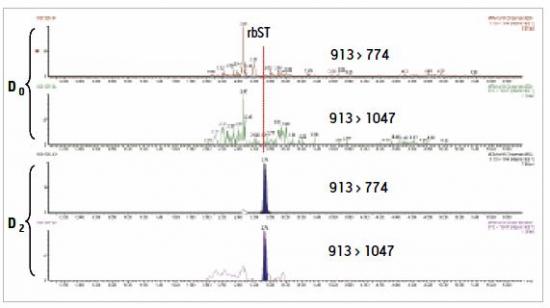
图 2 使用 UPLC ( ESI+ ) /MS/MS 分析注射药物前( D0 )与注射后两天( D2 )采集到的血浆样本的的 MRM 特征离子信号图谱
图 2 显示了注射药物前采集到的血浆样本得到的谱图( D0 )以及注射药物两天后血浆样本的谱图( D2 )。
图 2 的结果表明:可以在给动物注射生长激素两天后在奶牛的血浆中检测到 rbST 。对采集到的特征信号分析表明此方法可以对生长激素这个蛋白进行明确的确证,符合 2002/657/EC 的要求,同时确认了检测方法的灵敏度。
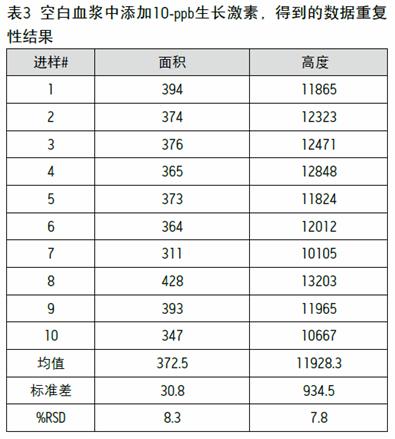
与预计的动物血浆蛋白水平一致。基质干扰几乎检测不到,在实际血浆样本中的良好线性可保证对 rbST 的进一步相对定量结果,在注射生长激素两天后还可以检测到血浆中 50 ppb 的药物,与以往实验结果一致 7,11 。表 3 显示了平行进样 10 次得到的分析结果,这充分说明 Xevo TQ MS 在检测低含量复杂样品时能够提供重复性好的数据。
结论
■ Xevo TQ MS 的高灵敏度可准确检测生物基质中的重组牛生长激素( rbST ),符合 2002/657/EC 要求
■ 方法的灵敏度高,非常适合用于在给药几天后检测动物血液中痕量的残留激素药物
■ Xevo TQ MS 提供重复性好的结果,且基质效应很低,这对于药物监控计划实施中的常规分析来说是十分重要的
参考文献
[1] Burton JL, McBride BW, Block E, Glimm DR and Kennelly JJ. A review of bovine growth hormone. Canadian Journal of Animal Science. 1994; 74: 167-201.
[2] Bauman DE and Vernon RG. Effects of exogenous bovine somatotropin on lactation. Annual review of Nutrition. 1993, 13: 437-461.
[3] Council Decision of 20 December 1994 amending Decision 90/218/ EEC concerning t he placing on t he market and administration of bovine somatotropin (BST). Official Journal of the European Communities. 1994/936/EC
[4] Council Decision of 17 December 1999 concerning the placing on the market and administration of bovine somatotropin (BST) and repealing Decision 90/218/EEC. Official Journal of the European Communities. 1999, 1999/879/EC.
[5] Blokland MH, Sterk SS, Van Ginkel LA, Stephany RW, and Heck AJR. Analysis for endogenous and recombinant porcine somatotropine in serum. Analytica Chimica Acta 2003, 438, 201-206.
[6] Pinel G, Buon R, Aviat F, Larre C, André-Fontaine G, André F, and Le Bizec B. Recombinant bovine somatotropin misuse in cattle. Evaluation of western blotting and 2D electrophoresis methods on biological samples for the demonstration of its administration. Analytica Chimica Acta 2005, 529, 41-46.
[7] Le Breton M H, Rochereau-Roulet S, Pinel G, Bailly-Chouriberry L, Ryc hen G, Jurjanz S, Goldmann T, and Le Bizec B. Direct determination of recombinant bovine somatotropin in plasma
from a treated goat. Rapid Communication in Mass Spectrometry. 2008; 22: 3130-3136.
[8] Le Breton M H, Rochereau-Roulet S, Pinel G, Cesbron N and Le Bizec B. Elimination kinetic of recombinant somatotropin in bovine. Analytica Chimica Acta. 2009; 637: 121-127.
[9] Monteau F, Antignac JP, Pinel G, Silcock P, Hancock P, Le Bizec B. Xevo TQ MS:Adressing new challenges in the field of growth promoters in biological samples. Waters Application Note 2009.
[10] Commission Decision of 12 August 2002 implementing Council Directive 96/23/EC concerning the performance of analytical methods and the interpretation of results. Official Journal of the European Communities. 2002, 2002/657/EC.
[11] Le Breton M H, Rochereau-Roulet S, Chereau S, Pinel G, Delatour T and Le Bizec. Identification of cows treated with recombinant bovine somatotropine. Journal of Agricultural and Food Chemistry, DOI:10.1021/jf903032q.
来源:沃特世科技(上海)有限公司
联系电话:电话: (021)68795888,4008202676(免费电话支持专线)
E-mail:lin_hai_zhang@waters.com