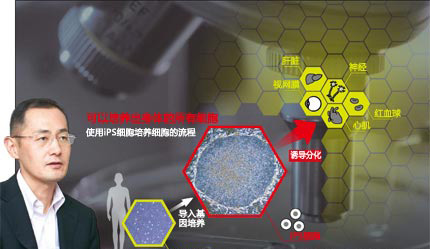
2012年诺贝尔生理学或医学奖得主、京都大学教授山中伸弥发现了iPS细胞(诱导性多能干细胞)。这项技术之所以能够得到被称为“革命”的评价,其中有两方面的原因。
其一是iPS细胞具有的不可思议的性质。只要有场地和资金,iPS细胞可以在培养皿中培养1万个、1亿个,甚至无限增加。而且,在不同的培养环境下,iPS细胞可以生长为神经、视网膜、心肌、血液、肝脏等身体所有组织的细胞。
其二是培养简单。iPS细胞的培养只需要在微量的皮肤和血液细胞中注入几个基因即可。随着iPS的出现,过去ES细胞(胚胎干细胞)存在的破坏受精卵的生命伦理问题迎刃而解。
iPS细胞产生的原理还有很多未解之谜,但iPS细胞蕴藏的潜力显而易见。使身体找回已丧失功能的再生医疗、发现疑难杂症致病机理和治疗药物的开发——iPS细胞对医疗产业的影响不可限量。
日本政府准备向iPS细胞研究领域投入巨额资金,规模之大和期间之长均史无前例。
但iPS细胞产业化的较量才刚刚开始。在基础研究上慢了半拍的欧美正虎视眈眈,准备凭借其擅长的商业化操作吹响反攻的号角。日本如果过分注重基础技术开发,或许会像家电和半导体等产业一样,重蹈“技术赢、业务输”的覆辙。
再生医疗商机无限
iPS细胞有望令再生医疗这一终极医疗手段成为现实。在日本,相关风险企业如雨后春笋般涌现,再生医疗商业化已然开始。然而其中要解决的课题依然很多,如安全性、成本、与海外企业的竞争等等。
因没有有效的治疗方法而使众多患者饱受折磨的疑难杂症,如今有了治愈的希望。打开希望之门的,是山中伸弥在2006年发现的iPS细胞。随着iPS细胞的发现,再生医疗商业化的时机日渐成熟。
位于神户市的理化学研究所正在进行利用iPS细胞培养眼球视网膜细胞的研究。这项研究的目的是把培养成薄膜状的视网膜细胞移植到患者的眼球中,使受损的功能得到恢复。
治疗的疾病是“老年性黄斑变性”。这种疾病会导致视网膜黄斑随年龄出现异常老化,造成视野狭窄、视力低下,最终甚至可能失明。截至目前,该病尚无有效治疗方法,只能通过保守治疗加以缓解。在日本,该病的老年患者也在不断增加,如果能建立起治疗方法,全世界的市场规模估计可达2万亿日元。
理研准备在2013年度把iPS细胞培养的视网膜细胞实际应用于患者,实施全球第一例临床研究。实施该研究的神户市尖端医疗中心的伦理委员会已于2月13日批准了这项计划。该计划预计在日本政府批准之后正式启动。
为商业化而成立的风险企业——日本视网膜研究所的社长键本忠尚表示:“视网膜治疗成为一项业务的各项必要条件已经齐备。”
这里所说的条件并不仅是市场规模的大小,还包括视网膜细胞具有易于避免iPS细胞“癌变”隐患的优点。
可分化成各种组织细胞的iPS细胞存在的难点是,与未分化的细胞混合时,有可能发生癌变。但治疗使用的视网膜细胞呈褐色,容易与透明的iPS细胞相区别。而且移植需要的细胞数量少,比较容易只挑选安全的细胞进行操作。除此之外,不同于内脏等器官,视网膜手术后容易进行随访,便于发现异常。
在日本,视网膜细胞膜估计会被划分成医疗器械,而非药品,可能会比较容易获得相关部门的批准。作为再生医疗应用的第一步,各项条件得天独厚的视网膜治疗最受期待。
iPS细胞可解决“血荒”问题
利用iPS细胞培养血液。为了实现这一目标,东京大学和京都大学合作成立的风险企业Megakaryon计划于2014年以后,在日美实施临床试验。
Megakaryon描绘的商务模式是,该公司将研究利用iPS细胞培养血小板,自己掌握核心的细胞分化技术,在此基础上与外部企业合作,大量制造血小板,然后向医院提供没有传染病隐患、可以稳定供应的输血用血小板。
目前,手术用血存在慢性短缺,Megakaryon社长三轮玄二郎预测,“单是弥补发达国家献血的缺口,在本世纪20年代后期,市场规模就有望达到600亿日元左右”。如果能够进入印度等献血制度不完善的发展中国家,市场规模还将得到进一步扩大。
血小板也是容易避开iPS细胞癌变问题的领域。由于没有包含遗传信息的细胞核,所以只需照射放射线,基本上就可以完全避免癌变风险。
iPS细胞应用方面已经出现了商业化动向。在角膜再生、改善心衰的心肌细胞、帕金森氏症和脊髓损伤的治疗等方面,日本政府也准备在5~7年内转入临床应用。
利用“细胞银行”降低成本
不同于视网膜和血小板,在上述领域,癌变风险有可能成为课题。京都大学iPS细胞研究所特聘助教渡边亮指出,“这除了需要在移植时防止混入未分化的iPS细胞之外,还需要结合在培养中去除基因受损细胞的技术”。在实用化之前,必须要收集iPS细胞是否会在人体内肆意繁殖、癌变由哪些基因引发等数据。
面对这些全面产业化中可能出现的课题,先头部队已经出动,那就是以降低iPS细胞本身的“生产成本”为目的的举措。
iPS细胞公认的优点是使用患者自己的细胞制作目的组织进行移植,能够避免排异反应。但从实际情况来看,培养iPS细胞需要1~2个月,使其分化成目的细胞也需要1~2个月,费用不下数百万日元。
在有望通过iPS细胞再生医疗得到治疗的疾病中,患者稀少的罕见疾病、脊髓损伤等事故发生后需要尽快治疗的疾病不在少数。在实现产业化之前,必须要建立起能在需要的时间、以低廉的价格提供所需细胞的方法。
在1月下旬于神户市召开的再生医疗研讨会上,山中教授宣布,“为临床应用事先准备合格iPS细胞的工作将由再生医疗用iPS细胞银行开展。该细胞银行将从2月份开始培养第一例iPS细胞”。
按照设想,iPS细胞银行的职能是利用志愿者提供的血液细胞培养iPS细胞,在确保品质的状态下将其保存。存储的iPS细胞虽然不是利用患者自身的组织培养,但通过按照细胞的“血型”、也就是“HLA型”进行合理选择,大多数患者都可以避免排异反应。
医疗应用面临的最大障碍是时间和成本的问题,可以说,iPS细胞银行是能够克服这些问题的“基础设施”。
iPS细胞的再生医疗应用虽然已经起步,但进展并不会一帆风顺。实际上,在日本,能够保本的再生医疗业务至今还没有成功的先例。
“要是现在再让我去做(再生医疗业务),我恐怕会犹豫。虽然研究者们最近表现出色,但作为业务开展的难度很大。”
Japan Tissue Engineering(J-TEC)的社长小泽洋介苦笑着这样说道。该公司是目前日本唯一一家获准制造销售再生医疗产品的企业。但从创业到2011财年为止,该公司已经连续亏损了14年。
J-TEC于2007年在日本率先获得利用烧伤患者自身的皮肤细胞制作培养表皮的许可,从2009年开始销售。从开始研发到能够销售花了大约10年的时间。
但是,由于日本的医疗保险仅适用于大面积烧伤的危重患者,而且1次使用的表皮量存在限制,常常出现患者在为期3周的培养期内死亡的情况,因此,产品的损耗增加了成本负担。在其他公司相继放弃业务的情况下,J-TEC虽然成功进入市场,但是,要想把再生医疗打造成一项业务,政府相关部门的推动,以及收益性评估必不可少。
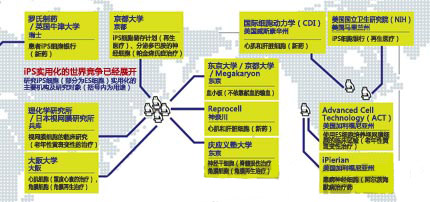
日本虽然在iPS细胞的基础研究上长期处于世界领先地位,但面对这项“梦之技术”,海外也加快了追赶日本的步伐。在日本意欲设立的细胞银行方面,海外其实已经走在了前面。
美国国立卫生研究院(NIH)已从2012年秋开始在华盛顿郊外建设iPS细胞银行。承建方是在治疗用细胞的培养方面已获得了优异业绩的著名药品代工生产商——瑞士龙沙集团(Lonza)。
龙沙内部人士自信地表示,“我们将尽快建立起能够应用于人体的iPS细胞高效培养方法,以及高品质的试验步骤”。从NIH的计划不难看出,美国虽然在iPS细胞的基础研究方面落在了日本的后面,但在着眼于商业化的细胞银行建设方面,美国要夺回霸权。
虽然京都大学iPS细胞研究所副所长林秀也强调“在简单、高效地培养优质iPS细胞的技术经验上,京都大学排在世界首位”,但“美国现在对事实标准虎视眈眈。日本在速度上无法与之抗衡”的危机感如今正在日本的iPS细胞研究者之间蔓延。
全面启动要待2020年以后
不同于日本,其他国家对于iPS细胞并不太执着。也有不少看法认为,为了尽快给患者送去治疗方法,日本也不应该抓着iPS细胞不放,而是要拓展研究视野。
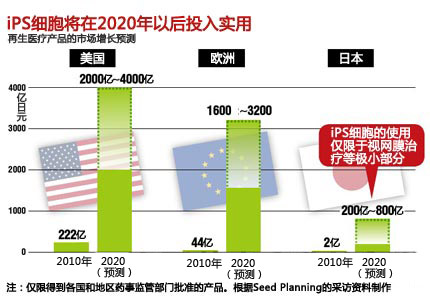
调查公司Seed Planning估算,到2020年,全世界再生医疗产品的市场规模最大将接近1万亿日元,是2010年的30倍。2010年仅为2亿日元的日本国内市场预计将激增到近1000亿日元,这依靠的是环境的快速完善,其中包括了日本政府积极提供研究经费补助、医疗产品审批速度的加快以及规定再生医疗手续的新法律的制定。
然而,在截至2020年的市场预测中,利用iPS细胞的产品还仅限于视网膜治疗等极小的一部分。带动再生医疗市场实现快速发展的动力是癌免疫细胞医疗,以及利用原本就存在于人体内、能够分化成其他细胞的“成体干细胞”的技术。使用iPS细胞的再生医疗估计至少要到等到本世纪20年代以后,市场才能全面建立起来。

Seed Planning执行董事五十岚夕子指出,“美国等其他国家并不拘泥于iPS细胞,而是为每个应用领域选择最适合的技术,在此基础之上争取早日实现再生医疗”。
其中,美国再生医疗风险公司Advanced Cell Technology(ACT)已经开始使用ES细胞(胚胎干细胞)来开展老年性黄斑变性治疗的临床试验。在今后很可能成为日本的强劲对手。
“请问iPS细胞最近有望投入临床应用的再生医疗有哪些?”“成年期脊髓损伤也能用iPS细胞来治疗吗?”
在神户市的研讨会上,有不少听众坐轮椅到场,在会场内,对于研究者的期待之声不绝于耳。确保安全性与经济效益,与海外的竞争,为了尽快投入实用,回报大家的期待,需要跨越的障碍还有很多。