近期,国际学术期刊Autophagy发表了中科院上海生命科学研究院/上海交大医学院健康所、中科院干细胞生物学重点实验室乐卫东研究组的研究成果Rapamycin treatment augments motor neuron degeneration in SOD1G93A mouse model of amyotrophic lateral sclerosis。本项研究发现早期脊髓运动神经元内特异性的自噬水平升高,同时首次报道自噬激活剂雷帕霉素加速肌萎缩侧索硬化症(ALS)模型小鼠的发病,并初步探讨其可能机制。
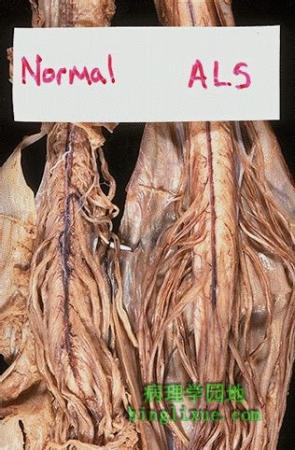
肌萎缩侧索硬化( ALS )很少见。它在中年开始发病,并且一直延续数年到死亡。
ALS运动神经元内蛋白质异常聚集可能是导致神经元选择性死亡的重要机制。自噬作为胞内蛋白质降解的主要途径,是现在蛋白质聚集类疾病的研究热点之一。自噬可能通过降解胞内聚集的蛋白质起到神经保护作用;但同时过度激活或者自噬途径的不完整可能加速神经元的死亡。而自噬在ALS发病过程及运动神经元选择性死亡中所发挥的作用至今仍未有相关报道。
乐卫东课题组的科研助理张晓洁等科研人员利用经典的ALS转基因小鼠SOD1G93A小鼠,发现在转基因小鼠脊髓前角运动神经元内特异性自噬小体(AVs)数目增加,而且神经元轴突内增加要早于胞内,提示运动神经元内自噬水平的特异性改变。进一步利用经典的自噬激活剂雷帕霉素作用于转基因小鼠后发现,其能够加速疾病进程,促进小鼠的死亡。同时雷帕霉素能够加重运动神经元内线粒体损伤,激活凋亡的发生。更有意思的发现是,雷帕霉素在激活运动神经元内自噬的同时不能减少胞内SOD1蛋白的聚集,且伴有自噬通量标记p62蛋白的异常改变,结果提示ALS转基因小鼠内可能存在自噬通量的异常即自噬通量完整性的改变。
研究结果首次报道了自噬激活剂雷帕霉素对SOD1G93A转基因小鼠疾病进程的影响并探讨了其可能机制。首次提出ALS存在自噬完整性异常这一科学问题,为研究自噬与ALS及其他蛋白聚集性疾病发病之间的关系指明了新的方向。
该项工作得到了国家科技部、国家基金委以及上海市科委经费的支持。







