microRNA是内源性和短的非编码单链RNA(18-23个核苷酸),参与信使RNA的转录后抑制。由于miRNA参与细胞增殖、分化和细胞死亡等各种生物学过程,因此失调的miRNA与癌症等疾病的发病机制密切相关。在基于液体活检的癌症诊断、预后和监测中,探索循环miRNAs是一种很有前景的策略。一个障碍是高性能检测生物样本中miRNA的挑战,因为它们的长度短,在miRNA家族中序列相似性高,在不同细胞类型和生物流体中的浓度范围大,以及相关的起源和载体的多样性。因此,迫切需要超灵敏、特异和稳健的生物测定和传感器,以促进临床上可行的疾病miRNA生物标志物的开发。
逆转录定量聚合酶链式反应(RT-qPCR)已成为检测miRNA的金标准工具。与长RNA物种(如mRNA)不同,短miRNA需要特殊的RT过程来结合有助于PCR扩增和检测的扩展序列。已经开发了许多等温分析来推进miRNA检测,包括滚环扩增(RCA),指数扩增反应(EXPAR),环介导的等温扩增(LAMP),杂交链反应和催化发夹组装。尽管这些测定具有简单甚至无需仪器操作的优点,但也存在限制广泛临床应用的缺点,例如EXPAR和LAMP的非特异性扩增和高背景信号,以及杂交链反应和催化发夹组装的相对较慢的动力学和低灵敏度。其他标准技术,如微阵列、NanoString和测序,需要复杂的仪器或具有复杂的分析工作流程、高操作成本和有限的分析性能,这阻碍了它们在临床诊断中的广泛应用。
近日,一组来自美国的研究团队在杂志Nature biomedical engineering上发表了一篇题为“A one-pot isothermal Cas12-based assay for the sensitive detection of microRNAs”的文章。在这篇文章中,研究团队报道了一种一步、一锅等温CRISPR-Cas12a检测方法(EXTRA-CRISPR),用于快速特异性检测miRNA,其灵敏度与RT-PCR相当。作者将EXTRA-CRISPR测定用于量化细胞外囊泡(EV)中的miRNA生物标志物(miR-21、miR-196a、miR-451a和miR-1246),用于基于液体活检的胰腺导管腺癌(PDAC)诊断,并通过对相同临床样本进行平行RT-qPCR分析,严格验证了EXTRA-CRSPR测试的分析和诊断性能。结果表明,该技术可能有助于推进miRNA检测和miRNA生物标记物的临床开发,以用于基于液体生物检测的癌症诊断和预后。

图片来源:Nature biomedical engineering
EXTRA-CRISPR测定的原理
图片 EXTRA-CRISPR检测被设计为三酶级联,利用CRISPR-Cas12a系统的核酸剪切活性(顺式切割和反式切割功能),将线性RCA转化为用于miRNA检测的指数扩增方法。简言之,Cas12a-RNP可以通过其顺式活性结合并切割RCA的长ssDNA扩增子,从而产生许多含有靶序列的二级引物来启动随后的RCA循环,从而导致靶的指数扩增。同时,扩增子激活的Cas12a RNP非特异性切割ssDNA报告子以产生和放大荧光信号。
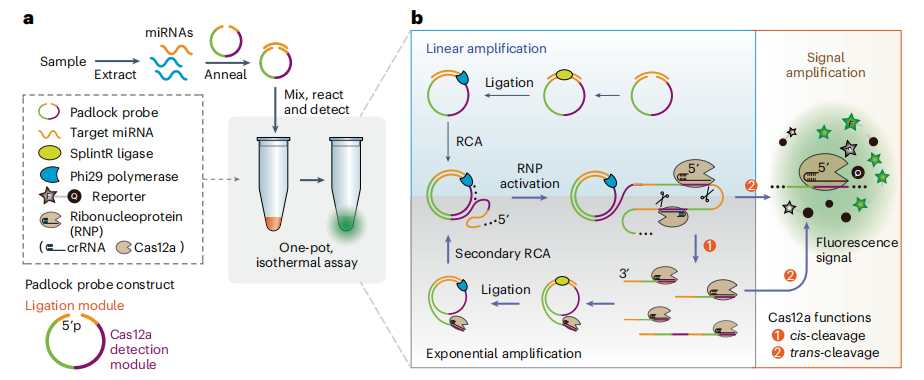
EXTRA-CRISPR测定的原理和工作流程(图片来源:Nature biomedical engineering)
EXTRA-CRISPR测定法的优化和表征
图片 作者优化了EXTRA-CRISPR测定法的padlock探针结构、连接酶、变性退火步骤、RCA相关缓冲液添加剂、聚合酶浓度、CRISPR组分如RNP和报告子浓度。优化后的EXTRA-CRISPR测定法的分析性能通过金标准RT-qPCR的平行测量得到了系统验证。与商业miRCURY LNA miRNA PCR试剂盒相比,EXTRA-CRISPR一锅法检测灵敏度相当,按照3小时实验流程其LOD为1.57 fM。
为了评估此方法的特异性,作者检测了许多非靶miRNA,包括一个在padlock-1连接位点具有单核苷酸错配的合成miR-21和8个1 pM的人miRNA。这些测试产生的信号水平约为miR-21信号的2%,甚至更低(如下图k),显示了优异特异性。对于从连接位点偏移三个核苷酸的单个错配,仍然可以获得相当好的特异性,非特异性信号水平约为25%。总的来说,结果验证了一锅EXTRA-CRISPR测定法,该测定法使用适当设计的padlock探针以个位数的飞摩尔敏感性和单碱基特异性快速检测miRNA。
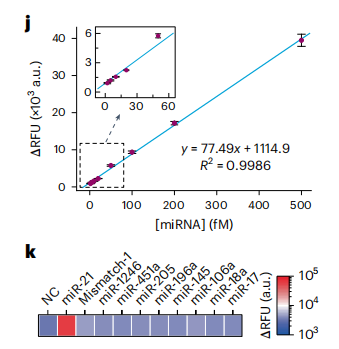
一锅法EXTRA-CRISPR miR-21测定的优化(图片来源:Nature biomedical engineering)
EV-miRNAs定量分析EV衍生的miRNA
图片 作者采用了EXTRA-CRISPR测定法来检测用于诊断PDAC的小EV(sEV)miRNA,为此,使用细胞培养基和人血浆样品分离sEV并提取短RNA,然后使用一锅EXTRA-CRISPR和两步RT-PCR测定进行平行测量在PDAC中失调的miRNA包括miR-21,miR-196a,miR-451a和miR-1246。通过EXTRA-CRISPR检测三种miRNA的校准图,从中确定miR-196a LOD为1.35 fM(5–500 fM线性范围),miR-451a为4.14 fM(5–500 fM线性范围)和miR-1246为7.96 fM(20–500 fM线性范围)。这些LOD与标准RT-qPCR测定的LOD相当(下图c)。EXTRA-CRISPR测定也显示出对四个miRNA靶标的高度特异性检测,单个padlock探针和三个非靶标之间的交叉反应性最小(下图d)。总的来说,这些结果证实了EXTRA-CRISPR方法有优异的敏感和特异性。
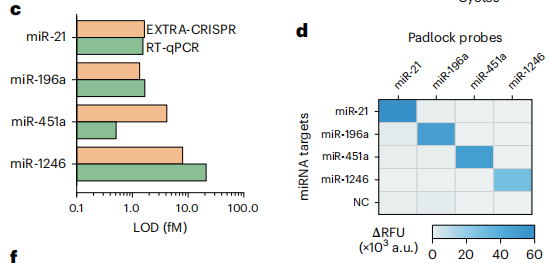
EV衍生的miRNA的定量分析(图片来源:Nature biomedical engineering)
EV-miRNAs定量分析在胰腺癌症诊断中的应用
图片 接下来评估了EXTRA-CRISPR分析法,以测量无癌对照组(n = 15) 和PDAC患者(n = 20) 的血浆样本。使用EXTRA-CRISPR测量EV miRNA,同时量化miR-21、miR-196a、miR-451a和miR-1246的水平。如图e所示,每个受试者的四种血浆EV miRNA标记物的浓度,它们在PDAC队列中的表达升高,与之前的研究一致。与单个标记物相比,EV Sig(miR-21、miR-451a和miR-1246的加权线性组合)提高了区分PDAC组和健康组的能力。AUC值范围从miR-196a的0.677到miR-451a的0.793。EV-Sig小组极大地提高了诊断能力,AUC为0.853。
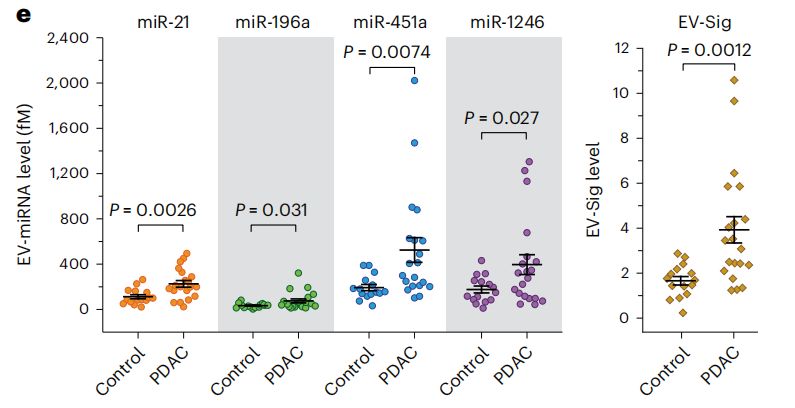
EV-miRNAs定量分析在胰腺癌症诊断中的应用(图片来源:Nature biomedical engineering)
用于POC测试的智能手机型EXTRA-CRISPR分析
图片 为了测试POC应用,作者试图建立一个低成本、便携式智能手机的EXTRA-CRISPR检测系统。这个原型是由3D打印的身体部件、蓝色LED管、光学滤波器和加热板组成(下图a)。将智能手机安装在设备上以获取荧光图像,然后对其进行分析以测量荧光强度。
作者首先评估了等温EXTRA-CRISPR反应的POC原型,并与商业qPCR热循环仪进行了比较。结果显示,当检测从四名对照供体和四名PDAC患者的血浆样本中分离的sEV中的标志物,POC设备能够检测三种sEV miRNA标记物的差异水平,并区分PDAC组与对照组,这与使用qPCR 等温测试的诊断结果一致。
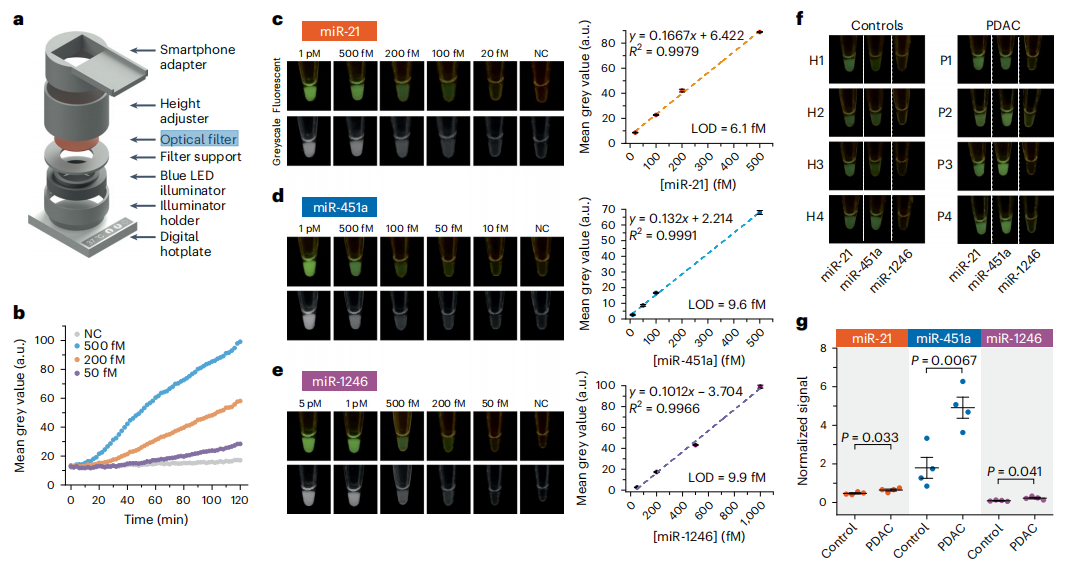
评估用于低成本POC测试的EXTRA-CRISPR测定(图片来源:Nature biomedical engineering)
用于POC测试的EXTRA-CRISPR-LFA分析
图片 EXTRA-CRISPR测试也可与侧流分析相结合(EXTRA-CRISPR-LFA)。下图i显示了使用EXTRA-CRISPR-LFA进行miRNA检测的结果,其显示了随着靶浓度增加,测试线的强度增加。与荧光检测模式相比,LFA检测显示定量分析性能下降,表现为校准图的线性下降,100 fM LOD和<2-log检测范围。尽管如此,EXTRA-CRISPR-LFA测试在miRNA检测方面大大优于现有的LOD在皮摩尔水平的LFA方法。
使用相同的患者样本测试智能手机设备,结果证明了EXTRA-CRISPR-LFA测试对sEV miRNA的无仪器临床分析的适用性。在这三种标记物中,sEV miR-451a的LFA检测产生了最高的视觉信号(下图j)和最佳的诊断性能(下图k)来检测PDAC样本。总的来说,对两种常用的POC检测模式的原理验证研究表明,EXTRA-CRISPR技术有潜力成为开发新的低成本POC诊断测试的适应性工具。
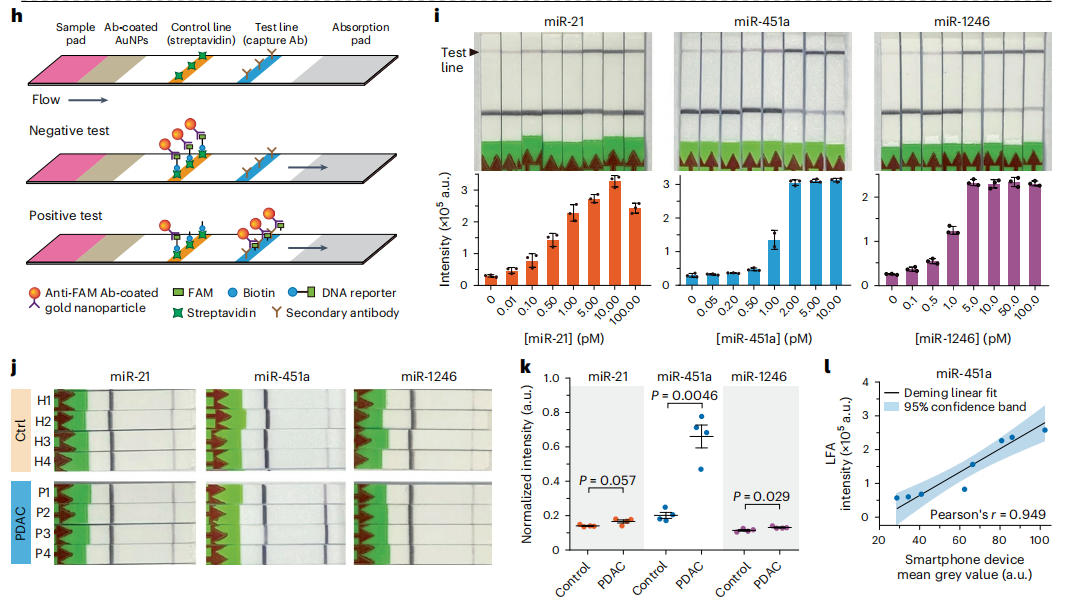
用于POC测试的EXTRA-CRISPR-LFA分析(图片来源:Nature biomedical engineering)
总结与讨论
图片 EXTRA-CRISPR具有灵敏和特异的分析性能、易于操作、快速反应和低成本的特点,为临床样本中的miRNA分析提供了一种替代标准RT-qPCR的有竞争力的选择。该方法的简单性将极大地促进未来仪器或微流体的小型化和集成,以完全自动化工作流程,进一步提高分析吞吐量和再现性,并减少样品消耗和周转时间。
EXTRA-CRISPR检测与现有的基于CRISPR的生物传感方法有三个主要区别。首先,它同时利用了CRISPR–Cas12a系统的顺式切割和反式切割活性的策略。其次,通过设计模块化padlock探针设计和反应动力学,将靶介导的连接、RCA、Cas12a结合和核酸切割的多种反应整合到一起,创建了一步单管等温分析。第三,这种一锅等温miRNA检测提供了与标准RT-qPCR相当的分析性能,包括具有飞摩尔检测极限的高灵敏度、单核苷酸特异性和快速灵活的周转。最后,一锅EXTRA-CRISPR技术极大地简化了分析工作流程,消除了对专用仪器的需求,为POC诊断提供了一种适应性强的模式。
本文转载自“小桔灯网”