最近的研究表明,高度突变的Omicron变体可以逃避大多数来自恢复期患者或完全接种疫苗个体的抗体。令人遗憾的是:在大多数接种两剂科兴灭活疫苗的中国人群中,没有或检测不到针对Omicron的中和抗体[1][2]。
辉瑞/BioNTech的mRNA疫苗BNT162b2在滴度和针对Omicron的保护方面显著优于同源加强剂量。然而,这种编码SARS-CoV-2完整S蛋白的商业mRNA疫苗在中国大陆尚不可用。编码SARS-CoV-2 S蛋白受体结合域(Receptor Binding domain,RBD)的“中国制造”mRNA候选疫苗AWcorna(原名ARCoV)正在多中心III期试验的最后阶段进行测试。近期,研究团队公布了ARCoV的临床数据。
科兴疫苗面对Omicron,接种者体内无有效抗体
2022年1月20日,香港大学和香港中文大学研究团队在Nature Medicine发表题为“Neutralizing antibodies against the SARS-CoV-2 Omicron variant BA.1 following homologous and heterologous CoronaVac or BNT162b2 vaccination”的研究成果(图1)[1]。研究发现针对Omicron,仅有3%的接种了三剂科兴疫苗的人,体内中和抗体滴度达到防护阈值。但是,80%的接种了BNT162b2的人,体内中和抗体滴度可达到防护阈值。研究团队建议使用科兴疫苗的国家应考虑使用mRNA疫苗加强剂来应对Omicron的传播。

图1 研究成果(图源:Nature Medicine)
在此项研究中,使用的SARS-CoV-2病毒是2020年1月分离的WT(Wild Type)病毒、2021年11月13日分离的Omicron变体BA.1和2021年6月分离的Delta谱系病毒。研究人员比较了接种疫苗的个体、感染恢复期个体和突破性感染个体血清中对WT、Omicron变体BA.1和Delta的PRNT50(Plaque Reduction Neutralization antibody Titer)和GMT90(Geometric Mean Titer)结果。
研究人员评估了未感染过COVID-19人在接种两剂辉瑞mRNA疫苗(BNT162b2,n=31)、接种两剂科兴灭活疫苗(CoronaVac,n=30)、接种三剂CoronaVac(n=30)、接种三剂BNT162b2(n=25)、接种两剂科兴灭活疫苗后接种异源加强剂量的BNT162b2(n=30)以及感染过COVID-19人在感染后143-196天从COVID19中恢复(出现Omicron之前)且尚未接种疫苗(n=30)、接种过一剂BNT162b2的COVID-19恢复期患者(n=30)、接种过一剂CoronaVac的COVID-19恢复期患者(n=28)3-5周后的血清PRNT50和GMT90(表1)。此外,对2021年11月和2021年12月在香港发现的六名Omicron感染者在急性感染和康复期间收集的血清进行了分析。
表1 受试者年龄、性别及接种后3-5周对比WT或Omicron变体BA.1的几何平均PRNT50滴度
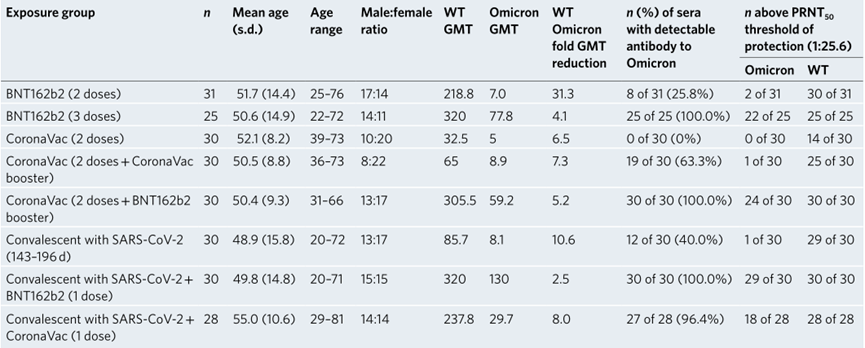
表格来源:[3]
研究结果(图2):
1、所有受试者对Omicron变体的抵抗力明显低于对WT病毒的抵抗力
在受试者中,相对于WT病毒的GMT,接种两剂BNT162b2疫苗对Omicron的GMT减少了31倍,两剂CoronaVac疫苗对Omicron的GMT减少了6.5倍,COVID-19恢复期血清对Omicron的GMT减少了10.6倍。
2、两针对Omicron的保护效力:BNT162b2为7%,CoronaVac为0
在31位接种二针BNT162b2人中,有2位的中和抗体对Omicron变体防护达到了阈值。在30位接种二针CoronaVac的人中,0位中和抗体达到Omicron变体的保护阈值。
3、同源剂量三针保护效力:三针BNT162b2为88%,三针CoronaVac为3%
在接种三针BNT162b2的25位疫苗接种者中,22位恢复了Omicron变体PRNT50抗体的保护阈值,但在接种三针CoronaVac的30位疫苗接种者中,只有1位恢复保护阈值。
4、异源剂量三针保护效力:2针CoronaVac+BNT162b2为80%,恢复期+1针BNT162b2为97%,恢复期+1针CoronaVac为64%
5、接种后6个月内抗体水平:BNT162b2为63%,CoronaVac为7%
在接种后5-5.8个月时,接种BNT162b2的30人中有19人PRNT50滴度>25.6,接种CoronaVac的28人中只有2人能达到此防护水平。
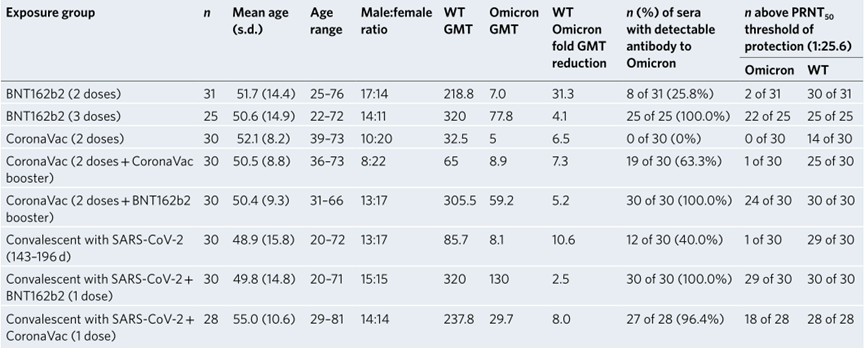
图2 研究成果(图源:[1])
研究结果表明,两剂BNT162b2或CoronaVac疫苗在接种后3-5周能引发针对Omicron变体的低中和抗体。两剂BNT162b2或CoronaVac后的同源或异源BNT162b2加强剂量可在3-5周提高针对Omicron变体的中和抗体水平。但是,在大多数接种三剂CoronaVac体内均未能引发对Omicron的中和抗体反应。研究建议:使用CoronaVac疫苗的国家可能需要考虑使用mRNA疫苗加强剂来应对Omicron的传播。然而,CoronaVac先前已被证明可以引发更广泛的病毒特异性T细胞反应,这可能会弥补中和抗体保护的一些损失。
国产新冠mRNA疫苗或安全有效
2022年5月31日,云南省疾病预防控制中心、军事医学科学院、广州呼吸健康研究所、北京食检院、华威生物科技有限公司和苏州安博生物科技有限公司研究团队在预印本平台medRxiv发布题为“Safety and superior immunogenicity of heterologous boosting with an RBD-based SARS-CoV-2 mRNA vaccine in Chinese adults”的研究成果(图3)[2]。研究表明中国成年人接种新冠病毒mRNA疫苗ARCov进行异源加强产生的中和抗体优于灭活疫苗。ARCov具有较好的安全性和免疫原性,可在中国作为新冠病毒的异源增强疫苗。

图3 研究成果(图源:medRxiv)
在此项随机临床试验中,以300名接种过两剂灭活疫苗(科兴疫苗,CoronaVac)的中国成年人为实验对象。在接种灭活疫苗6个月后,受试者被随机分配到ARCov(n=200;异源)或CoronaVac(n=100;同源)加强组。试验开始时受试者的BMI(Body Mass Index)、生命体征、合并症等差异均无统计学意义(P>0.05)。所有受试者在加强免疫前或加强免疫后0天、14±2天、28±2天连续完成入组疫苗接种和3次血液检查。随后,通过基于标准细胞病变效应(Cytopathic Effect,CPE)和ELISA(Enzyme Linked Immunosorbent Assay)在加强前、加强后14天和28天分别评估针对WT SARS-CoV-2和VOC(Variants of Concern)的中和IgG(Immunoglobulin G)抗体滴度。WHO(World Health Organization)标准IgG抗体被用作所有血清学检测的参考样本。
研究结果:
1、与灭活疫苗相比,ARCov对WT SARS-CoV-2的中和滴度增加了66.59倍
在两组参与者中,针对WT SARS-CoV-2的活病毒中和滴度均低于检测限,但是,ARCov加强剂将WT SARS-CoV-2的中和滴度增加了66.59倍。在加强剂后14天和28天,GMT分别达到293.9和242.4(WHO参考值1:139),而CoronaVac组的GMT分别仅为89.1和64.3。
2、与灭活疫苗相比,ARcov对Omicron的抗体更持久
在ARCov和CoronaVac进行第三次加强免疫后,针对Delta变体的中和抗体滴度也显著增加,而ARCov组的GMT在14天和28天时分别比CoronaVac组高5.1和6.5倍。此外,18-59岁和60岁以上参与者的增长趋势相似。尽管在两组中针对Omicron变体的中和抗体滴度与针对WT病毒的相比均显著降低,但针对Omicron的GMT在ARCov加强后28天保持为28.1,而CoronaVac加强组中的GMT仅为6.4。ARCov加强组中83.75%的参与者达到了针对Omicron的中和抗体滴度阈值(1:8),而CoronaVac加强组中只有35%的参与者达到了阈值。
3、两组受试者均未报告严重不良事件
在接种疫苗后的30分钟内和0-14天的窗口内记录了请求的局部和全身不良事件(Adverse Events,AE),并在加强疫苗接种后0-28天内记录了主动的AE。对于这两种疫苗,注射部位疼痛是报告最多的局部AE(发生率,IR:ARCov为17%,CoronaVac为2%;P<0.0001)。发热是最常见的全身性AE(IR:33.5%),其次是ARCov组的头痛(IR:26.0%)和肌肉疼痛(IR:7.5%)。在ARCov组的200名参与者中,共有8名受试者报告了3级发烧(IR:4%)。对于CoronaVac组,头痛是最常见的全身AE(IR:7.0%),其次是发热(IR:4.0%)。
总的来说,此项研究表明用ARCoV进行的第三剂异源加强是安全的,并且对Delta和Omicron变体均具有潜在的保护作用。尽管ARCov加强剂在预防SARS-CoV-2和其他VOC感染方面的疫苗有效性仍有待确定,但针对WT和VOC的强效中和抗体的诱导,以及可负担的安全性,支持紧急使用ARCov在中国作为异源加强针疫苗。目前,需要一种更有效的mRNA疫苗和改进的加强剂策略,以满足阻止中国正在进行的Omicron疫情和全球COVID-19大流行的紧迫和巨大需求。
2022年1月24日,ARCov的I期试验结果发表于The Lancet,I期试验结果表明ARCoV在所有五组剂量下安全性耐受性良好,并可诱导强烈的免疫反应(图4)[3]。但是,I期试验仅包括20名18-59岁的成年人(15 μg组),而此项研究招募了200名参与者,其中包括10名60岁以上的受试者。样本量的扩大和疫苗制造技术的改进有助于提高研究中观察到的安全性。正在进行的有28000名参与者的国际III期试验将提供有关ARCov安全性方面更有意义的数据。

图4 研究成果(图源:The Lancet)
在大多数中国人群中几乎没有或没有检测到针对Omicron的有效抗体,为此,世界卫生组织和中国国家卫生委员会均建议普通中国民众接种第三剂加强针。在从不同技术平台生产的COVID-19疫苗中,mRNA疫苗作为同源或异源加强剂是最合理的选择。
题图来源:沃森生物,仅用于学术交流。
撰文|文竞择
排版|乔维钧
参考资料:
[1]Cheng, S. M. S. et al. Neutralizing antibodies against the SARS-CoV-2 Omicron variant BA.1 following homologous and heterologous CoronaVac or BNT162b2 vaccination. Nat Med 28, 486-489, doi:10.1038/s41591-022-01704-7 (2022).
[2]Liu X Q, Li Y H, Wang Z F, et al. Safety and superior immunogenicity of heterologous boosting with an RBD-based SARS-CoV-2 mRNA vaccine in Chinese adults. medRxiv 2022.05.30.22275753; doi: https://doi.org/10.1101/2022.05.30.22275753
[3]Chen GL, Li XF, Dai XH, et al. Safety and immunogenicity of the SARS-CoV-2 ARCoV mRNA vaccine in Chinese adults: a randomised, double-blind, placebo-controlled, phase1 trial. Lancet Microbe. 2022 Mar;3(3):e193-e202. doi: 10.1016/S2666-5247(21)00280-9. Epub 2022 Jan 24. PMID: 35098177; PMCID: PMC8786321.