如今,肿瘤免疫疗法已进入研究爆发期,自从 ipilimumab 成为美国FDA批准的第一款免疫检查点疗法(immune check-point blockade therapy,ICB therapy)用药后,肿瘤免疫疗法的一大重要分支 ICB疗法便进入了发展黄金期,针对PD-1、PD-L1、CTLA-4等免疫检查点的抑制剂迅速走入人们的视野,在治疗黑色素瘤、非小细胞肺癌、肾癌等方面得到了长足的进步,也为癌症患者们带来了新的希望。
不过,值得注意的是,目前研究显示,在患有黑色素瘤、非小细胞肺癌以及肾癌的患者中,仅有不到30%的人群能够通过这些抑制剂得到良好的治疗,而患有其他癌症的患者们则对ICB疗法无法产生有效应答。科学家们必须开拓新的思路解决这一问题,才能在攻克癌症难题上更上一层楼。
近日,来自中国科学院、中山大学、哈佛医学院、塔夫茨大学、马里兰大学等高校的中美科学家们,在 Science Tranlational Medicine 上联合发表题目为“Reactivation of the tumor suppressor PTEN by mRNAnanoparticles enhances antitumor immunity in preclinical models”的研究文章,研究提出了为肿瘤免疫疗法保驾护航的新方向——通过脂质聚合纳米颗粒将 PTEN mRNA递送进肿瘤细胞内,可以有效诱导肿瘤细胞自噬,并通过释放损伤相关模式分子(damage-associated molecular patterns,DAMPs)来触发细胞死亡相关免疫的激活,从而提升ICB疗法的疗效。

DOI: 10.1126/scitranslmed.aba9772
研究指出,PTEN基因是一种目前被广泛研究的肿瘤抑制基因,它能够直接参与抗肿瘤免疫系统的调节。很多临床数据已经表明,PTEN的缺失与肿瘤部位T细胞浸润减少以及PD-1阻断治疗的不良反应或耐药性显著相关。为探究其中的关系,研究人员以PTEN缺失的前列腺癌细胞和PTEN变异的黑色素瘤细胞为研究对象,采用目前火热的mRNA技术和脂质聚合纳米颗粒递送方式进行了系统研究。
研究人员首先开发了一种脂质-聚合杂化纳米颗粒(NP)平台,并对脂质纳米颗粒在PTEN mRNA 封装以及维持递送稳定性等多方面进行了严格的验证,被封装好的 PTEN mRNA 被命名为mPTEN@NPs。
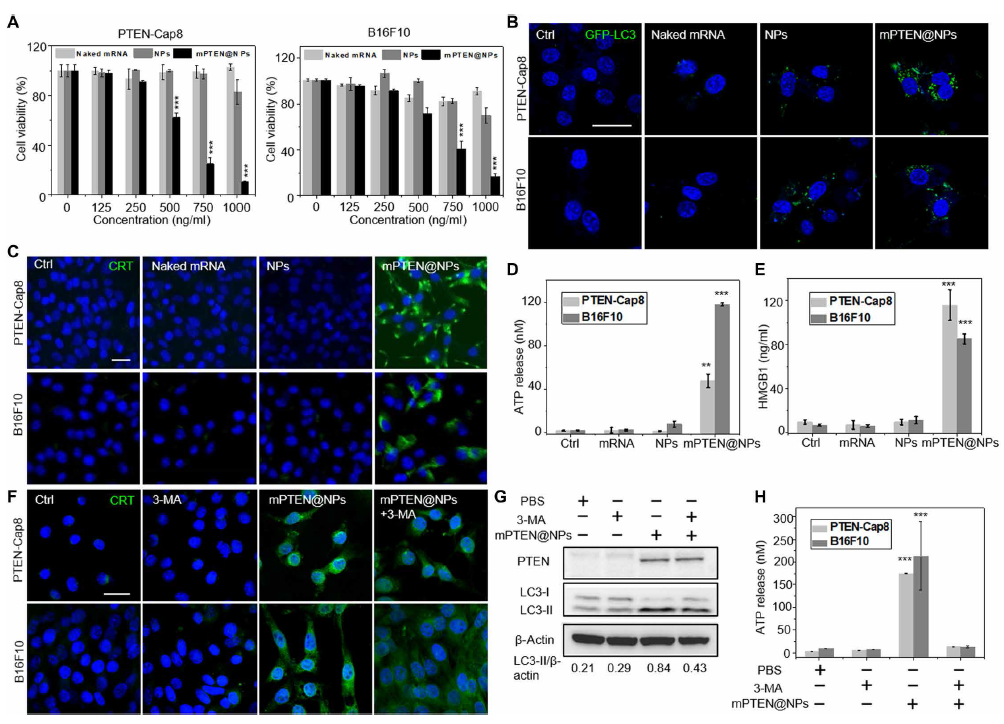
接下来便是试验阶段,研究人员首先进行了体外试验,将样本分为4组,分别为控制组、未封装的PTEN mRNA、无PTEN mRNA的脂质纳米颗粒以及mPTEN@NPs,接着,采用蛋白质印迹法(Western-blot)来确认PTEN的激活是否能够诱导肿瘤细胞的自噬。结果显示,mPTEN@NPs疗法的使用导致了自噬标志物LC3-II以及p62蛋白的增加,这表明,mPTEN@NPs 能够诱导自噬体的形成,并可导致其在细胞内的积聚。同时,试验验证了研究人员关于PTEN能够诱发DAMPs释放的猜想,其结果表明,自噬体的积聚也导致了DAMPs以及肿瘤抗原的释放与增加,从而引起了肿瘤细胞的免疫原性细胞死亡(immunogenic cell death,ICD)。
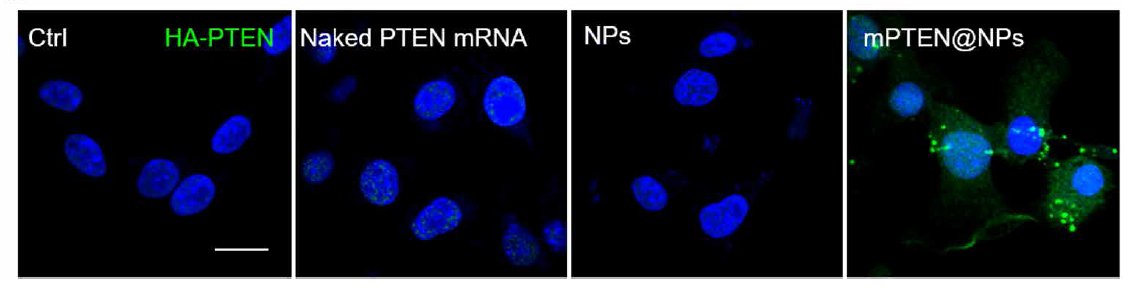
荧光免疫检验法下的PTEN表达,从左至右分别为未进行治疗的控制组、未进行封装的PTEN mRNA、无PTEN mRNA的脂质纳米颗粒、mPTEN@NPs
mPTEN@NPs疗法提高了肿瘤细胞的死亡
在体外试验取得了可喜进展后,研究人员又进行了小鼠体内试验。当小鼠体内的肿瘤细胞长到一定规模时,研究人员将其分为3组,分别采用生理盐水、无PTEN mRNA的脂质纳米颗粒以及mPTEN@NPs进行注射治疗,结果显示,与其他两组对照组相比,在采用了mPTEN@NPs进行治疗的小鼠体内,其肿瘤内的CD3+CD8+ T细胞显著增加,同时,在肿瘤免疫系统中扮演重要角色的Treg和MDSCs细胞数量也呈现上升趋势,而它们的增加,促进了免疫抑制肿瘤微环境的产生,这些实验现象都证明,mPTEN@NPs 能够触发抗肿瘤免疫的激活,并逆转免疫抑制肿瘤微环境,从而诱发肿瘤细胞的死亡。
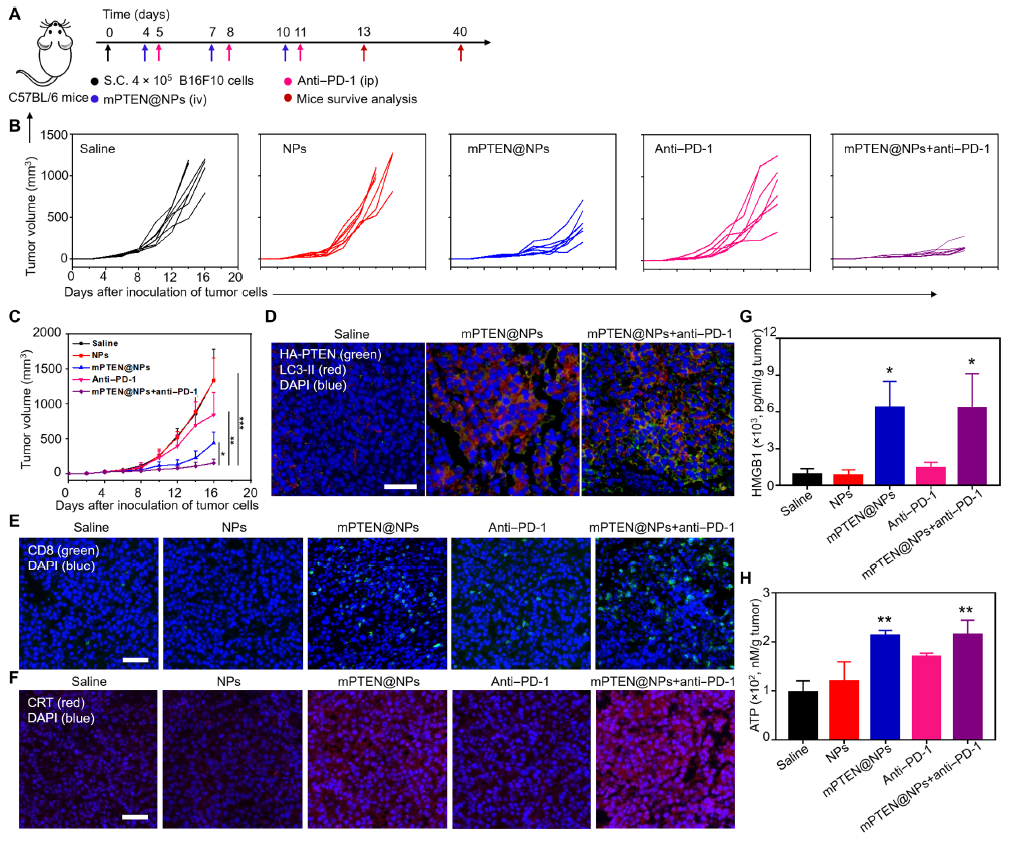
由于以往的研究已经证实,PTEN的缺失会导致抗PD-1靶向疗法的不良反应,因此,研究人员在患有PTEN变异的黑色素瘤小鼠体内进行试验,以探求PTEN的修复是否能够促进抗肿瘤免疫系统的激活。患有肿瘤的小鼠分别在第4天、第7天以及第10天采用生理盐水、无PTEN mRNA的脂质纳米颗粒以及mPTEN@NPs进行注射治疗,同时,进行mPTEN@NPs治疗的小鼠也将在第5天、第8天和第11天同时接受抗PD-1治疗。
在经过3轮治疗后,mPTEN@NPs+anti-PD-1的联合疗法实现了更好的抗肿瘤疗效,这一疗法促进了抗肿瘤免疫应答的增加以及免疫抑制肿瘤微环境的改善,同时也增强了CD8 T细胞在肿瘤组织内的渗透作用,而这些试验结论同样在PTEN缺失的前列腺癌小鼠模型中得到了证实。
mPTEN@NPs+anti-PD-1联合疗法试验流程与结果分析
以抗CTLA-4 和抗PD-1/PD-L1作为一线疗法来治疗非小细胞肺癌以及黑色素瘤,已经被证实为一种非常有力的癌症治疗方法,即使会出现疗效受限的情况,目前医药界也会使用ICB疗法与传统化疗相结合的联合疗法来提升免疫应答,但是,传统化疗的极大副作用是我们无法避免的,因此,通过mRNA纳米药物修复肿瘤抑制因子以提高ICB疗法的敏感性,或许将为治疗多种恶性肿瘤提供更加有效的联合疗法。
参考资料:
[1]https://stm.sciencemag.org/content/13/599/eaba9772