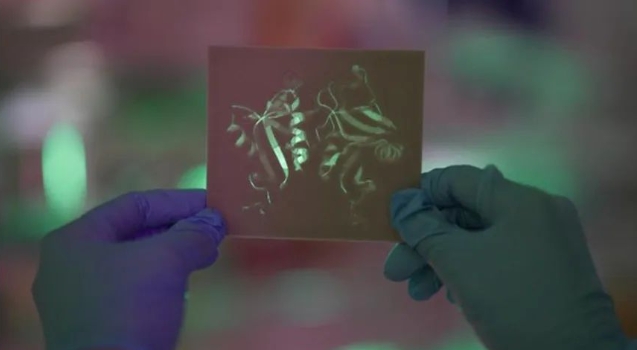
色素性视网膜炎(RP)是一种视网膜退行性变,由70多种不同的基因突变引起,影响了全球超200万人。这种疾病被称为不治之症,患者一经确诊,即便辗转治疗,最终也难逃失明的厄运。
近年来,随着现代医学技术的突飞猛进,基础医学尤其是免疫学、分子生物学以及遗传学的研究也朝着深度和广度挺进,使得一些遗传性疾病的基因诊断和治疗成为可能。然而面对早发性色素性视网膜炎,目前也仅有针对RPE65基因突变的基因替代疗法“Luxturna”可有效应对。
令人振奋的是,当地时间5月24日,匹兹堡大学(University of Pittsburgh)知名眼科专家José-Alain Sahel教授利用一种名为“光遗传疗法(optogenetic therapy)”的新型基因技术,首次帮助一名40年前就被诊断为视网膜色素变性的失明患者成功恢复部分视力。相关研究发表于权威学术期刊《Nature Medicine》上。

https://doi.org/10.1038/s41591-021-01351-4
光遗传疗法技术诞生于2005年,由斯坦福大学的科研人员首次在《Nature Neuroscience》 杂志中被提出。与传统的基因疗法不同,该疗法可通过将DNA插入神经元,利用光敏通道蛋白(ChR)使神经元响应光照,从而帮助所有光感受器受损患者重建光明。

https://doi.org/10.1038/nn1525
尽管色素性视网膜炎患者失去了视网膜感光细胞,但是他们的眼睛内仍然存在神经节细胞,可通过视神经将视蛋白将光转化为电信号传递给大脑。因此研究人员猜测或许可通过向眼内注射微生物视蛋白使患者恢复视力。
众所周知,利用病毒感染将外源光敏蛋白的遗传信息传递给靶细胞的方法是最方便快捷的,因此,得益于腺相关病毒(adeno associated virus,AAV)对大脑特异的组织嗜性,AAV成为光遗传研究中的重要工具。
基于此,在这项最新的研究中,研究人员将编码了光敏蛋白视紫红质“ChrimsonR”遗传指令、同时融合了红色荧光蛋白“tdTomato”的腺病毒载体(GS030-DP)通过玻璃体腔注入患者的眼内,以改造视网膜中央凹的神经节细胞,并使患者能感受到琥珀色的光。
患者注射微生物视蛋白4个月后,研究人员开始训练他们使用经工程改造的光刺激护目镜(GS030-MD)。这种护目镜自带一个专用摄像头,可以拍摄图像,并将视觉图像转换成光脉冲,光脉冲再被实时投射到视网膜上,从而激活被被改造的视网膜神经节细胞。
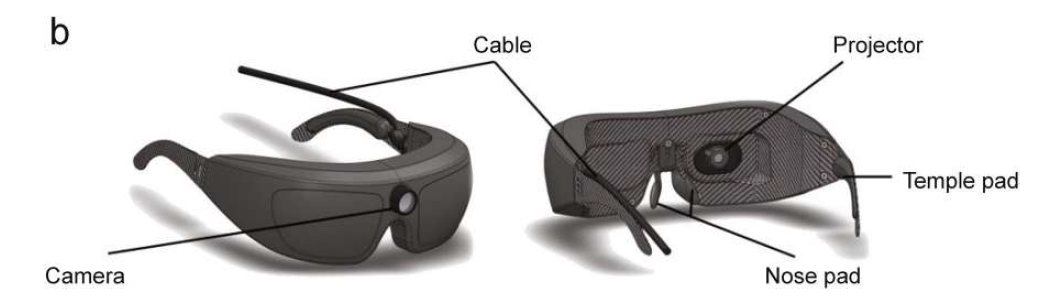
护目镜
为了验证视力恢复与神经元活动之间的联系,研究人员将视力评估与非侵入性脑记录技术“颅外多通道脑电图(EEG)”相结合,以读取患者整个皮质的神经元活动。

EEG记录
令人欣慰的是,经治疗后,随着神经节细胞稳定地表达光敏蛋白,患者的大脑也逐渐适应经过改造的视觉系统,并可准确的感知、定位、计数和触摸不同的物体。当研究人员在桌子上放置一些笔记本、杯子等物体后,患者不但能正确的识别物体数量,还能指出他们的位置。
不仅如此,在接受长达84 周、多达 15 次的随访后,研究人员惊喜的发现,该患者的视觉功能越来越完善,不仅可以看到人行道的斑马线,还能清楚的知道共有几条!
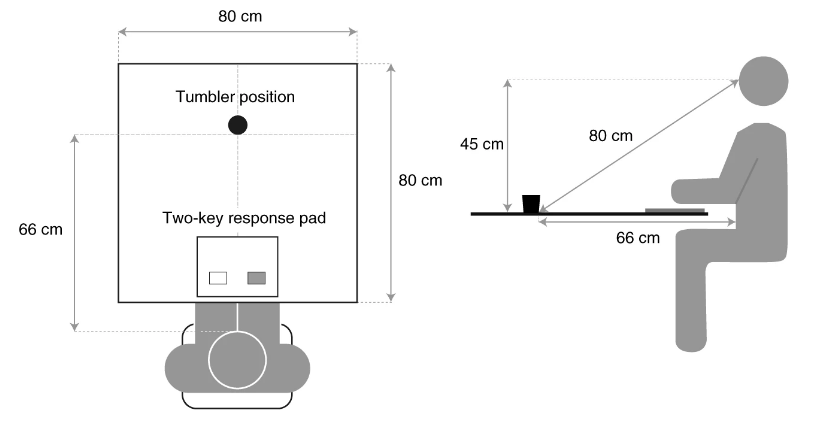
视觉检测任务
最后,为使患者的视力水平达到最佳状态,研究人员通过对EEG记录下的视觉信号进行光谱分析,找到了大脑皮层中视觉信息最丰富的区域,即大脑皮层中鉴别光线能力最强的区域“对侧枕叶皮层(the occipital cortex contralateral)”,使得失明患者被治愈的希望又更进一步。
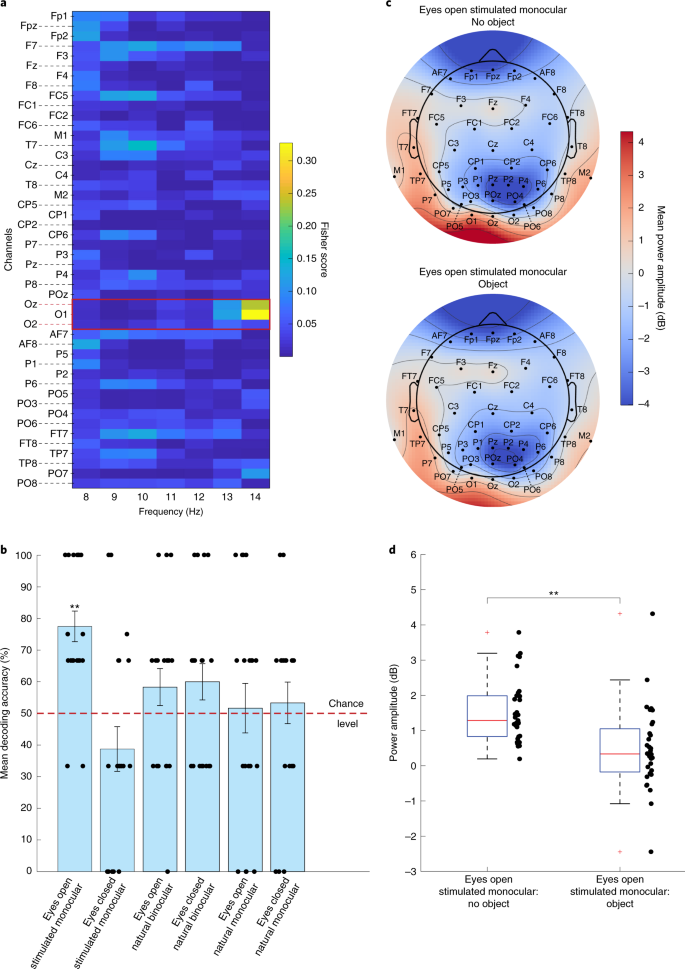
基于枕脑波振幅调制的脑电信号解码
据了解,这项突破性疗法的1/2a期临床试验“PIONEER”仍在进行中,未来,期待能有更多的新型基因疗法问世,让世界再无不治之症。
参考资料:
[1]https://www.nature.com/articles/s41591-021-01351-4#Sec1
[2]https://www.statnews.com/2021/05/24/scientists-use-optogenetics-for-first-time-to-help-blind-patient-see/