*本文节选自专题报告《PARP抑制剂前途无量》,系GBI原创,如需转载或引用文中内容,请联系授权。

今年8月,阿斯利康旗下多聚二磷酸腺苷核糖聚合酶(PARP)抑制剂Lynparza(olaparib,奥拉帕尼)获得了中国国家药品监督管理局(“国家药监局”)的上市批准,这一具有里程碑意义的决定显示了中国不断变化的药物行政监管环境。该药是第一个进入中国的PARP抑制剂,标志着可将卵巢癌转变为长期慢性病的新疗法正式登陆中国市场。该药物是在中国发布允许跨国公司使用国际试验数据支持上市申请新规后,第一个获批产品,彰显了国家药监局确保中国患者能够受益于最新模式转变类药物,尤其是治疗癌症药物的决心。
GBI经过研究发现,国内生物技术公司也加入了研发抗肿瘤PARP抑制剂的激烈竞争中,以 “快速跟随”(Fast-Follow)方式研究包括具有最佳同类药(best-in-class)潜力的化合物在内的产品,并探索在全球范围内扩大该新型药物治疗潜力。
中国PARP抑制剂发展情况
阿斯利康于2017年7月与默克达成协议,共同在全球范围内开发其奥拉帕尼 Lynparza (olaparib),该药于2018年8月在获得中国批准,维持治疗铂类敏感的卵巢癌患者,无论BRCA基因是否发生突变。该药的上市批准基于一项国际试验(SOLO2)数据。 这是中国2018年7月发布《接受药品境外临床试验数据的技术指导原则》后,第一个受益于该政策的进口药物,文件规定,境外临床试验数据应支持有效性和安全性评价,遵循ICH关于接受国外临床资料的种族影响因素(E5)要求,分析中国亚组与总体人群的一致性,以支持境外临床试验结果外推至中国人群。
中国正采取多项措施,提高抗癌药供应保障能力,很明显的一点就是一系列重磅抗癌药物在中国的上市,包括:PD-1抑制剂帕博利珠单抗注射液(Keytruda)和欧狄沃(Opdivo),以及辉瑞旗下首治疗乳腺癌的创新药(first-in-class)CDK4/6抑制剂帕博西尼 (Ibrance)。GBI SOURCE数据显示,截至目前,2018年在中国首次获批的37种新药中,有15种是抗癌药物。此外,今年中国发布了48个境外已上市临床急需新药名单,如果符合ICH指南的种族原则,不存在人种差异的,药品申请人可直接提出上市申请,而奥拉帕尼 Lynparza (olaparib)正是这48种可豁免临床直接上市的进口癌症药物之一,有希望加快开发其他适应症步伐。
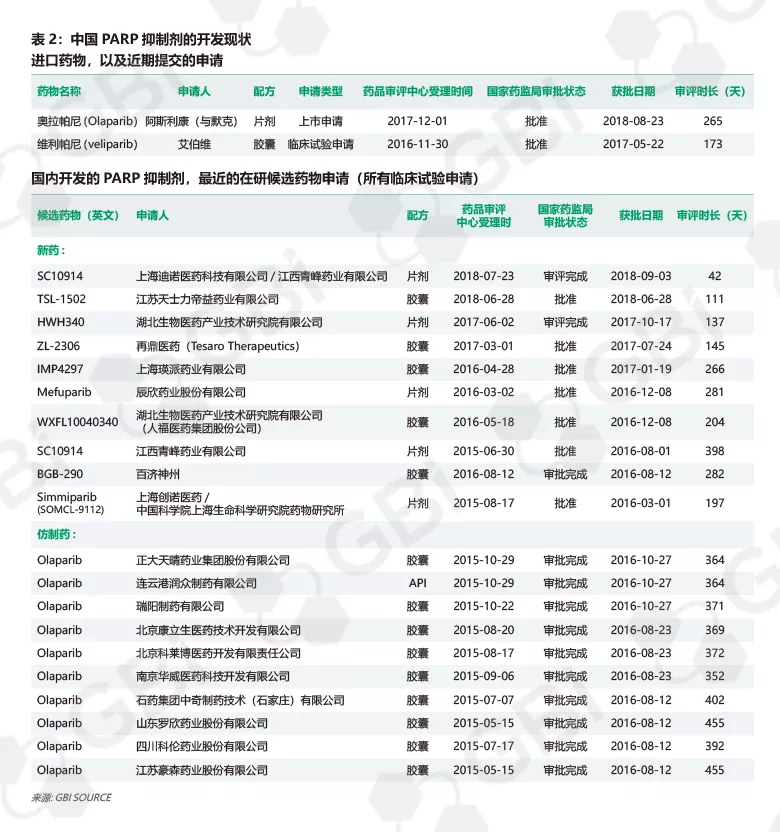
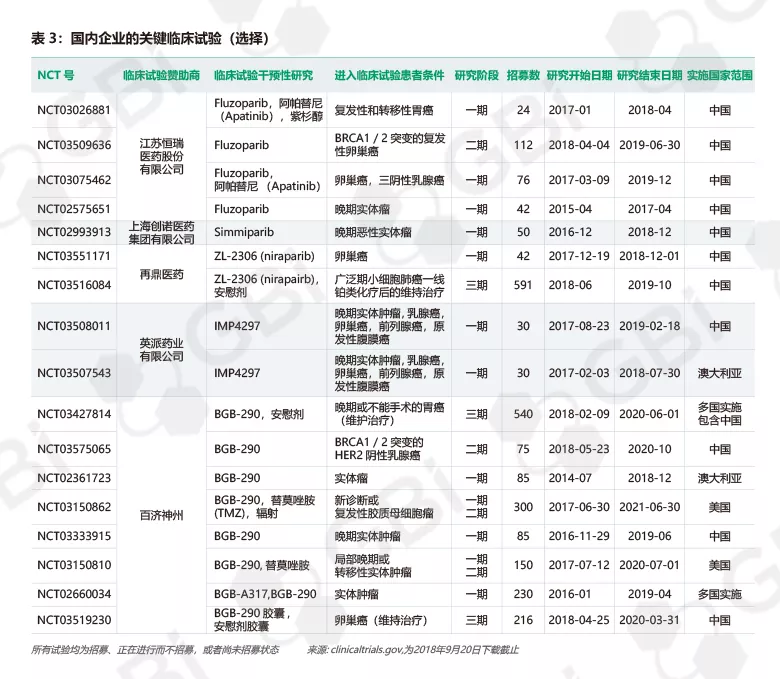
不过,奥拉帕尼独霸中国癌症药物市场的时日可能无多了。因为早在2015年,上海上海创诺制药有限公司(Acebright Pharma) 与上海药物研究所在中国首次提交了一款新型PARP抑制剂候选药物的上市申请,目前国内至少有11名新候选药物正在开发中(见表2)。国家药品监督管理局(NMPA)尚未公布江苏恒瑞医药 PARP抑制剂的信息,但clinicaltrials.gov显示该药正在进行三个临床试验(见表3)。另外,江苏豪森药业等10家公司已经提交了奥拉帕尼仿制药临床试验的申请。
 中国癌症治疗领域有望取得突破
中国癌症治疗领域有望取得突破
国内公司有希望在众多的候选药物中产生一款同类最优(best-inclass)药物。百济神州或将凭借其PARP抑制剂BGB-290成为国内公司的领头羊,与该公司其它领先候选药物相比,该药曾经是个无足轻重的小角色。Pamiparib在中国与全球同步进行的临床开发程度使人信服,其中一项国际临床试验将该候选药物与百济神州的PD-1抑制剂BGB-A317(tislelizumab;见表3)联合用药。 该公司今年早些时候启动了两项关键的III期临床试验,评估该药维持治疗中国卵巢癌患者;并于2018年7月启动一项全球临床试验, 使用该药作为对铂类一线化疗响应的无法手术的局部晚期或转移性胃癌(GC)患者维持治疗。在后一适应症上,百济神州的BGB-290可比国外药企抢先一步,外国公司迄今为止PARP抑制剂与化疗联合直接治疗胃癌的试验出乎意料地遭遇了失败,特别是阿斯利康2016年5月终止的GOLD临床试验。在百济神州精心设计了此项评估pamiparib作为维持疗法的临床试验,其主要终点为无进展生存期,旨在证明“可维持化疗反应而不产生相关毒副作用”(不过总体生存率仍然是一个重要的次要终点)。预计初步结果将于2020年6月公布。
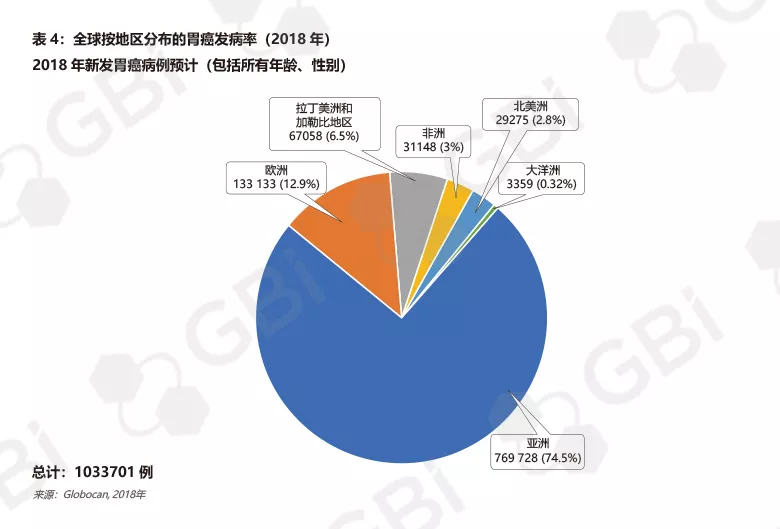
如果 pamiparib 在这些临床试验中取得了积极的结果,那么PARP抑制剂的中国市场前景将不可估量。胃癌是中国第三大常见癌症,预计2018年将有456,124例胃癌患者。该病在中国的治疗情况不尽人意,预计2018年将有390,182名患者死于该病(来源:Globocan)。PARP抑制剂作为一种小分子药物,相对便宜且易于患者服用,将受到中国医药监管部门的青睐。同时,中国企业将与全球同行共同致力于克服与骨髓抑制等毒副反应难题,通过更好地了解与该类药物相关的生物标志物可开发新的肿瘤适应症、 非肿瘤适应症,前景诱人。
 ……
……
附:《PARP抑制剂前途无量 》报告目录:
一、引言
二、PARP抑制剂研发历史回顾
三、以其人之道,还治其人之身
四、组合疗法的潜力
五、PARP抑制剂耐药性问题
六、中国PARP抑制剂发展情况
七、中国癌症治疗领域有望取得突破
如何获取完整专题报告?
1. GBI SOURCE企业用户可在公众号GBISOURCE数据库“个人中心”绑定账户信息后,通过“资讯报告-专题报告”直接查看;

2. GBI SOURCE企业用户也可登录网页版GBI SOURCE数据库,通过“资讯报告-专题报告”查看;
3. 非企业用户可转发本文到朋友圈,并回复公众号GBIHealth您的转发朋友圈截图、企业邮箱,我们会在24h内将报告发至您的邮箱。