只有母亲、没有父亲的小鼠能够正常发育、繁殖,图中它正在照顾自己的幼崽(图片来源:Leyun Wang)
10月11日,《Cell Stem Cell》期刊在线发表了这一篇题为“Generation of Bimaternal and Bipaternal Mice from Hypomethylated Haploid ESCs with Imprinting Region Deletions”的创新文章,由中国科学院动物研究所的李伟课题组、周琪课题组与胡宝洋课题组合作完成。他们利用单倍体干细胞和基因编辑技术,首次突破了哺乳动物同性生殖障碍。
具体而言,研究团队培育出具有两个母系基因组的孤雌小鼠。这些双亲是两个“妈妈”的小鼠能够发育成年,并且繁殖出下一代。
更重要的是,研究团队打破空白,第一次培育出“孤雄小鼠”——双亲是两个“父亲”。这些小鼠外观正常,可以自主呼吸。


论文的3位通讯作者:李伟研究员(左)、周琪研究员(中)和胡宝洋研究员(图片来源:中国科学院动物研究所)
同性生殖:不需要另一半?
同性生殖(unisexual reproduction)现象在自然界并不鲜有。不少爬行类、两栖类雌性动物可以在不交配的前提下依靠自己就能生育下后代,也就是“孤雌生殖”。 作为有性生殖的补充,孤雌生殖能在缺乏雄性的情况下,维持个体的繁衍与种群的更新。与之对应的“孤雄生殖”却极其罕见,迄今为止科学家们只在一种斑马鱼中发现了这一现象。
虽然我们尚不了解同性生殖背后的机制,但是对于哺乳动物而言,这两种生殖方式都不存在,至少在自然条件下无法实现。即便人工构建出孤雌或孤雄胚胎,它们都在发育早期就死亡了。
遗传印记:我们不一样?
为什么两个精子或者两个卵子无法结合发育成健康个体呢?究其原因,主要与遗传印记(genomic imprinting)有关。
基因印记是指附着在DNA、负责关闭基因表达的化学标签,属于表观遗传学修饰。某些特殊位点的基因受到印记的影响,只表达父源或者母源的等位基因,例如编码胰岛素的生长因子 2(IGF2 / Igf2)基因,只有来自父亲的IGF2基因能够表达,而来源于母亲的IGF2基因虽然序列无异,但是却处于关闭状态。
这意味着,只有同时携带父母双方的染色体才能实现互补,后代才能正常发育。这正是同性来源的胚胎无法正常发育的关键。
删除印记?实现孤雌生殖
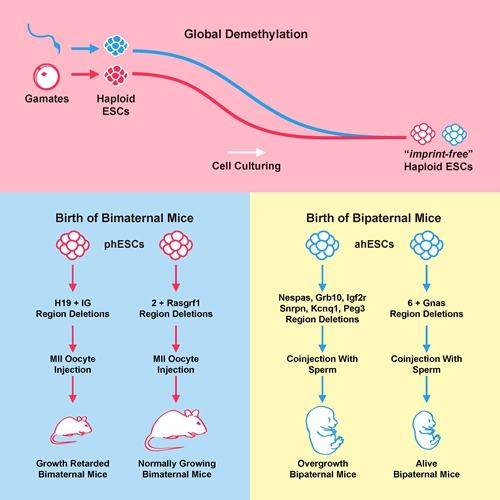
突破哺乳动物同性生殖障碍(突破来源:《Cell Stem Cell》期刊)
科学家们试图打破哺乳动物的同性生殖障碍,即删除印记(让母亲的特定基因正常表达,不依赖于父源的补充)。早前,来自日本的研究团队曾通过删除未成熟卵细胞中的2个印记控制区段,成功获得孤雌小鼠,首次实现了哺乳动物的孤雌生殖。
这一尝试为中国团队的进一步工作埋下了伏笔。2012年,动物研究所研究团队通过向没有细胞核的卵细胞注射精子,制造出染色体数目只有正常数目一半的小鼠胚胎干细胞。2013年,他们又从未受精的卵子中培育出单倍体胚胎干细胞(haploid embryonic stem cells),这些细胞携带更少的基因印记。2015年,科学家们将母源单倍体细胞注射到卵母细胞中,培育出来自两个母亲的小鼠,即实现了“孤雌生殖”。虽然由此而培育的幼鼠能够繁殖后代,但是它们总体上比野生小鼠小。
在最新的研究中,他们首先发现,携带两个印记区域缺失(与日本科学家工作相同)的单倍体干细胞培育出的小鼠在行为测试中表现异常,而且体型较小。为了让它们更接近于野生小鼠,研究团队随后又删除了Rasgrf1基因上游的印迹区域。Rasgrf1基因在同性生殖而来的小鼠以及野生型小鼠的大脑中表达不同。结果证实,这一选择很正确。删除来自雌性小鼠的单倍体胚胎干细胞中的3个基因印记区域之后,研究团队将其与另一只雌性老鼠的卵子结合,培育出新的胚胎(携带两个母亲的遗传物质)。由此产生的小鼠后代发育正常。
他们共培育出29只“孤雌小鼠”,这些小鼠在发育、行为、代谢和生育力上均与正常小鼠无异。其中,有7只健康生长至成年,并生下了自己的后代。
突破空白,培育孤雄小鼠
只有父亲,没有母亲?相比于孤雌生殖,孤雄小鼠的获得更为复杂。“最大的挑战是我们不知道孤雄繁殖是否可能存在。” 胡宝洋表示道。
为了找寻答案,他们利用了类似的方法,筛选并删除了来源于雄性小鼠的单倍体干细胞中的7个印记区。随后,他们将该干细胞的遗传物质与来源于另一只雄性小鼠的精子一起注入新鲜的去核卵细胞中,最终获得只有两个“父亲”的孤雄小鼠。
研究团队共培育出12只孤雄小鼠,但是这些小鼠因为呼吸困难等问题仅存活了2天。

只有两个“父亲”的小鼠(图片来源:Leyun Wang)
意义与思考
这项研究展示了“在同性哺乳动物之间繁衍后代的一种全新而清晰的方式”,并指明突破同性生殖障碍需要经历3步:
1) 单倍体干细胞展现出类似原始生殖细胞的“无印记”模式;
2) 在单倍体干细胞中对特定印记区段进行修饰,建立新的印记模式;
3) 结合卵母细胞注射或四倍体囊胚补偿技术获得孤雌或孤雄动物。
虽然这项研究对理解基因组印记的进化、调控和功能具有重要意义,为开发新的动物生殖手段提供了线索,但是科学家们怀疑这项技术是否能够应用于人类。
Weizmann 科学研究所的分子遗传学家Jacob Hanna认为,这一研究中的大部分胚胎依然是异常的。孤雌胚胎的发育成功率为14%,而孤雄胚胎的成功率仅为2.5%。“这几乎不可能被允许应用于临床。” Jacob Hanna表示。
责编:悠然
参考资料:






