
图片来源:yahoo
帕金森病(Parkinson’s disease,PD)是一种常见的神经退行性疾病,其最主要的病理改变是黑质纹状体多巴胺(dopamine, DA)能神经元死亡, DA分泌显著减少进而导致患者运动能力损伤。目前的治疗方法只能改善疾病症状,无法消除病因。8月30日,日本科学家报告的一项疗法为患者带来了新希望。在这项发表于Nature期刊上的研究中,科学家将由人类诱导多能干细胞(iPS)制成的神经元移植到帕金森病猴子中,使它们在两年内症状得到显著改善,并且没有产生任何危险的副作用。日本京都大学的干细胞科学家Jun Takahashi领导了这项研究,他的团队计划在不久后开展临床实验。

多能干细胞具有分化出多种细胞组织的潜能。由于帕金森病患者多巴胺能神经元死亡,研究人员一直试图让多能干细胞补充缺失的多巴胺神经元,从而阻止甚至逆转疾病进展。此前的研究表明,人类胚胎干细胞具有这种功能,但是使用胎儿组织治疗存在伦理问题。而通过诱导多能干细胞(iPS),能够诱导成年细胞进入于胚胎样的状态,不仅具有相同的多能性,同时也避免了伦理问题。
人类iPS细胞成功减轻了帕金森猴的症状
在这项研究中,Takahashi的团队将健康人群和帕金森患者的iPS细胞转化为能产生多巴胺的神经元。然后将这些细胞移植到猕猴帕金森模型中。移植的脑细胞存活了至少两年,并与猴子的脑细胞形成了连接,被细胞治疗的猴子运动能力得到显著改善。
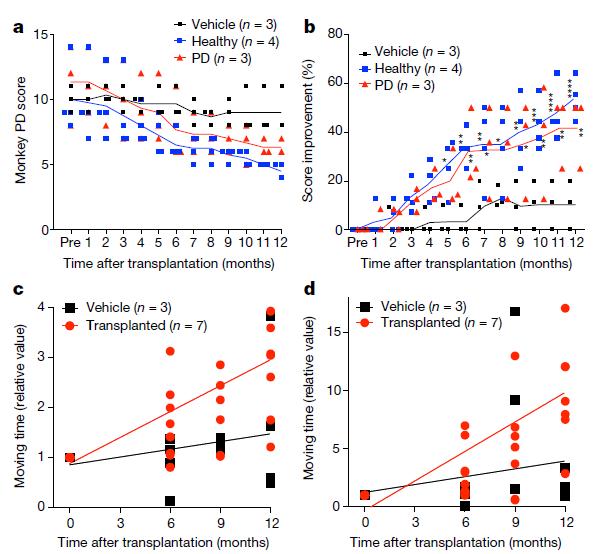
猴子的行为分析。图片来源:Nature
更令人惊喜的是,Takahashi的研究小组没有观察到移植细胞有发育成肿瘤的迹象——这是多能细胞治疗面临的一个最关键问题。并且,细胞移植也没有引发严重的免疫反应。
此外,研究人员还发现供体细胞的质量对DA神经元的存活有很大的影响。具体来说,他们找到11个可以标志细胞质量的基因。其中一个基因是Dlk1。研究人员表示,Dlk1是由胚胎干细胞制成的DA神经元移植到大鼠时细胞质量的预测标志之一。他们在移植到猴子的DA神经元中也发现了Dlk1。研究人员希望在未来的临床实验中Dlk1能用来评估细胞质量。
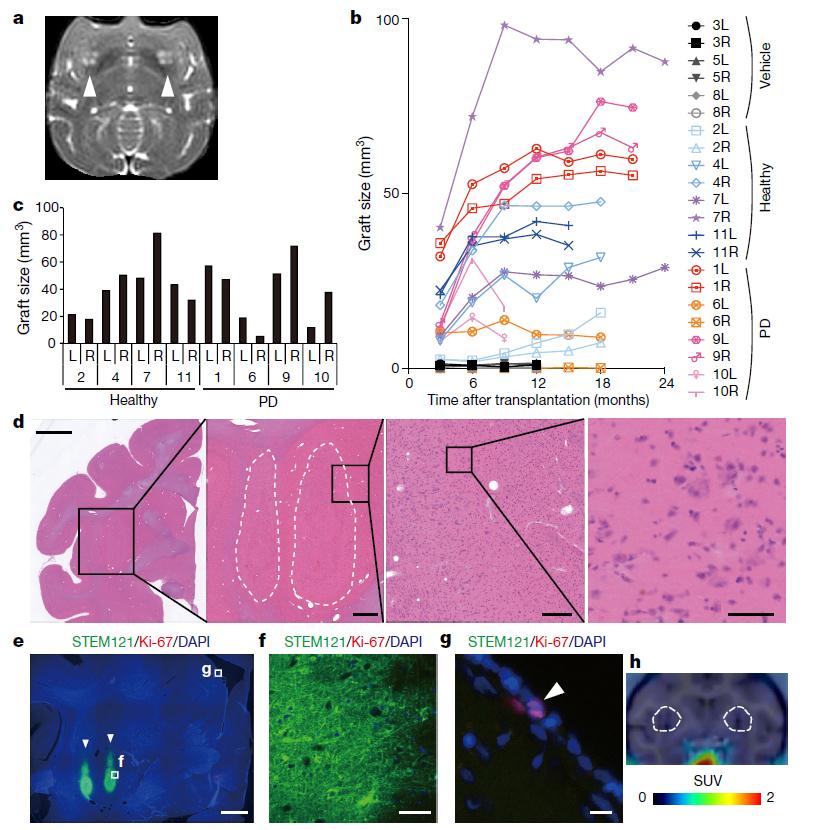
iPS来源的多巴胺神经元祖细胞在体内的生长和存活情况。图片来源:Nature
计划在明年年底前开启临床实验
Takahashi希望能在明年年底前开始临床试验。这是首个利用iPS细胞治疗帕金森病的临床实验。在2014年,一名70多岁的日本妇女曾首次利用iPS细胞治疗黄斑变性。
理论上,iPS细胞可以为个体患者量身定制,从而避免对外来组织可能出现的免疫反应。但Takahashi指出,定制iPS细胞的制作成本很高,而且需要花几个月的时间来获得和生长。因此,他的团队计划从健康人那里建立iPS细胞系,然后利用免疫细胞生物标志物与帕金森患者匹配,希望能尽量减轻免疫反应。
在Nature communications的一篇相关研究中,Takahashi的团队将来自不同猕猴的iPS细胞来源的神经元植入猴体中。他们发现,携带相似白细胞标志的猴子之间的移植触发的免疫反应更加温和。
参考资料:
Human iPS cell-derived dopaminergic neurons function in a primate Parkinson’s disease model






