Jennifer A. Doudna教授(图片来源:网络)
上周刚刚在《科学》子刊上发表了新成果的CRISPR先驱Jennifer A. Doudna教授本周又有1篇Science论文出炉。7月20日发表的这篇题为“Structures of the CRISPR genome integration complex”的研究揭秘了CRISPR蛋白是如何找到它们的目标的。
具体来说,加州大学伯克利分校的研究人员发现了Cas1-Cas2(与细菌中CRISPR免疫系统能力有关的蛋白质)是如何适应新的病毒感染,并鉴定出了它们在基因组中插入病毒DNA的位置。研究证实,Cas1-Cas2对插入位点的识别并不是依赖序列,而是依赖结构。
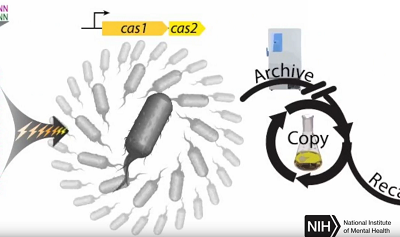
图片来源:NIH视频
值得一提的是,Cas1-Cas2最近刚被用于在细菌基因组的CRISPR区域编码了一部电影。相关成果于7月12日以“CRISPR–Cas encoding of a digital movie into the genomes of a population of living bacteria”为题发表在了Nature杂志上。哈佛大学遗传学大牛George M. Church是这一研究的通讯作者。(详细报道:Nature:首次!“小电影”被科学家刻进了活细菌的DNA)
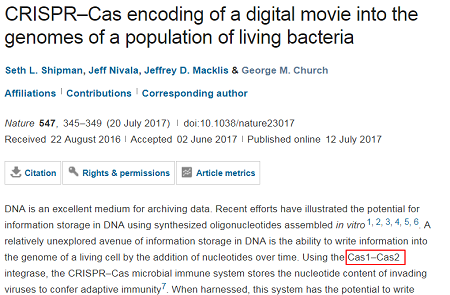
结构解析:第三蛋白让DNA弯曲成U型
在这项新研究中,科学家们发现,Cas1-Cas2依赖独特的CRISPR DNA灵活性来识别病毒DNA应该被插入的位点,从而确保先前病毒感染的“记忆”被正确存储。
借助电子显微镜和X射线晶体学,研究者们捕捉到了病毒DNA插入到CRISPR区域时Cas1-Cas2的结构。
这种结构揭示出,一种称为IHF的第三蛋白(third protein)结合在插入位点附近,将DNA弯曲成U型,从而使Cas1-Cas2可以同时绑定两个识别位点。研究发现,这种反应需要目标DNA弯曲并部分解开,并且这只会在正确的目标DNA上发生。
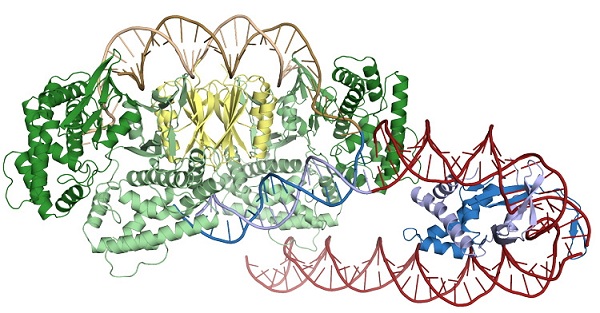
A protein called IHF (blue) creates a sharp turn in the DNA (red helix) upstream of the CRISPR repeat (brown helix), allowing Cas1-Cas2 (green and yellow) to recognize and bind the insertion site. (Addison Wright image)
(图片来源:加州大学伯克利分校)
CRISPR系统是细菌的免疫系统,可以让细菌适应并抵御病毒感染。CRISPR,即“成簇规律间隔的短回文重复”( Clustered Regularly Interspaced Short Palindromic Repeats),是DNA中的独特区域。病毒DNA片段被储存在这一区域,使得细菌细胞能够识别任何试图再度感染的病毒。病毒DNA与“短回文重复”交替出现。这可以作为一种识别信号,指引Cas1-Cas2添加新的病毒序列。
该研究的共同第一作者Addison V. Wright说:“Cas1-Cas2对这些重复(repeats)的特异性识别对将病毒DNA整合到CRISPR阵列中起到了限制作用。这将避免将病毒DNA插入错误的位置带来的潜在致命影响。”
特殊识别:不依赖序列,依赖结构
虽然很多DNA结合蛋白(DNA-binding protein)是直接“读取”它们识别序列的核苷酸,但Cas1-Cas2是通过更加间接的方式来识别CRISPR重复(CRISPR repeat):它的形状和灵活性。除了编码蛋白质外,一段DNA的核苷酸序列也决定了分子的物理性质,其中,一些序列表现为灵活的铰链,另一些则形成了刚性杆(rigid rods)。
CRISPR重复的序列使得它能够以恰好正确的方式弯曲,从而被Cas1-Cas2绑定。这种现象也使得Cas1-Cas2能够通过形状来识别它们的目标。
Wight在接受GEN采访时说:“Cas1-Cas2最明显的功能利用了它们的进化角色,即作为一种信息存储设备。正如George Church最近的成果所展示的那样(注:即本文第3段提到的那篇Nature)。在我们的研究中,我们发现Cas1-Cas2的识别更多的依赖于结构,而不是直接的序列识别。这对于改变Cas1-Cas2的用途具有相当重要的影响。”
相关推荐:新成果“剑指”脱靶效应
作为CRISPR技术的先驱,Jennifer A. Doudna教授每年都会发表大量的科研成果。除这篇Science外,本月12日,她带领的研究小组还在Science Advances杂志上发表了关于脱靶效应的最新成果(论文题目:Disabling Cas9 by an anti-CRISPR DNA mimic)。研究发现,CRISPR“关闭开关”AcrIIA4能够降低Cas9编辑人类细胞基因组的脱靶效应。
参考资料: