成年神经干细胞是否再生仍旧存在争议。尽管已经有很多的证据支持在海马齿状回、脑室下区、纹状体等区域存在神经再生,而且内源性的神经祖细胞在脑损伤时会迁移到损伤部位参与神经修复。神经祖细胞一直是研究热点,因为对于临床的诱惑太大,很多神经系统疾病都期待于神经干细胞的治疗,如脑损伤、脊髓损伤、神经变性病、脱髓鞘疾病等。
今天介绍的这项研究发现了在围生期大脑的脑膜上也存在神经祖细胞,而且这种神经祖细胞能够迁移到皮层形成成熟的功能性神经元。
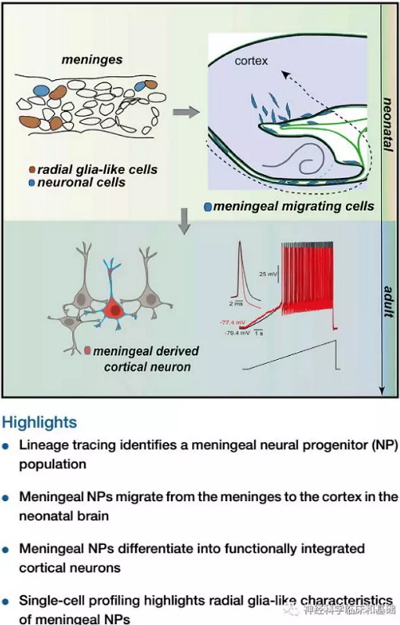
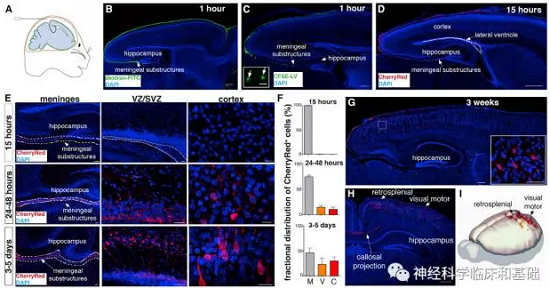
首先,研究人员采用慢病毒表达的CherryRed标记脑膜的干细胞,然后观测这些细胞在脑室下区、皮层的分布。他们发现随着时间的推移,脑膜上CherryRed标记的细胞会逐渐的出现在SVZ和皮层。需要注意的是CherryRed并不标记脑实质和室管膜细胞,这是研究的前提。
空间解剖学证据:接下来,研究人员研究了到底这些脑膜细胞是如何迁移到皮层的,他们发现了这些细胞经过侧脑室的脉络组织进行迁移。
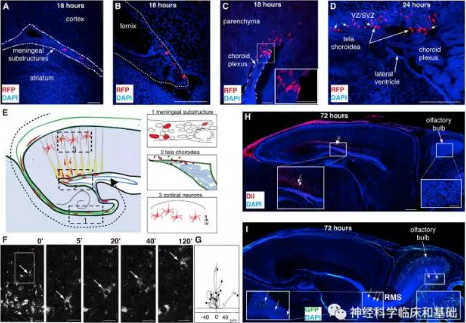
时间动态迁移证据:研究人员对这类脑膜细胞在何时迁移到皮层的问题进行了研究。发现了这类细胞在胚胎发生的14.5和16.5天产生,之后保持静息状态,而在出生后第1天逐渐迁移到皮层,而且以III、IV层为主。此外,这些脑膜中迁移来的细胞还表达DCX、NeuN和Satb2等神经元和神经祖细胞的标记物。
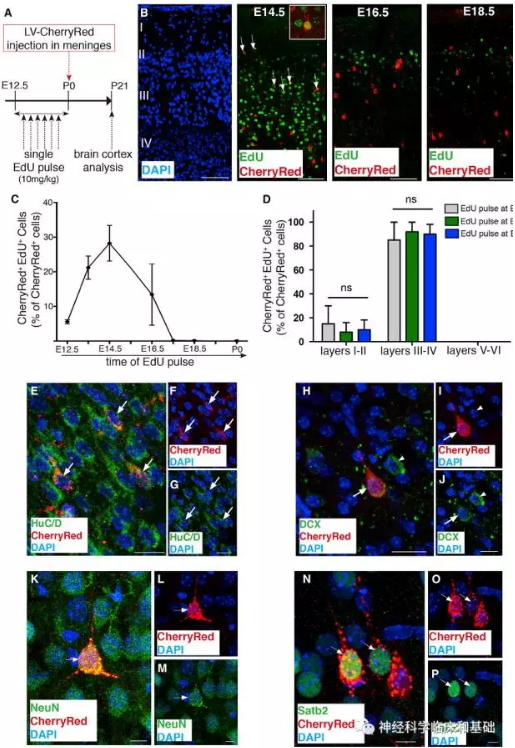
功能学证据:经电生理学研究,研究人员进一步发现这些脑膜细胞具有发放动作电位的特性,而且其动作电位的属性跟正常的皮层神经元还不一样。

起源探索1:那到底这些脑膜细胞是一类神经细胞呢?研究人员使用了GLAST-YFP、Nestin-YFP、PDGFRß-YFP三个转基因小鼠品系,证明在胚胎第13.5天时,16.5%的脑膜迁移来的神经元来自于脑膜上的Radial-Glia(GLAST+或Nestin+),而大部分来自于PDGFRß+系的祖细胞。
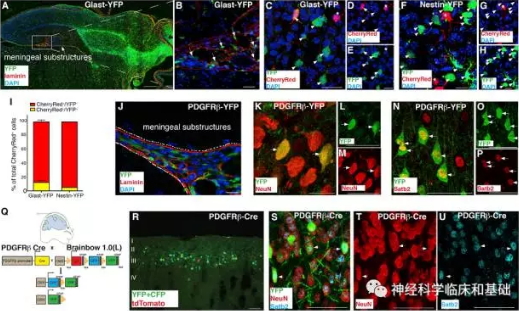
分子表达谱证据:研究人员接下来使用转录组学进一步研究了这些脑膜细胞来源的神经球所具有的转录产物,发现其主要与神经元来源的祖细胞相似。
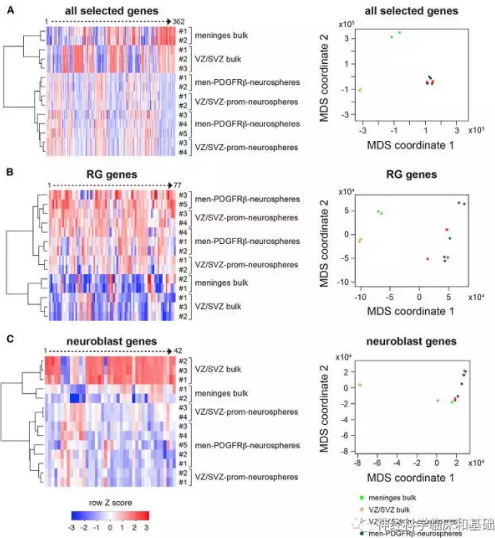
分子表达谱证据2:研究人员采用单细胞RNA-seq进一步证明,这些脑膜细胞具有Radial Glia样和神经元样的表达谱。
总结
这项研究表明,在胚胎发生过程中,脑膜中存在神经祖细胞,且这些祖细胞能够在出生后第一天能够逐渐迁移到皮层,参与皮层的神经发生。






