Josue和他的父母
11月28日,在马里兰大学医学中心的手术室中,一个仅仅4个月大的小男孩儿Josue,躺在手术台上,接受了他人生的第二次手术 。来自美国马里兰大学医学中心的Sunjay Kaushal博士和Si M. Pham医生给他的心脏中注射了干细胞[1],希望能帮助这个患有先天左心发育不良综合征(hypoplastic left heart syndrome,HLHS)的孩子更好地“活下去”。
HLHS在先天心血管畸形中占1.4%,死亡率非常高,患儿在出生之后如果不接受治疗的话,平均存活期只有4-5天,而多数48小时后,就会离开这个世界。但即使接受了手术治疗,他们的五年存活率平均也只有60%不到。
从八年前,Kaushal博士就开始探索用干细胞来医治HLHS的可能。而这次接受治疗的Josue是首次尝试用干细胞来修复婴儿心肌的临床实验中的一例。HLHS患儿的左心室很小,不能将富氧的血液输送到全身,因此患儿出生后就会出现进行性发绀、气促或呼吸困难和心力衰竭等表现。
目前最常用的治疗手段是通过三次阶段性手术对不同的动脉和静脉血管进行隔断和合并,让右心室来承担两个心室的“工作”。但即使手术成功,右心室“工作量”的增加会导致严重的“磨损”,最终的解决办法只能是“换心”。

Sunjay Kaushal博士
但是心脏源的稀少以及手术难度高、术后排异等问题都是不容忽视的,这对大多数患儿来说并不是一个简单的解决方法。因此,研究人员希望能在进行双向腔静脉-肺动脉吻合术(BDCPA,治疗先天心室发育不良的一种常用手术)时注射干细胞,利用干细胞的分化作用,增加心肌细胞,让右心“变强”,在不需换心手术的前提下,让患儿获得更高的生存率和生存年限。
马里兰大学的干细胞生物学与再生医学中心的主任Curt I. Civin表示,新生儿的心脏其实就是一个丰富的心脏干细胞源,但是HLHS患儿的干细胞不足,所以需要外来源的补充,来帮助他们“克服疾病”。研究人员选用的是异源间充质干细胞(MSC),MSC属于多能干细胞,在成人中,研究人员已经发现异源间充质干细胞可以修复心脏疤痕,减少炎症,促进细小血管、心脏干细胞和心肌细胞生长,进一步刺激心脏再生[2,3]。

Curt I. Civin主任
而在今年的早些时候,Kaushal博士和他的同事在美国生理学会下属的官方期刊《美国生理学杂志-心脏与循环生理学》(《American Journal of Physiology - Heart and Circulatory Physiology》)上发表研究[4],他们选择了心脏结构与人相似的小猪作为模型,模拟出了HLHS右心室超负荷的状态,分别给它们注射等量的干细胞和安慰剂进行治疗。4周后,实验结果显示,安慰剂组心肌细胞变大,心电图异常,右心室出现明显肥大,同时,基因检测发现,与肥大相关的基因表达量显著增加。
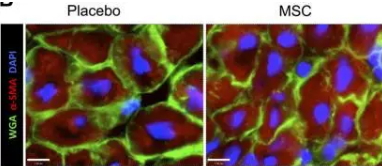
心肌细胞横截面对比(左为安慰剂组,右为MSC组),安慰剂组面积明显比MSC组大
而反观MSC治疗组,小猪的右心功能正常,抗肥大的生长分化因子15(GDF15)的表达量增加。MSC的残留量很少,心肌细胞和血管内皮细胞的增殖明显增加,有新的血管形成。同时内源性c-kit +心脏干细胞在右心室中广泛存在,c-kit +心脏干细胞是成体心肌组织中含量最多、增殖能力最强的干细胞类型,被认为是目前最有希望实现完全心肌再生的干细胞类型。
这些关键的结果表明,MSC治疗对于HLHS患者来说可能是一个潜在的有效疗法,基于这个研究,Kaushal博士也申请到了规模为30人的1期临床试验(NCT02398604)[5],而包括Josue在内的已经接受了MSC注射的两个案例,目前的表现都很好,这也给了Kaushal博士很大的信心。Josue的父母虽然知道这个疗法并不能保证一定会有一个完美的结果,但是看到目前稳定的状况,他们还是非常地开心,Josue的父亲一直向医生们表示,“上帝和我们在一起,我们都在努力”。
目前,Kaushal博士的临床试验还在招募志愿者,这项研究会一直持续到2020年,到那个时候我们才会真的知道,MSC疗法究竟效果如何。在Josue接受手术前,Kaushal博士对Josue的父亲说,“我知道这太让人紧张了,但是,一切都会好起来的。”我想,这句话可能也是Kaushal博士想对自己说的吧,我们也希望这个未完待续的故事能早日迎来一个好的结局。
参考文献:
[1] https://www.statnews.com/2016/12/20/stem-cell-heart-infant/
[2] Hare JM, Fishman JE, Gerstenblith G, DiFede Velazquez DL, Zambrano JP, et al. Comparison of allogeneic vs autologous bone marrow-derived mesenchymal stem cells delivered by transendocardial injection in patients with ischemic cardiomyopathy: the POSEIDON randomized trial. JAMA 308: 2369 –2379, 2012.
[3] Hare JM, Traverse JH, Henry TD, Dib N, Strumpf RK, Schulman SP, et al. A randomized, doubleblind, placebo-controlled, dose-escalation study of intravenous adult human mesenchymal stem cells (prochymal) after acute myocardial infarction. J Am Coll Cardiol 54: 2277–2286, 2009.
[4] Wehman B, Sharma S, Pietris N, et al. Mesenchymal stem cells preserve neonatal right ventricular function in a porcine model of pressure overload[J]. American Journal of Physiology-Heart and Circulatory Physiology, 2016, 310(11): H1816-H1826.
[5] https://clinicaltrials.gov/ct2/show/NCT02398604?term=NCT02398604&rank=1






