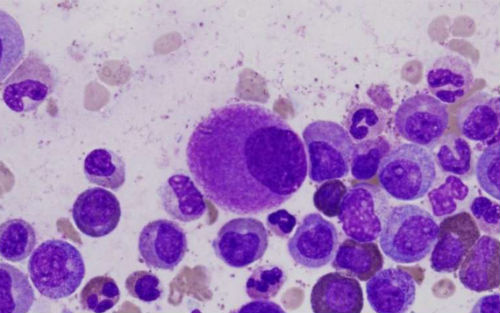
麻省总医院MGH、Broad研究所的研究人员在单细胞水平上对脑瘤进行基因组分析,首次在人类脑瘤样本中鉴定到了癌症干细胞及其分化后代。这项重要的研究成果十一月二日发表在Nature杂志上。
少突胶质细胞瘤是一种生长缓慢但无法治愈的脑瘤。“我们提出了强有力的证据,证明癌症干细胞是少突胶质细胞瘤的主要生长源,这些细胞将成为很有前景的治疗靶标,”文章资深作者Mario Suvà博士说。
近年来人们逐渐意识到,一些肿瘤的发展和耐药性与癌症干细胞有关,特别是白血病等血液系统肿瘤。此前也有研究发现,癌症干细胞在胶质母细胞瘤中起作用。不过这些研究主要针对移植了人类肿瘤的小鼠。为了准确分析少突胶质细胞瘤,研究人员在单细胞水平上进行了RNA测序研究。
他们分析了六个早期肿瘤样本的四千多个肿瘤细胞,发现肿瘤细胞在发育上可以分为三类。其中一类比较像神经干细胞,另外两类具有一定的分化特征。研究显示,只有癌症干细胞表现出增殖迹象,其他任何癌细胞都没有这种表现。研究人员指出,靶标癌症干细胞(比如用免疫疗法)有望为少突胶质细胞瘤患者带来帮助。
著名癌症生物学家Robert A.Weinberg相信肿瘤之中存在着癌症干细胞。这些细胞能够通过自我更新和分化,启动并维持癌症的形成和发展。它们相当于癌症的种子,能抵抗化疗并在多年后导致癌症复发。理论上,特异性靶标这些细胞,就可以控制住癌症。Weinberg的公司Verastem Inc.启动了新一轮的临床试验,希望用事实证明上述理论。
癌症干细胞就像杀不死的僵尸,它们拥有恐怖的再生能力,不断生成新的癌症干细胞和肿瘤。加州大学的研究人员在Cell Stem Cell杂志上发表文章指出,癌症干细胞利用基因编辑系统来克隆自己。这一机制使白血病前期的白细胞前体变成了白血病干细胞。
中科院生物物理所的科学家们通过深入研究,鉴定了一种支持肝癌干细胞自我更新的lncRNA(lnc-β-Catm)。这项重要研究成果于五月三十日发表在Nature Structural & Molecular Biology杂志上,文章通讯作者是中科院生物物理所的范祖森(Zusen Fan)研究员。






