导读:4个碱基三三组合可行形成64个密码子,而生命所需氨基酸只要20种,密码子的富余不可避免地出现。不过既然同一种氨基酸对应数个密码子,为什么在进化中会出现密码子偏好呢?加州大学的最新研究回答了这个问题。
加州大学的研究人员发现了隐藏在遗传密码中以前从未被认识到的信息。他们的这一发现得归功于加州大学开发的一种叫做核糖体作图(ribosome profiling)的技术,该技术可对活细胞内的基因活性进行测定—包括基因所编码的蛋白质翻译的速度。
通过对细菌中蛋白石产生的速度进行测定,该研究团队发现,细微的遗传变化都会带来强烈的影响,即便是看起来并不怎么重要的、被称为“无表型突变”—即对基因中的某个碱基进行替换而不改变最终的基因产物—的遗传改变也是如此。令人惊讶的是,科学家们发现这些改变可导致蛋白质生产速率降低到正常速度的十分之甚至更低。
发表在Nature上的 研究论文称,这种速率的变化是由冗余密码子—组成遗传密码一部分的小段DNA—中所包含的信息引起的。它们被认为是“冗余的”是因为它们此前被认为其含有的信息只是简单重复,而非唯一的结构。
该新发现挑战了生物学中盛行了半个世纪的基本假说。这还可能帮助加速蛋白质的工业生产,这对于生物燃料生产以及用于治疗许多常见疾病(从糖尿病到癌症)的生物药的生产来说影响深远。
“遗传密码一直被认为存在富余现象,但冗余密码子显然并非完全一样,”加州大学霍华德•休斯医学研究所的Jonathan Weissman博士说。他说道:“我们以前对该规则了解不多。”
不过现在新的研究表明,自然选择也在冗余密码子中基于遗传速度及遗传意义而发生着。
举个相似的例子,一个人在向朋友发短信时可能选择用“NP”带代替“No problem”。这两者所代表的意思是一样的,但是打NP明显要比打No problem快的多。
关于DNA密码子
地球上的所有生命都将遗传信息储存在DNA中(某些病毒将遗传信息存在RNA中)并将DNA所携带的信息表达为蛋白质,以此而构建细胞组分、执行生命的遗传指令。
地球上所有器官中的所有组织中的每一个活细胞都在持续地进行基因表达并翻译为蛋白质,贯穿着每个生命的整个生命周期。我们所消耗的大量能量无非就是这些基本过程所提供的。
遗传信息是一套基本的指导DNA翻译为蛋白质的通用指令信息。DNA基因由四种被称为碱基或核苷酸(通常由A、G、C、T四个字母表示)组成。但是蛋白质是由20种不同的氨基酸组成的。
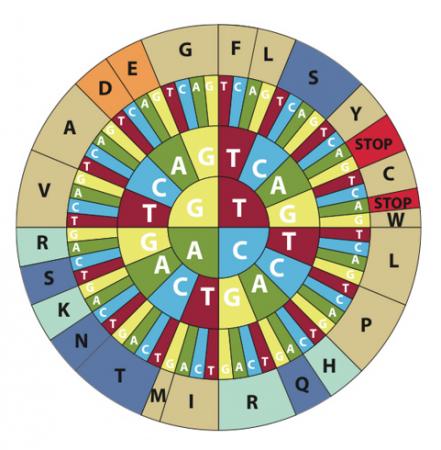
要编码所有20种氨基酸,遗传密码需要每次读取基因上3个碱基来对应蛋白质中的一个氨基酸。这种三联的DNA碱基就被称为密码子。不过由于四种碱基进行三三组合可形成64种可能的组合,而生命所需的氨基酸仅20种,密码子的数量超过了需求量。故同一种氨基酸会对应着这64个密码子中的数个密码子。
科学家们50年前就知道了这种密码子的富余现象,但是直到最近几年,越来越多生物(从家养的犬类到野生的老鼠)的基因组被解码,科学家们已经意识到,并非所有富余的密码子都发挥等同的作用。
许多的生物会明显偏好编码同一个氨基酸的数个密码子中的其中一个,即便是在不管选用哪个密码子其结构都相同的情况下。这就出现一个无法回避的问题:既然富余的密码子作用都是一样的,为什么自然选择会对其中一个有偏好。新的研究完美地回答了这个问题。

 The anti-Shine–Dalgarno sequence drives translational pausing and codon choice in bacteria
The anti-Shine–Dalgarno sequence drives translational pausing and codon choice in bacteria
Gene-Wei Li, Eugene Oh & Jonathan S. Weissman
Protein synthesis by ribosomes takes place on a linear substrate but at non-uniform speeds. Transient pausing of ribosomes can affect a variety of co-translational processes, including protein targeting and folding. These pauses are influenced by the sequence of the messenger RNA. Thus, redundancy in the genetic code allows the same protein to be translated at different rates. However, our knowledge of both the position and the mechanism of translational pausing in vivo is highly limited. Here we present a genome-wide analysis of translational pausing in bacteria by ribosome profiling—deep sequencing of ribosome-protected mRNA fragments. This approach enables the high-resolution measurement of ribosome density profiles along most transcripts at unperturbed, endogenous expression levels. Unexpectedly, we found that codons decoded by rare transfer RNAs do not lead to slow translation under nutrient-rich conditions. Instead, Shine–Dalgarno-(SD)6-like features within coding sequences cause pervasive translational pausing. Using an orthogonal ribosome possessing an altered anti-SD sequence, we show that pausing is due to hybridization between the mRNA and 16S ribosomal RNA of the translating ribosome. In protein-coding sequences, internal SD sequences are disfavoured, which leads to biased usage, avoiding codons and codon pairs that resemble canonical SD sites. Our results indicate that internal SD-like sequences are a major determinant of translation rates and a global driving force for the coding of bacterial genomes.
文献链接:https://www.nature.com/nature/journal/vaop/ncurrent/full/nature10965.html







