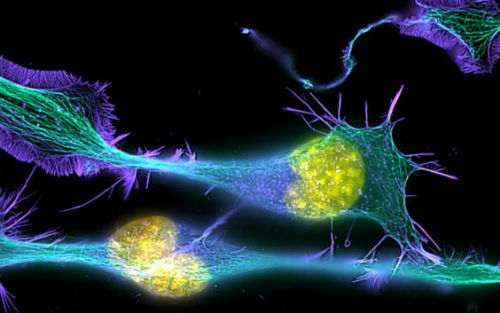
5月底,GEN网站发表一篇论述干细胞市场格局的文章。作者指出,从2012年至2016年PubMed文献库共录入125,692篇学术文章,干细胞学术研究投入正以超5%的总体增长率上升。从上游的干细胞存储、中游的干细胞药物开发到下游的干细胞治疗,围绕干细胞的产业链体系已经趋向完整。
干细胞因其能够自我更新复制、具有多向分化的独特功能而备受科学家青睐,它是转化医学、再生医学、精准医学的重要基础和实现手段。ViaCyte公司首席科学官Kevin D’Amour表示,这种快速发展得益于大量的基础研究工作。ViaCyte研究团队数十年来一直致力于分离、培养、纯化胚胎干细胞。现在,这项技术开始运用于临床研究,使其真正实现价值。
每个人都可以预见干细胞治疗的巨大潜力,但是瓶颈在于跨越细胞本身与实现治疗的鸿沟。这也是很多研究团队、医药企业正在努力和创新的方向。
神经干细胞库
神经干细胞治疗中枢神经系统疾病是一个前沿领域。目前,StemCells公司已经在临床前、临床试验中取得了积极的结果。该公司掌握了一套从胎儿脑组织中分离、纯化、放大并低温保存神经干细胞的技术,并以此构建了一个人类神经干细胞库(HuCNS-SC®)。保存的神经干细胞可以直接用于移植。
该项目起始于1999年,并于2009年完成首例临床试验。最初因为政策、安全性问题进展缓慢。公司总裁兼首席执行官Ian Massey博士表示,考虑到一旦移植进入人体就没有办法删除干细胞,研究团队一直严谨操作。
现在,得益于研究的谨慎、坚持,StemCells已经掌握安全可靠的大规模数据,能够很好的支撑该技术实现转化。鉴于多年临床前、临床早期试验,HuCNS-SC治疗体系已经建立。现在,研究团队开始寻找支持干细胞治疗疾病更多的证据,特别是移植后神经干细胞的自我更新、迁移、分化过程。
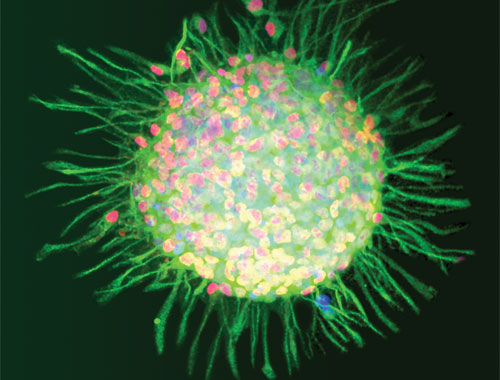
HuCNS-SC是纯化的神经干细胞库。图中所示细胞群是在Leica SP2共焦显微镜下观察的图像。这些神经干细胞保持有自我更新、多项分化的能力。
Massey博士表示,这项技术的潜在能力在于通过内源性补给神经营养因子治疗中枢神经系统疾病,因为这类干细胞能够生成新的神经元、少突胶质细胞和星形胶质细胞。此外,借助基因编辑,这些神经干细胞还有望被修改为蛋白质工厂。当下,我们正处于一个良好的时机,去验证它们是否能够实现医学突破。神经干细胞很有可能能够应对目前没有有效治疗方案的疾病。
封装干细胞
干细胞治疗1型糖尿病的优势在于它可以成为补充胰岛素细胞的资源,还能作为免疫调节剂减轻自身免疫反应。但是这一疗法首要面临着“低值入率”的问题。科学家提出一种“细胞封装”(encapsulation)技术,能够突破免疫限制实现干细胞的植入。
ViaCyte公司研发的VC-01™胰岛素替代疗法就是运用了该封装技术,它由两部分组成:在体外从多能干细胞诱导获得的胰腺前体细胞群,以及一种巨囊化装运设备。这一特殊设备被称为 Encaptra®,负责装载、运输治疗细胞。它可以植入皮下组织,并将前体细胞运输至需要分化出胰岛细胞的部位。

图中所示的是ViaCyte的PEC-01 胰腺祖细胞被封装在Encaptra运输系统中。一旦植入人体,胰腺祖细胞能够分化成分泌各类激素的胰腺细胞,包括胰岛素、胰高血糖素和生长抑素。
D’Amour博士强调,这一替代疗法的临床目标是“治愈”1型糖尿病。这里之所以加引号,是因为它并不会更改自身免疫致病机理,而是通过取消患者需要不断检测血糖、注射胰岛素的繁琐过程,帮助患者对抗疾病。
目前,VC-01™胰岛素替代疗法正处于临床Ⅰ/Ⅱ期试验阶段。数据显示,植入12周后,前体细胞开始促进细胞生成并血管化,最后分化成β细胞。
对于糖尿病而言,VC-01™胰岛素替代疗法有望成为首个将多能干细胞应用于治疗的成功案例之一。作为一个概念性验证,它将对再生医学领域产生巨大影响。此外,细胞封装技术有望用于多种细胞治疗中,旨在取代分泌激素细胞。
干细胞构建器官芯片
采集干细胞并培养在芯片上,以模拟和构建人体器官的技术被称为“微型器官”,是干细胞应用领域又一个新奇技术。这种微型装置可以实现非侵入性监测,相比于传统设备更有利于数据的读取。
中佛罗里达大学纳米科技中心教授、Hesperos公司首席科学家James Hickman 博士是该领域的专家。Hickman博士表示,微型器官并不是通过检测20种生物标记物简单确定肌肉是否收缩,而是直接能够测量肌肉的收缩力。它是一个真正的表型系统,其优势在于能够直接读取数据。
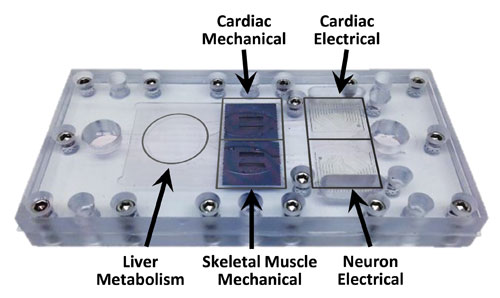
图示即Hesperos公司的微型器官系统,可以模拟肝脏、心脏、骨骼肌和神经功能。芯片系统可以通过生化检测、微电极阵列评估细胞功能和活性。
值得注意的是,这种技术可以用于评估不同器官模型之间的互作情况。例如,一种治疗心脏病的药物经过肝脏降解后会产生毒素,所以提前评估药物在多种器官的互作情况很重要。研究人员通过这种芯片能够实现演示。
Hickman 博士解释:“当我们将肝脏剔除系统,结果发现心肌细胞不受毒素影响。但是将肝脏加入系统,我们发现了损伤心脏的毒素。”所以,微型器官系统有利于推动个性化医疗。Hickman博士强调,你可以从多种患病组织中采集成体干细胞,在实验室芯片培养,以此验证不同种治疗药物的效果,实现个性化医疗。
此外,该技术有望应用于快速、低成本地构建疾病模型,从而取代动物模型。这有利于减少动物甚至人类临床试验风险。借助芯片构建多种疾病模型,包括癌症、糖尿病、遗传学疾病,将有利于我们跨越伦理限制、更快速的投入疾病研究中。
基因编辑干细胞
随着基因编辑技术的发展,干细胞基因组编辑也成为该领域一个关注热点。例如Sangamo Biosciences公司的 Edward Lanphier正带领团队专注于这一研究,通过锌指核酸酶(ZFNs)修改干细胞中与临床相关的特定序列,再将修饰后的细胞移植入人体实现疾病治疗。ZFNs是Sangamo Biosciences公司的核心技术,而其他包括 CRISPR/Cas9 或者 TALEN 编辑技术也可以实现这一目标。
Lanphier团队借助ZFNs扰乱艾滋病患者造血祖细胞的CCR5基因,旨在实现免疫系统免受病毒感染并增强抗病毒的能力。借助干细胞治疗,不再需要抗逆转录病毒慢性治疗,从某种意义上而言这实现了治愈艾滋病的目的。
备注:文章编译、整理自GEN网站,原文链接“Reaping What Stem Cell Technology Sows”。






