来自美国印第安纳大学医学院的研究人员报告称,他们发现了一种提高造血干细胞移植效率的新方法。这项重要的研究在线发表在6月11日的《细胞》(Cell)杂志上。
领导这一研究的是印第安纳大学医学院的杰出教授、美国血液学会前主席Hal E. Broxmeyer博士。Broxmeyer博士的研究领域是调节造血细胞和胚胎干细胞的自我更新、增殖、存活、分化和迁移,以及造血功能和免疫细胞的活性,为造血干细胞领域和脐带血干细胞领域做出了重大的贡献。
Broxmeyer是第一位提出脐带血干细胞移植治疗恶性白血病的专家,同时也是第一位开展脐带血干细胞移植的专家,是脐带血干细胞研究和应用的领军人物。作为国际公认的脐带血移植领域的奠基人。Broxmeyer博士曾获得诸多奖项,担任过十多个组织的主席,他目前担任11个科学杂志的编委,已发表700多篇论文,并撰写了15项专利。
造血干细胞(Hematopoietic Stem Cells,HSCs)是指存在于骨髓、外周血、脐带血、肌肉以及其他有造血组织的器官中的一类稀有多能细胞,其具有自我更新能力并能分化为各种血细胞前体细胞,最终生成各种血细胞成分,包括红细胞、白细胞、血小板和淋巴细胞等,可以说它是一切血细胞的原始细胞。
近30年里,造血干细胞被广泛地应用于血液病治疗的临床实践,已成为治疗和治愈恶性血液病、重型再生障碍性贫血(SAA)、某些实体瘤、某些异常免疫病、某些遗传病、代谢病和极重度骨髓型放射病的最有效方法,已成为现代医学异军突起的重要方向。但由于获得的造血干细胞数量有限,输注后产生的成熟细胞的生物动力欠佳等不足,目前临床上造血干细胞移植还受到极大的限制。
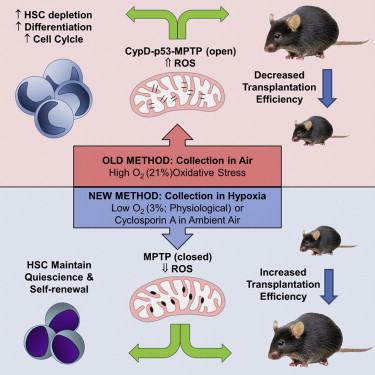
在这篇文章中作者们指出,生理状况下的造血干细胞是定位在人体内平均氧浓度为3%的低氧环境中,而现在的造血干细胞采集及处理程序则是在比人体内氧浓度高得多的(21%)的环境下完成。
研究人员发现即便是短暂地暴露于这样的高氧环境下,也会给造血干细胞带来负面的影响,造成造血干细胞数量减少、功能下降最终导致移植后的疗效下降。他们将这种效应称作为超出生理范围的氧冲击/压力(extraphysiologic oxygen shock/stress,EPHOSS)。因此,平常骨髓和脐带血中造血干细胞的真实数量有可能被低估了。
通过进一步的机制研究,研究人员将由活性氧(ROS)介导的这种造血干细胞数量减少,与CypD-p53-MPTP(线粒体通透性转换孔)信号轴、miR210和hif-1α关联起来。他们进而证实在空气中收集小鼠骨髓和人类脐带血HSCs时,添加MPTP抑制剂环孢菌素A(cyclosporin A)可以保护这些细胞免受EPHOSS的损害。
研究人员指出,在细胞收集和处理过程中采用药物来减轻EPHOSS,有可能是一种帮助改善临床造血干细胞移植的有效方法。






