被困网中
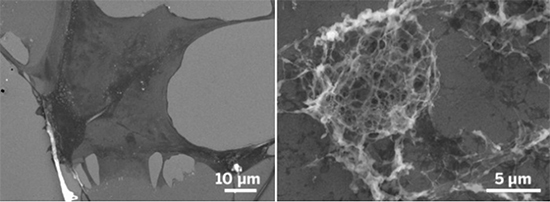
图为扫描电子显微镜下的骨癌细胞在存在(右)和
缺乏(左)碳水化合物型分子的环境里培育七个小时后的情形。
在癌细胞周围,散布着分子自组装成的纳米纤维网状结构。
纽约城市大学亨特学院(City University of New York’s Hunter College)的Rein V. Ulijn表示,用分子牢笼困住细胞的灵感来源于自然界。很多体细胞都处在细胞外基质中。细胞外基质是生物分子构成的复杂网络,可为组织提供结构,促进细胞间的信息传递,收集营养物质。科学家正开发可自发组装为简单外基质的分子,以提供细胞的生长介质,尤其是在生物组织工程中提供营养。
该领域的研究主要集中在自组装肽。在最近的研究中,布兰代斯大学(Brandeis Unuiversity)的徐冰(音)及其同事设计出一种非培育肽,该肽发生团聚并在移除磷酸基团之后,吞没癌细胞。无磷肽有亲水端和疏水端,这使它们能以类似细胞膜上脂质的方式组装。磷酸基团上的负电荷产生了分子间的静电斥力,阻止了自组装的过程。因为一些种类的癌细胞对碱性磷酸酶(一种用于切割磷酸基团的酶)过表达,磷酸基团的存在与否对定位癌细胞十分有利。
Uljin和他的同事,包括葡萄牙米尼奥大学(University of Minho)的Iva Pashkuleva,认为他们能使碳水化合物型分子表现出同样的行为。Uljin表示,与肽相比,碳水化合物可以生成更丰富的结构,开拓新的应用前景。为了合成织网型分子,研究者先在一种亲水的碳水化合物氨基葡萄糖上添加了疏水的芳香族基团,以合成可以自组装的分子,然后再在这种糖上添加了一个磷酸基团。
研究者将分子添加至癌细胞及正常软骨细胞培养基中以测试合成分子的抗癌能力。较之癌细胞,在正常细胞组中只观察到其约5%的碱性磷酸酶活性。七小时后,约有95%的骨癌细胞死亡,而软骨细胞死亡率为15%。
根据扫描电子显微镜下细胞的成像,骨癌细胞表面了形成了牢笼状的水凝胶。虽然引起细胞死亡的机制尚未清楚,但Uljin怀疑是由于纳米纤维牢笼窒息细胞所致:既不允许营养物质进入,也不允许细胞废物流出。
徐冰认为,这项研究显示高酶活动性可以成为定位癌细胞的一种方法。徐还认为团队需要使用比常规药物浓度更高的分子进行测试。对患者而言,高浓度往往对应较大的剂量,也就意味着可能有更高的副作用风险。Uljin同时认为其团队需要针对自组装碳水化合物型分子可能的副作用开展一些研究。
推荐阅读:Self-Assembling Carbohydrates Trap Cancer Cells In A Cage







