绝大多数癌细胞的某些染色体拷贝太少或太多,这种状态称之为非整倍体(aneuploidy),但几十年来,科学家们一直在讨论是否非整倍体会促进癌症的生长,或者其只是癌细胞快速生长的副作用,DNA的这种大规模改变一直以来都难以研究。
近日,一篇发表在国际杂志Nature上题为“Cancer aneuploidies are shaped primarily by effects on tumour fitness”的研究报告中,来自MIT等机构的科学家们通过利用所开发的计算工具进行研究后发现,非整倍体会驱动癌症的进展;利用这种方法,研究人员比价了1万多名癌症患者机体肿瘤细胞的大型染色体改变,并识别出了关键的染色体区域,当这些区域被复制或剔除时就会对肿瘤细胞产生有害或有益的影响,本文研究还揭示了名为WRN的已知癌症基因所扮演的关键角色,研究人员揭示了这种类型的分析是如何能揭示出对癌症生物学的新的认识的。
相关研究结果或有望帮助开发指导癌症治疗或开发新型靶向性疗法的新方法;研究者Rameen Beroukhim说道,本文研究通过直接利用来自患者机体的肿瘤样本提供了一种计算答案来回答一个古老的问题,即是否这些大规模的事件真的能够驱动癌症的发生或者只是顺便而已。研究者发现,这些非整倍体正在被直接选择或反对,而这取决于其对癌细胞所产生的影响。大多数的人类细胞都包含有23对染色体,但在19世纪末期,科学家们注意到,肿瘤往往会携带含有异常数量染色体的细胞,直到最近有研究表明,非整倍体(包括染色体整臂的重复或剔除)或许存在于几乎90%的人类癌症中,而且常常会在癌症早期被发现,且与患者较差的临床治疗结局相关。
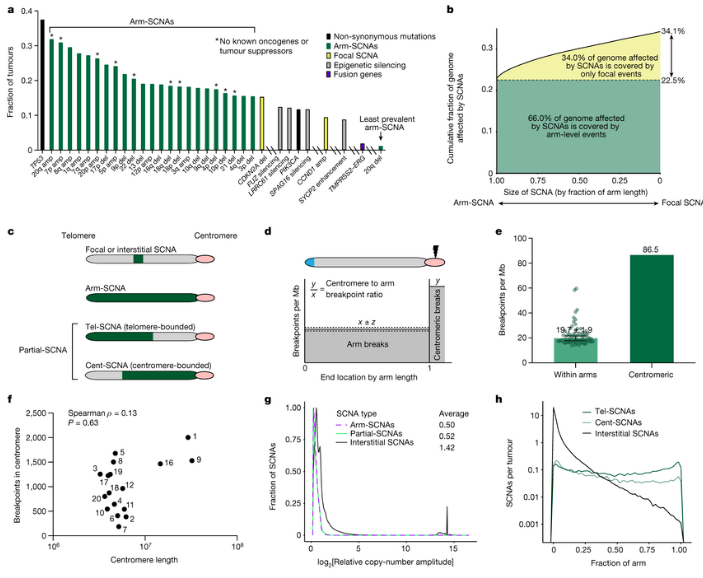
对1万多份人类癌症样本分析揭示了染色体失衡驱动癌症发生背后的分子机制。(图源:Nature)
一些研究人员怀疑,非整倍体的出现是因为癌细胞的严重失调,这对于癌症并没有任何实际的影响,由于参与非整倍体形成的DNA区域的剔除或复制常常包括数百或数千个基因,因此,阐明非整倍体对肿瘤生长的分子机制非常困难。研究者Alison Taylor说道,一个多世纪以来我们一直知道,这些非整倍体在癌症基因组中非常突出,但我们并没有很好的方法对其进行相关研究。为了对癌症中的非整倍体进行研究,研究人员就想知道是否其能利用癌细胞中其它更短类型的染色体改变,来找出到底是染色体的哪些部分在肿瘤生长和生存过程中扮演着关键角色。
研究者表示,有一些大规模的变化并不太符合非整倍体的典型定义,但其任然会影响染色体臂的很大一部分。如今研究人员开始思考,这些较短的事件能够给予癌细胞是否会选择某些染色体变化的特殊信号。文章中,研究人员开发了一种名为BISCUT(重要癌症未发现靶点的断点识别技术,Breakpoint Identification of Significant Cancer Undiscovered Targets)的方法来分析每条染色体中大的变化最优可能会在哪里开始或哪里结束;如果开始和结束点处于完全随机的位置,这或许就表明,这种非整倍体对于癌细胞的生存并没有直接的影响,然而,如果一个特定的区域通常包括在大规模的染色体改变之中,这或许就能暗示,这一区域的非整倍体或能帮助癌细胞生存,相反,如果这一区域经常被排除在外的话,这就表明,这种包含这一区域的非整倍体能杀死癌细胞并阻碍其生长。
随后研究者利用BISCUT对来自癌症基因组图谱(TCGA)中的33种癌症类型的10872份肿瘤样本进行分析,分析结果表明,非整倍体内部或附近的193个区域似乎能被癌细胞进行选择或“反对”,而不到一半的区域包括已知的癌症基因。此外,研究人员还发现,不同染色体上的非整倍体的频率或与非整倍体区域中预测的选择性压力相关。研究者Beroukhim指出,这或许是一种非常明确的方法,其揭示了,选择似乎是非整倍体模式的主要驱动因素,因此,非整倍体或许会对癌细胞的生存产生一定的影响。
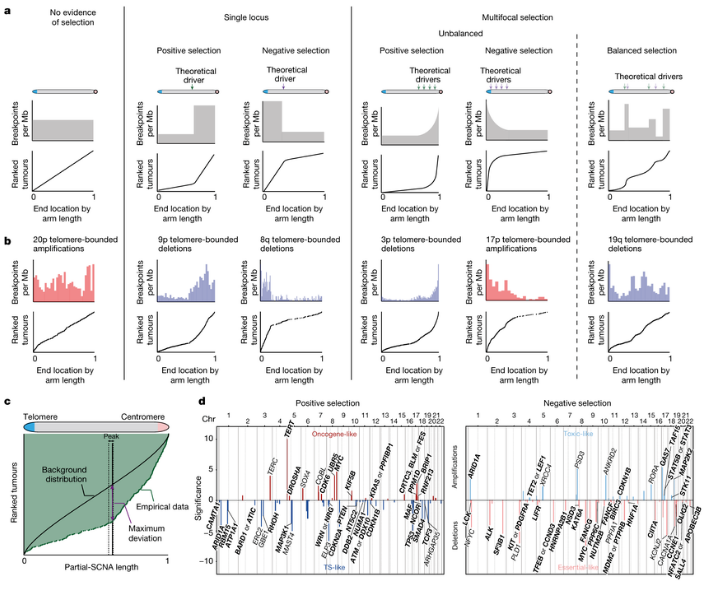
对1万多份人类癌症样本分析揭示了染色体失衡驱动癌症发生背后的分子机制。(图源:Nature )
在TCGA的所有癌症类型中,近乎有三分之一的癌症缺少8号染色体的一个臂,但研究人员一直不确定为何这种非整倍体如此普遍;本文研究结果表明,相比DNA的其它区域而言,8号染色体的剔除更有可能会包含癌症基因WRN,这就表明其或许真的会产生特别大的影响。众所周知,某些癌症类型已知会依赖WRN,而且研究人员目前正在开发阻断该基因功能的药物;本文研究揭示了,在高达三分之一的癌症中,基因的部分缺失似乎能帮助癌细胞存活;这一观察性结果或许有望帮助开发新型疗法来选择性杀灭携带WRN缺失的癌细胞,同时还能帮助识别出更有可能从这些类型疗法中获益的癌症患者。
这项研究发现是研究者Beroukhim等人认为其数据集最终会导致的数十种见解中的一个案例,独立的研究能深入研究BISCUT所识别出的每个染色体区域背后的机制,研究人员推测,许多区域或许能指向新的药物靶点或筛选癌症患者从而获得最有效疗法的方法。研究者Beroukhim表示,我们解决一个世纪之久的问题的能力就是一个很好的案例,这或许就能表明,癌症研究如何帮助实现更大的飞跃,即使是一些看似并没有研究希望的区域。综上,本文研究结果有望帮助科学家们更深入地理解非整倍体发生背后的驱动因素以及其对肿瘤发生的“贡献”。
文章来源“生物谷”