在一项新的研究中,来自美国斯坦福大学的研究人员发现了一种诱导癌细胞死亡的方法,这种方法对大约50%的癌症有效。他们描述了一类名为转录/表观遗传邻近化学诱导剂(transcriptional/epigenetic CIP, TCIP)的新分子,这类分子可以借助癌细胞内癌症生长基因的表达激活细胞凋亡。相关研究结果于2023年7月26日在线发表在Nature期刊上,论文标题为“Rewiring cancer drivers to activate apoptosis”。

这些作者设计了能将特定转录抑制剂(transcriptional suppressor)与转录激活剂(transcription activator)结合在一起的小分子。他们构建的最有效的分子是TCIP1,它通过将结合BCL6的小分子与结合转录激活剂BRD4的小分子连接起来而发挥作用。
癌细胞之所以会癌变,其中一个原因是它们无视周围健康组织发出的停止生长、启动细胞凋亡的信号。这种细胞凋亡途径仍然存在,但在某些类型的癌症中被主动阻断:转录因子BCL6与凋亡基因的启动子结合,并通过表观遗传机制抑制它们的表达。
这些作者将结合 BCL6 的小分子与结合转录激活剂 BRD4 的分子连接起来,开发出了 TCIP。转录激活剂(如 BRD4)在癌细胞中的正常活性是促进癌细胞的快速生长和增殖。当与 BCL6 连接在一起时,BRD4 将激活 BCL6 所结合的任何东西,激活癌细胞试图用 BCL6 抑制的任何基因表达,包括凋亡基因。
TCIP1 成功杀死了大 B 细胞淋巴瘤细胞系,包括化疗耐药的 TP53 突变系,并表现出细胞特异性和组织特异性效应。细胞凋亡的激活到细胞死亡只需 72 小时。
BCL6 对淋巴系统至关重要,没有 BCL6 基因的小鼠会因复杂的炎症反应而死亡。BRD4 在许多过程中都与基因组功能和稳定性密切相关。这项新的研究解决了人们对利用这些重要基因表达及其如何影响脱靶健康组织的担忧。
TCIP1 以一种环境特异性的方式发挥作用,需要同时存在 BRD4 和 BCL6 的表达,才能与它们结合,并在仅占BCL6总分子的一小部分的浓度下起作用。
在小鼠模型中,这些作者发现 TCIP对缺乏 BCL6 的细胞无毒性。没有 BCL6 的三阴性乳腺癌细胞系不受 他们设计的TCIP的影响。
TCIP1在脾脏中诱导了巨大的转录组变化,特别是FOXO3基因的上调,这反映了靶癌细胞中的活性。尽管脾脏的转录组发生了显著变化,但 TCIP1 的耐受性很好,没有不良反应,小鼠体重没有明显差异,也没有出现炎症浸润或细胞凋亡等明显异常。
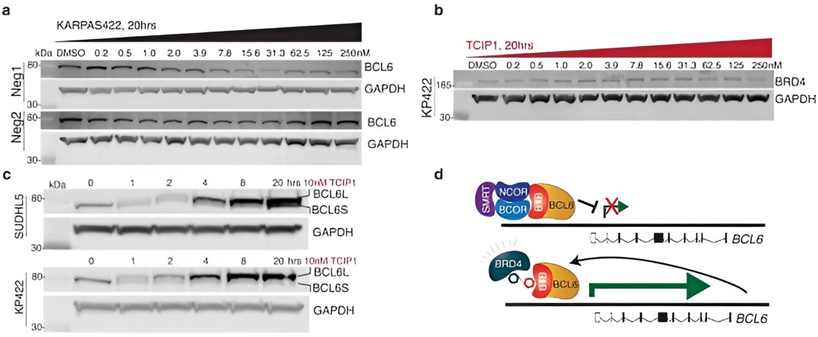
图片来自Nature, 2023, doi:10.1038/s41586-023-06348-2
TCIP 仅通过将每个细胞中的部分癌症驱动分子重新连接在一起来产生作用。在这项新研究中使用的剂量浓度下,TCIP1能使BCL6位点的BRD4升高1.5倍,对其他位点的常规活性几乎没有干扰,同时还能在癌细胞内发挥强大的基因激活和细胞杀伤作用。这表明TCIP可能能够被开发成一种治疗药物,但还需要更多的研究来证明它们的安全性。
这些作者认为,小分子 TCIP对基因的激活作用可能会应用于生物学和医学的许多其他领域。例如,TCIP可能经设计后用于激活衰老细胞的死亡途径,激活治疗基因或单倍不足的基因的表达,激活人类免疫疗法中新抗原的表达,或调节细胞或生物中的基因表达以便用于合成生物学应用。
虽然在开发的早期阶段很难评估一种新方法的治疗潜力,但这种方法显然具有创新性,在各种病理学中都很容易获得和使用。
文章来源“生物谷”