近日,Nature Chemical Biology在线发表了中国药科大学郝海平/叶慧团队最新研究成果:Chemoproteomic mapping of the glycolytic targetome in cancer cells。中国药科大学田扬博士、皖宁博士、邵畅博士及张汉卿博士研究生为本文共同第一作者,郝海平教授和叶慧研究员为本文共同通讯作者。合作作者还包括我校王广基院士、生命科学与技术学院丁明研究员、胡海洋副研究员、药学院孙慧涌副研究员,南京大学陈帅教授团队以及我校研究生鲍秋雨、刘宸光等。研究还获得了药学院肖易倍教授、药物科学研究院江炜老师的协助和支持。
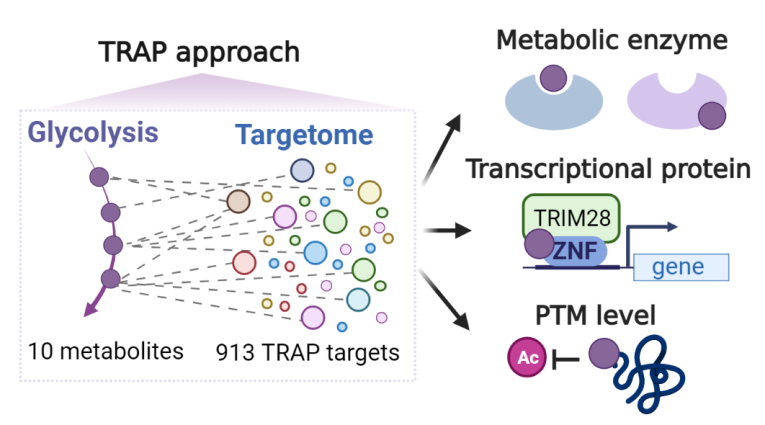
示意图
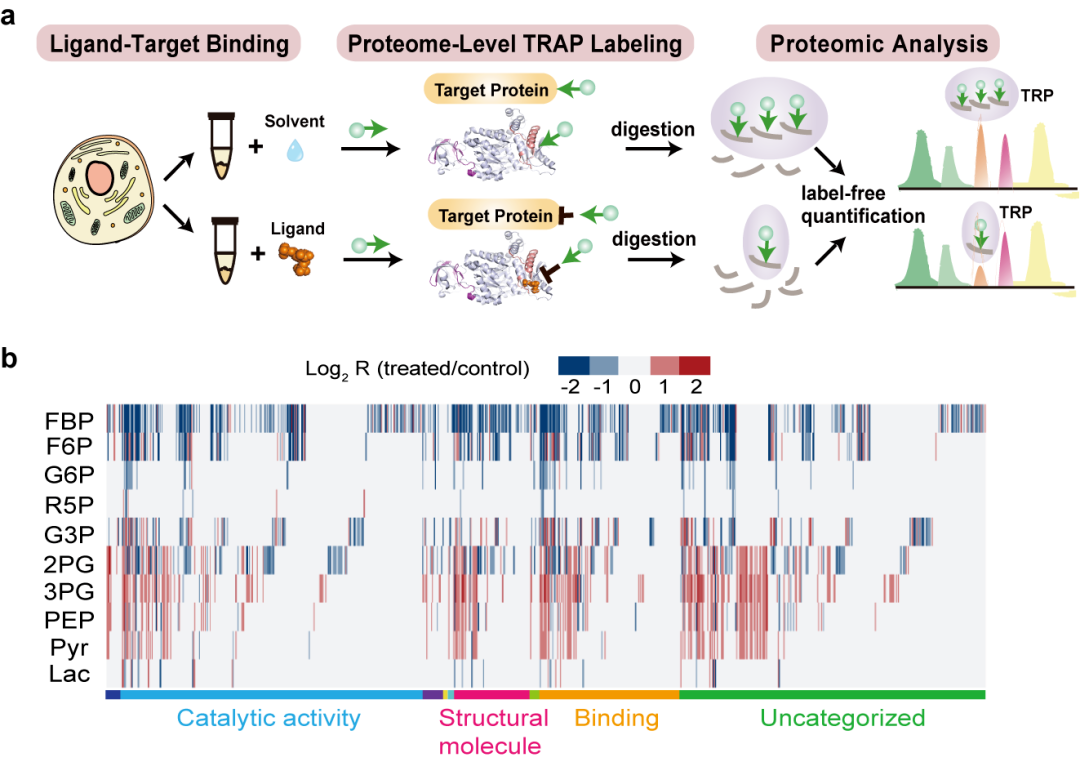
研究聚焦于大多数癌细胞中过度活跃的糖酵解通路。基于前期多个重磅研究揭示出糖酵解通路上部分代谢物可以作为信号分子发挥非代谢的功能,研究团队提出通过描绘糖酵解通路上主要代谢物的靶标组,全面理解糖酵解支撑肿瘤发生发展的机制。为了高通量描绘多个代谢物的靶标,郝海平/叶慧团队在现有靶标发现技术体系中寻求创新,建立了靶标响应可及性变化谱TRAP技术(Target-Responsive Accessibility Profiling)。TRAP通过标记全蛋白组水平赖氨酸来表征蛋白的溶剂可及性,再通过比较配体结合前后蛋白可及性的变化,鉴定靶标及配体结合区域,具有互补于现有靶标发现方法的技术优势。
利用TRAP技术,团队在模型癌细胞系中共描绘了10种糖酵解代谢物的靶标组,共发现913个可及性变化的候选靶标。进一步的机制研究揭示了糖酵解代谢物对靶标组的丰富调控模式,包含干扰碳代谢酶的活性、影响转录蛋白的功能及靶标的翻译后修饰水平等(见示意图)。上述结果确证了癌细胞中糖酵解代谢物除了参与代谢层面的活动以外,还作为信号分子发挥全局调控功能,为后续基于糖酵解代谢物的靶标组挖掘癌症治疗靶点提供了重要的线索与数据资源。
新闻封面图
本文转载自“生物谷”