2019年,耶鲁大学陈列平教授研究组关于Siglec-15和FGL1两个全新的抗肿瘤免疫靶点的研究相继在全球著名学术杂志《Nature Medicine》和《Cell》发表,在生物医药行业引起轰动。
作为操刀这两个新靶点的第一作者和陈列平教授的资深弟子,沉隐多年的王俊博士开始进入大众视野。

王俊博士
师从肿瘤免疫领域巨擎陈列平教授,在旁人看来顶着巨大的光环,科研之路似乎应是一帆风顺,然而在两项重磅研究见刊之前,王俊博士在美国十年博后生涯却基本无任何文章发表。
全新分子探索的背后是一次次失败的挣扎和怀疑,中间的放弃或坚持,是怎样的一段历“炼”?
10月30日-11月1日,同写意将汇集近两百位一线一流专家,安排一天主论坛和一天半7个平行分论坛,在苏州凯宾斯基大酒店举办同写意成立15周年全球生物医药前沿技术与政策法规盛大会议。美国纽约大学研究员王俊博士受邀作为本次大会分论坛一“抗体药物发现与创新:未来我们能做什么”的联合策划人之一,并展开主题演讲“FGL1/LAG-3:一种新的肿瘤免疫逃避通路”。
01 如果不是陈列平教授,我不会学免疫学
2004年的夏天,从南京工业大学生物化工专业临近毕业的王俊,决定从生物工程下游技术转向基础生物科学。
他用一封长达八页的手写信,阐述了自己从小到大对科学的理想,对科幻的痴迷,其真情实感打动了中国科学院生物物理研究所(IBP)的毕汝昌教授,得到了一份难得的实习机会。
彼时IBP以蛋白质结构解析见长,感染与免疫中心也刚刚成立,并从海外邀请了陈列平、刘勇军、傅阳心、苏立山、刘阳等七位著名华人免疫学家组建海外团队,回国招收学生联合培养。一次机缘巧合的学术报告中,王俊遇到了自己后来的导师陈列平教授。
1999年,陈列平教授实验室首次克隆人类B7-H1(PD-L1)并鉴定其T细胞调节功能(Nature Medicine,1999),在后面的几年内,又陆续鉴定了B7-H2、B7-H3和B7-H4等免疫调节分子,这些发现深刻影响了肿瘤免疫领域后来的药物研发方向。
“那时教授在讲B7-H4,有趣的是我在IBP听了无数的报告,基本上都能听得懂,但他讲的东西我什么都不懂,却觉得十分有意思“。
回忆起这段与恩师初始的趣事,王俊直言自己当时甚至不知道台上的老师就是肿瘤免疫领域大名鼎鼎的陈列平教授。
因为听不懂,所以提出留下参加报告后的座谈会。恰逢那次也是陈教授回国招生,于是他就成了陈教授在IBP的第一批学生(和王盛典教授联合培养),自此踏入了免疫领域。

王俊博士与导师陈列平教授
21世纪初,是全球免疫治疗遇冷的时候。在陈列平教授和王盛典教授的指导下,王俊选择了中国特色的乙肝方向开始了他免疫生涯的启程,希望解决乙肝病毒的基础免疫学问题:如何用免疫调节的办法打破乙肝病毒的T细胞肝脏免疫耐受。
他花了四年半的时间完成了硕博的工作,用一个HBV转基因小鼠模型意外的发现了如今肿瘤免疫行业大热门的4-1BB抗体肝脏毒性的现象,并首次建立了一个真正模拟临床表征的,由T细胞引起的肝炎到肝癌转化的动物模型,至今仍被很多实验室使用。
提及博士期间的研究,王俊表示这与他在IBP接受的训练密不可分:IBP感染与免疫中心的七位世界级海外免疫专家轮番精心指导,以及IBP联合导师的手把手教学,这种高水准,开放的培养模式,不亚于在当前美国顶尖高校的训练。
02 春风化雨 十年磨剑
2009年初,王俊前往美国开始他的博士后研究。
从上个世纪九十年代开始,陈列平教授就以他在肿瘤免疫领域里的独到见解和坚韧的毅力,鉴定PD-L1/PD-1,4-1BB等通路在肿瘤免疫中的重要作用并推动了其在免疫治疗中的应用。
早年,抗4-1BB的刺激性抗体在动物实验中抗肿瘤效果非常好,甚至有些时候优于抗PD-1抗体。
然而也正是2009年初,两种疗法的临床数据初步结果显示,PD-L1/PD-1疗法富有成效而且副作用也比较小;不少病人的肿瘤得到很好的控制并且生存期得到很大的延长,逐渐引起了全世界的关注和轰动;并成为全球药企竞相研发的药物靶点;然而抗4-1BB抗体却在人体具有比较严重肝脏毒性不得不在当时终止临床实验。
两种疗法在临床前和临床后表现出的很大差异也引起陈列平教授课题组对免疫治疗靶点机理的深入思考,再加上抗PD-L1/PD-1疗法也只是对20~30%的肿瘤患者有效,自此,寻找一些潜在的免疫疗法新靶点就成了王俊的博士后课题。
• 2009-2010年两年的时间内,王俊克隆和表达 一个个新基因,一个个进行筛选均以失败告终。最后克隆出了一个功能未知的新分子——Siglec-15。后续的多年潜心研究(和孙静玮博士合作)表明这是一种不依赖于B7-H1/PD-1途径的新型免疫抑制分子。
• 2011年初,王俊跟随陈教授从约翰霍普金斯大学医学院去了耶鲁大学医学院。为了继续寻找潜在的免疫疗法新靶点,继续完善并创建新的基因组筛选平台。每天的工作就是继续找靶点、克隆基因、做蛋白、不停的筛选以及提出新的假说。
• 2011年下旬,王俊克隆出了纤维蛋白样蛋白1(FGL1),后来证实了FGL1是一种独立于MHC-II的LAG-3的主要功能配体,揭示了又一种新的免疫逃避机制。
• 2014年,历时近5年,全基因组新分子筛选平台终于基本建好。但不久,王俊暂停了大张旗鼓的新靶点筛选,选择了深挖一两个项目(Siglec-15和FGL1),钻研其生物学机制以及转化潜能。
• 2015年,辅助陈列平教授成立NextCure,开始和公司合作开发Siglec-15单克隆抗体(NC318),进行机制研究,以及推进人体肿瘤免疫治疗临床试验的开展。而FGL1的项目则选择和Boehringer Ingelheim合作,双线并进。
• 2019年,Siglec-15(Nature Medicine,2019)和 FGL1/LAG3(Cell,2019)研究成果相继见刊,王俊终于在这一年迎来自己文章的收获期,并开始被大众熟知。
※ NC318的first in human临床实验于2018年下半年在美国开始,目前一期临床临近结束。而NextCure也于2019年5月在纳斯达克上市。
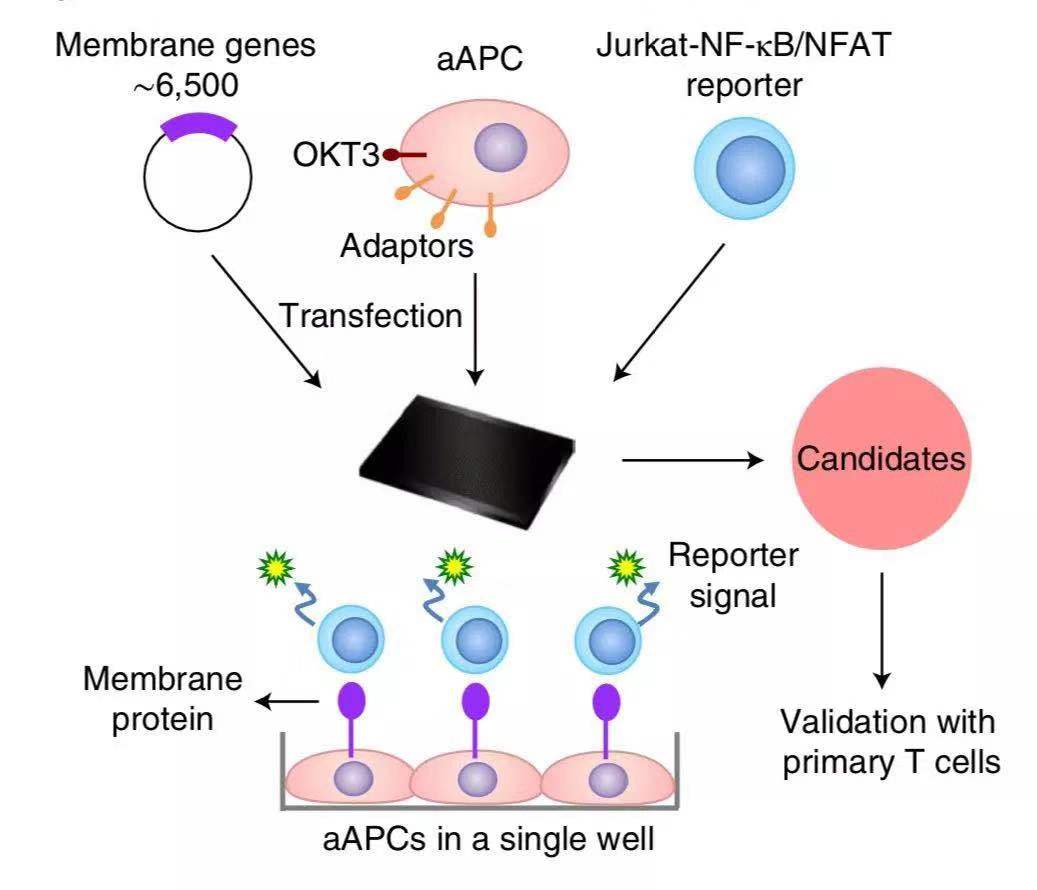
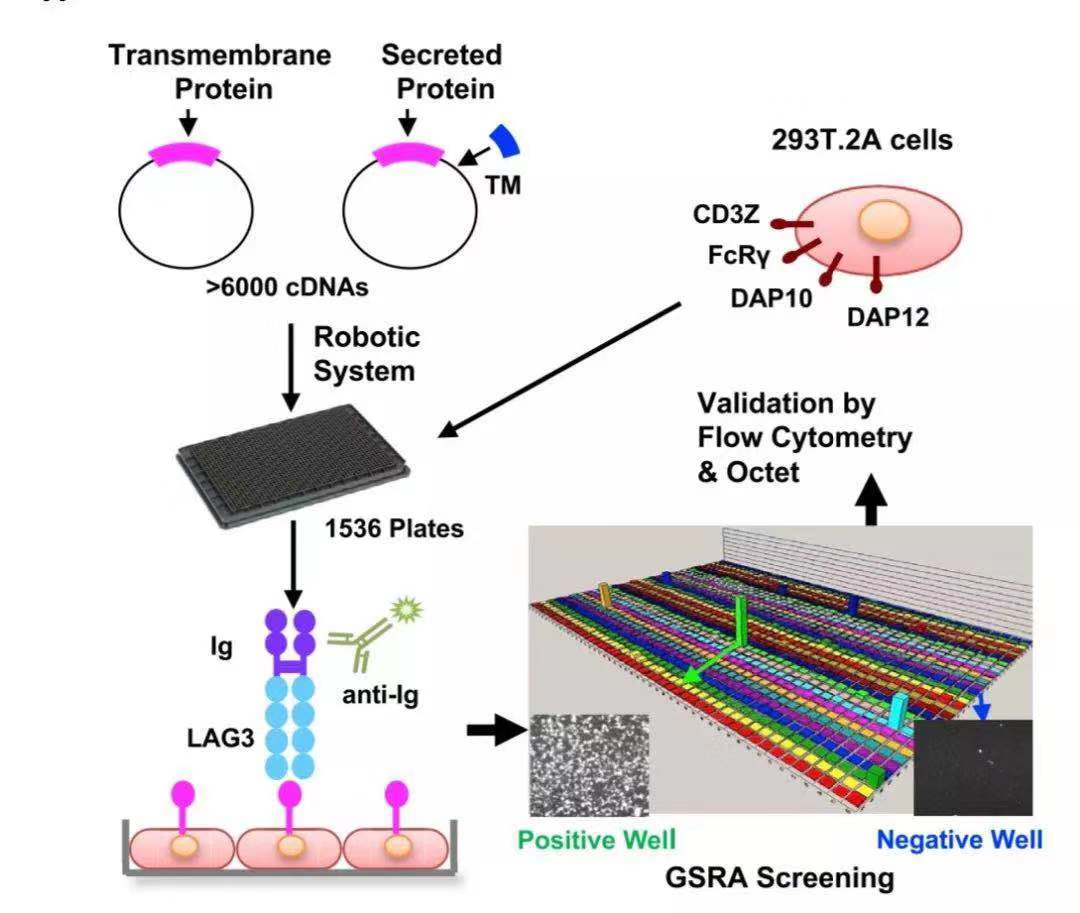
筛选平台示意图
03 媲美PD-1的Siglec-15?
Siglec-15的研究结果发表之后,媒体渲染用媲美PD-1来形容Siglec-15。
Siglec-15有何“魔力”?王俊博士向我们介绍,他们最初发现Siglec-15的蛋白质序列分析显示其细胞外结构域包含一个免疫球蛋白可变区(IgV)和一个2型恒定区(IgC2),与B7基因家族成员(比如PD-L1)有30%以上的相似性,暗示了Siglec-15与B7基因家族关系密切,可能与B7家族成员一样,具有免疫调节功能。
进一步的实验证明,Siglec-15通过依赖IL-10发挥抑制功能,其单克隆抗体α-S15也的确能阻断Siglec-15对抗原特性T细胞的抑制作用,且免疫抑制不依赖于B7-H1/PD-1途径,这就为当前免疫治疗无响应,尤其是对anti-PD-1/PD-L1治疗不响应的患者提供了新的候选方案。
谈到Siglec-15是否能媲美PD-1这一说法,王俊博士表现得很是冷静。
“免疫逃逸机制是理解肿瘤细胞和免疫细胞之间相互作用的关键点。这些分子存在于T细胞上,也会存在于其他免疫细胞比如NK和巨噬细胞上。Siglec-15就是这样一个主要在巨噬细胞上的新靶点。它和PD-1是两个东西,它们在不同生物过程中发挥作用,具有不同的机制,不好直接比较;而且不到临床最后谁都不知道最终效果到底如何”。
后续怎么样去发现更多这样的靶点,以及药物联用的内在逻辑,这些是肿瘤免疫领域很重要的方向。

Siglec-15,Nature Medicine,2019
04 NextCure的新模式
Siglec-15能引起业界不小反响的另一个原因是对该分子惊人的药物研发速度。
王俊博士参与研发Siglec-15单克隆抗体α-S15(NC318)的进程,对业界来说也许是一个很好的范例。
早在2018年10月,NC318的临床1/2期研究(NCT03665285)就已经开始招募患者了,适应症为多种实体瘤,包括肺癌、子宫癌、头颈癌等;而那时论文还在审稿阶段,没有发表。
直到今年三月论文在Nature Medicine发表,而此时NC318的一期临床已经进行一半。
这种先推临床,后发表论文的模式在国内十分罕见。在国内,如果有公司对最新的科学研究感兴趣,是等成果写成文章,经过同行评议,发表之后才有可能发生。
然后企业经过和学校协商引进专利授权,期间可能要等上十多年产品才能上临床。这也是国内学术界与产业界之间存在的一道转化的鸿沟。
谈及国内学术成果转化,王俊博士表示出些许担忧。
“目前中国许多生物制药公司只关注后期开发、产业化,而不大重视基础研究。如果只从国外License一个项目回来,不去做背后更深层次的机理研究,对于创新药来说很难做成,也会造成产品高度同质化”。
美国有相对成熟的转化系统,学术界专注做研究,小型的初创公司去做转化型的研究,然后有大公司来买单继续做产业化推向市场,这是一条成熟的生态链。
所以很多大公司看似没有去做早期的研究,其实也有创新的产品出现。
而Nextcure和耶鲁的合作,是一种学术界和工业界齐头并进的新模式。在Siglec-15单克隆抗体(NC318)研发过程中,Nextcure和耶鲁实验室是一起研究机理的,双方实验的最新数据也是共享的。
“每两周一次的交流会,双方都把Siglec-15当成自己的孩子,研发进行到每一步大家都很明确,任务也比较清晰。这种独特的合作模式也使得Siglec-15项目走的很快”。
还有,王俊表示虽然早期大家都不知道Siglec-15有多好,但都还是静下心来愿意一起去尝试和探索。很多事情急不来,尝试和探索是一个好的研究心态。

NextCure
05 寻找新的免疫靶点就像在人类基因组里面钓鱼
回顾这段摸着石头过河的过往,王俊博士不胜唏嘘。旁人看来风景无限,但背后的挣扎和自我怀疑,只有自己知道。
刚进耶鲁的前几年,王俊也走了很多弯路。那时筛选平台还没搭好,不知取舍,心态比较着急,经常被一些不重要的东西给缠了进去,就连Siglec-15这个靶点也差点被劝阻放弃。一次次的实验失败,异常难熬。
是什么支撑他一路走下来?王俊向我们分享了他的三个重要精神支柱。
第一是他对科研的着迷以及执着。为了搞明白一个问题,废寝忘食是经常的事。
第二是恩师陈列平教授在精神上的鞭策。
谈及自己的导师,王俊博士神情中尽是感恩和尊敬。“有洞察力,有决心,有耐心,一辈子做好一两件事情,顶级的科学家,难得的学术和工业思维兼具的一个人”。
“好的科学只是在现有的阶段往前走那么一点点就行,但一定是得往前走。”这是陈教授初遇王俊的一句话,却也是对其科研态度影响一生的话。
此外,多年钻研的爱好也成为了他的一个重要支柱。在科研做的痛苦的时候,他就经常去海边扔石头,进而开始喜欢上了钓鱼。
如何收获一个良好的研究者心态,采访的最后,王俊用自己学习钓鱼的故事做出了一些有趣的分享。
在耶鲁大学附近的长岛海湾里有一种鱼叫海鲈鱼,这种鱼在美国东岸非常有名,所有钓鱼者都想钓这种鱼,但是难度非常高。此外,这种鱼只有钓到28英寸以上的,政府才允许你带走,小的海鲈鱼是不能带走的,必须得放回水里。
“我从想做这样的事情到钓到第一条可以带走的keeper海鲈鱼花了整整三年的时间,中间想了各种各样的办法,利用周末研究这种鱼的习性,钓鱼的时间、地点、温度、气候,路亚(lure)的种类、重量、颜色,调整各种装备甚至是手的抖动方式等等。有一天终于钓到了,非常大,而且和朋友一下钓到三条”。
大鱼一次次在激荡的水花里被拉出水面,伴随着的是巨大收获的愉悦心跳。自此之后王俊就把那张照片贴在工作的地方,觉得非常有成就感”。
寻找新的免疫靶点就像在人类基因组里面钓鱼,鱼群聚集的好钓点通常没那么好找,需要披襟斩棘,趟深水,过泥淖;有时海钓时,风浪过大还可能会在海上翻船流落孤岛。
不过因为钓鱼,看过朝阳静静地在船头升起,清冷平静的湖面和血色的天边相接;看过夕阳霞光万丈,金色的海浪波光粼粼;看过流星在湖边那棵树头上坠落,野鸭在孤月影照的芦苇荡里惊叫着飞起。这一切,潮起潮落,云淡卷舒,内心很容易平静下来。
钓鱼如此,做科研亦是如此。
深研甚至开创新方法新方向,需要有耐心,需要静下心去仔细琢磨;也更需要有激情、有开拓精神。

王俊博士与三年上钩的“海鲈鱼”
后记
2019年8月,王俊博士正式加入纽约大学(New York University,NYU)Langone Health,开始了自己的独立研究生涯。
在这里我们也期待这位华人科学家新秀可以在肿瘤免疫领域有更多新的发现,有更好的转化成果,造福全球肿瘤患者。
王俊博士美国纽约大学研究员 王俊曾是耶鲁大学免疫学系、耶鲁大学癌症中心陈列平教授实验室的助理研究员。
他在肿瘤免疫领域有超过十年的学术培训。王俊博士曾在约翰•霍普金斯大学和耶鲁大学先后进行博士后训练,此前他在中科院生物物理所获得免疫学博士学位。
他的研究兴趣在于发现和理解新的受体和配体在免疫调节过程中的功能以及如何最好地利用它们,成为癌症免疫疗法的潜在靶点。
近些年,王俊开发了数个基因组水平筛选平台对工业界产生了价值,为新锐生物技术公司 NextCure打下基础。他发现数个first-in-class靶点,如Siglec-15、FGL1/LAG3,代表了新的肿瘤免疫逃避机制,为癌症免疫治疗提供了新方法。目前针对Siglec-15通路的人体临床试验正在美国进行。
参考文献:
1. Jun Wang et al. Siglec-15 as an immune suppressor and potential target for normalization cancer immunotherapy. Nature Medicine, 2019
2. Jun Wang et al. Fibrinogen-like Protein 1 Is a Major Immune Inhibitory Ligand of LAG-3, Cell ,2019
3. 华人抗体:Siglec家族--肿瘤免疫疗法新方向
4. 预防界:媲美PD-1,跨时代新药Siglec-15单抗横空出世!
5. 药明康德:专访陈列平教授:说到免疫治疗,我有些不同看法







