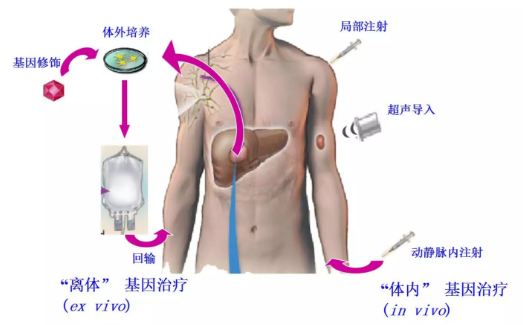
▲ 图1-基因治疗的主要方式
本文转载自“新叶社”,原标题:基因治疗的国内外研究进展。
1.发达国家和制药巨头加大基因治疗研发投入
美国对基因治疗领域的资助持续增加。2014年6月,美国国家卫生研究院(NIH)资助2500万美元,用于传染性疾病(疟疾和流感)的基因治疗研究。2015年底,美国白宫发布《美国创新新战略》,明确把包括基因治疗在内的精准医疗作为未来发展战略,未来10年将投入48亿美元重点资助。
欧洲对基因治疗领域的资助也持续增加。欧盟研究框架建立了专门基因治疗资助计划——CliniGene(2006-2011)计划,出资6580万欧元推动欧洲临床基因治疗的发展。“地平线2020”是欧盟最大的科研创新框架计划,其中基因治疗获得4910万欧元资助。2016年6月,法国政府宣布投资6.7亿欧元启动基因组和个体化医疗项目,项目为期10年,将重点开展基因组学、个体化医学、基因治疗等研究。
此外,跨国的制药巨头对基因治疗领域投入了大量资金。2014年12月辉瑞(Pfizer)与美国罕见病基因治疗公司Spark Therapeutics签署合作协议,共同开发B型血友病的基因治疗产品。2015年4月,百时美施贵宝(BMS)与基因治疗领域的领导者——荷兰的生物技术公司uniQure签署了一份高达10亿美元合作协议,共同开发重组腺相关病毒(AAV)表达载体的心血管基因治疗药物。2016年,百健公司宣布投资20亿美元与宾夕法尼亚大学以及REGENEXBIO公司合作开发基于AAV载体的基因治疗药物。
2.基因治疗研究开发和产业化已取得重要进展
截止到2017年4月,全球在Clinical Trial网站上登记了2463项基因治疗临床试验方案(图2),其中进入Ⅱ/Ⅲ期的基因治疗临床试验方案近500项,共有7个基因治疗产品已经在美国、欧盟、中国等国家上市。2012年7月,欧洲药品管理局(EMA)在欧盟范围内批准由uniQure公司研发的以AAV为载体的基因治疗药物Glybera上市,用于经严格限制高脂肪饮食却仍然发生严重或反复胰腺炎发作的脂蛋白脂酶缺乏症(LPLD)患者的治疗。此外,2014-2015年,Calledon、Spark Therapeutics和Bluebird Bio公司的产品MYDICAR、SPK-RPE65和LentiGlobin获得FDA批准上市。2016年5月,EMA批准了葛兰素史克(GSK)的药物Strimvelis用于治疗罕见病腺苷脱氨酶缺陷所致重症联合免疫缺陷症(ADA-SCID),这是首个上市的体外基因修饰的造血干细胞基因治疗产品。
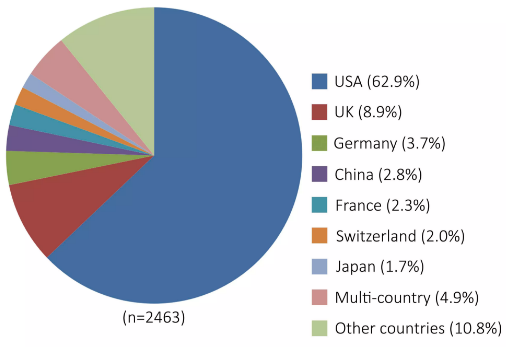
▲ 图2-全球主要国家的基因治疗临床试验方案分布统计
2017年8至11月,基因治疗领域迎来了4个里程碑事件。8月,FDA在全球率先批准诺华公司的CAR-T细胞治疗产品Kymriah上市,用于治疗复发或难治性急性淋巴细胞白血病。10月,FDA的专家小组全票支持批准Spark公司研发的AAV为载体的基因治疗药物AAV-RPE65(Luxturna),用于治疗RPE65基因缺陷引起的视网膜疾病,该药可以阻止患者向完全失明发展,有效地改善了患者的光感和视觉;同月,FDA批准了Kite Pharma公司的CAR-T基因治疗产品Yescarta上市,用于治疗成人复发/难治性大B细胞淋巴瘤;11月,美国Sangamo Therapeutics公司利用锌指核酸酶(ZFN)技术实现人类历史上首次患者体内基因组的编辑。
3.基因治疗研发的主要发展趋势
(1)重组腺相关病毒(AAV)载体基因治疗。重组AAV源于非致病的野生型腺相关病毒,具有安全性好、宿主细胞范围广、免疫源性低、在体内能长时间表达外源基因等特点,是最有前途的基因治疗载体之一。2017年11月,《新英格兰医学杂志》发表了一项临床试验结果:重组AAV基因治疗成功延长了15名身患严重遗传性疾病-1型脊髓性肌萎缩症(SMA1)患儿的生命,让他们有机会重获健康。此外,还有多种以AAV为载体的基因治疗药物正在开展II期或III期临床试验,其治疗对象几乎都是单基因遗传的罕见病,包括血友病A型和B型、地中海贫血、脊髓性肌萎缩症(SMA)等。
(2)慢病毒载体(LV)基因治疗。LV主要用于体外转基因研究。LV具有可感染非分裂细胞、转移基因片段容量较大、目的基因表达时间长、不易诱发宿主免疫反应等优点,是应用前景比较良好的病毒载体。Strimvelis、Kymriah和Yescarta等基因治疗药物所用的载体都是LV。
(3)基因修饰的溶瘤病毒基因治疗。携带治疗基因的溶瘤疱疹病毒、溶瘤腺病毒、新城疫病毒等治疗恶性肿瘤发展前景良好。近年来,跨国药企纷纷布局溶瘤病毒项目。安进、辉瑞、阿斯利康等跨国药企都参与了溶瘤病毒项目。如2011年,安进公司以10亿美元收购了专业的基因治疗公司BioVex公司(主打产品为GM-CSF修饰的疱疹病毒OncoVEXGMCSF);2015年10月,FDA批准该产品上市,用于治疗黑色素瘤。
(4)CRISPR/Cas9等基因编辑技术用于基因治疗。近年来,基因编辑技术迅猛发展,正在革命性地改变整个生物技术领域。与传统基因治疗方法相比,基因编辑技术能在基因组水平上对DNA序列进行改造,从而修复遗传缺陷或者改变细胞功能,使得彻底治愈白血病、艾滋病和血友病等恶性疾病成为可能。基于锌指核酸酶(ZFN)基因编辑技术的两种抗艾滋病和一种B型血友病产品已经进入临床阶段。CRISPR/Cas9基因编辑技术对特定基因组DNA的定位更加精准,成本更加低廉,正在成为基础研究和临床应用的主流技术(图3)。最近,美国、英国、日本政府都放开了对基因修饰人胚胎的限制,开展了一系列基因编辑技术修饰胚胎,从而对先天性遗传病进行基因治疗的研究。
▲ 图3-使用基因剪刀(CRISPR)修改基因组DNA
4.国内科技发展现状
我国政府对基因治疗等相关的基础研究、目标产品及关键技术的研发非常重视,“十一五”和“十二五”期间,863计划对重大疾病的基因治疗专门立项,参加单位包括二十多家国内从事生物治疗研究的优势单位,10余家国家重点实验室和多家专业的公司,储备了一批具有自主知识产权的生物治疗相关技术和项目。同时,973计划也资助了基因治疗的基础研究和应用基础研究项目,取得了多项重要的研究成果,论文发表在Nature、Science及Cell等国际顶级期刊上。
我国基因治疗研究及临床试验与世界发达国家几乎同期起步,主要以肿瘤、心血管病等重大疾病为主攻方向。我国已经有2个基因治疗产品上市,主要用于头颈部的恶性肿瘤治疗。此外,我国还有近20个针对恶性肿瘤、心血管疾病、遗传性疾病的基因治疗产品进入了临床试验,其中在Clinical Trial网站上登记的基因治疗临床试验方案有70个,占亚洲基因治疗临床试验方案总数的46.7%(图4)。如华中科技大学等研发的肿瘤基因治疗产品ADV-TK对肝癌和难治复发性头颈癌都具有显著疗效,正在开展多中心的Ⅲ期临床试验。中山大学等研发的重组人内皮抑素腺病毒注射液(E-10A)治疗晚期头颈鳞癌效果较好,目前该产品在中国和北美地区开展Ⅲ期临床试验研究,发展前景好。军事医学科学院研发的治疗心肌梗塞的基因治疗产品Ad-HGF注射液进入II期临床试验,与人福医药公司合作研发的治疗肢端缺血的基因治疗产品重组质粒-肝细胞生长因子注射液获得了Ⅲ期临床批文。成都康弘生物研发的治疗头颈部肿瘤的工程化溶瘤腺病毒基因治疗制剂KH901已完成II期临床试验。四川大学等研发的具有抗肿瘤血管生成的基因治疗产品EDS01正在开展Ⅱ期临床试验研究。
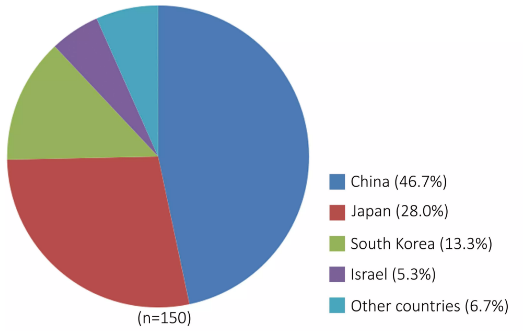
▲ 图4-亚洲主要国家的基因治疗临床试验方案分布统计
此外,我国还有40多项重大疾病的基因治疗制剂处于临床前研究阶段,上百个项目处于实验室研究阶段。
我国在基因编辑治疗领域也处在世界前列。2015年4月,中山大学的黄军就团队首次在人类胚胎细胞中进行了基于CRISPR技术的基因编辑操作,并于2017年9月再次报道利用单碱基编辑系统在人类胚胎基因组精确修复特定类型的单碱基突变(地中海贫血症HBB-28)。2016年,四川大学华西医院在国际上率先开展了CRISPR/Cas9基因编辑技术治疗肺癌的临床研究。
虽然基因治疗的研究已经取得了较显著进展,但仍然存在一些安全性及伦理问题,值得进一步研究。临床试验应严格按照获得批准的技术规程与标准操作,重视基因治疗技术的安全性,充分保障病人知情权,保护病人隐私。尽管基因治疗研究还存在很多待解决的技术难题以及一些法律或伦理等方面的问题,但这并不妨碍人们对其治愈重大疾病寄予厚望。