肿瘤免疫疗法是当前肿瘤治疗领域最具前景研究方向之一,各大药企纷纷寻求与其他公司合作研发肿瘤免疫相关治疗方法。初步的临床试验结果表明其治疗有效率非常高,Science杂志也将肿瘤免疫疗法评为2013年十大科学突破第一位。本文首先介绍肿瘤免疫疗法在肿瘤治疗中的地位,然后是作用机制和具体分类,已经上市或在研药物、市场预测,最后列举各公司之间的收购合作及国内部分参与相关研发的公司。
肿瘤治疗发展历程
1.传统疗法:包括手术切除、化疗、放射线治疗。其具有局限性:手术切除的方式常因为癌细胞入侵蔓延到邻近组织或远端转移而效果有限;化疗受限于对体内其他正常组织的毒性;放疗辐射也同样会对正常组织造成伤害。传统疗法都是对身体有极大负担,并且在发生恶性转移后,无论是何种方式都是很难彻底治愈。
2.靶向疗法:20世纪末出现的靶向疗法是在细胞分子水平上,针对已经明确的致癌位点来设计相应的治疗药物,药物进入体内会特异地选择致癌位点来相结合发生作用,使肿瘤细胞特异性死亡,而不会伤及肿瘤周围的正常组织细胞。包括小分子靶向药物和单抗。
小分子靶向药物:针对可能导致细胞癌变的环节,如细胞信号传导通路异常、过度表达某些受体蛋白、抗肿瘤血管形成等,从分子水平来一转这些恶性生物学行为,从而抑制肿瘤细胞生长。
单抗:诱导机体产生抗体依赖的细胞介导的细胞毒作用;作为靶向治疗的载体,将化疗药物、放射性同位素、毒素等细胞毒性物质特异性地运送到目标部位,而选择性杀伤靶细胞。
但靶向药物存在不足:主要有分子靶向药物有效性低,某种药物只能对特定突变基因型肿瘤产生作用;肿瘤基因突变产生药物耐受性导致长期的治疗效果下降;存在严重的不良反应;部分肿瘤不能通过靶向药物得到有效治疗。
3.免疫疗法:最新的肿瘤免疫治疗是通过调动机体的免疫系统,增强肿瘤微环境抗肿瘤免疫力,从而控制和杀伤肿瘤细胞。
初步的临床研究表明免疫疗法在晚期肿瘤种效果显著。耶鲁大学等机构研究表明,接受百时美施贵宝免疫检验点单抗nivolumab治疗后,出现了令人印象深刻的长期生存数据,有62%的患者在1年后仍存活,43%的患者在2年后仍存活。
纪念斯隆-凯特琳癌症中心在对16名晚期成人急性B淋巴细胞白血病(B-ALL)患者进行的嵌合抗原受体修饰的T细胞疗法结果显示,所有患者的整体完全缓解率为88%,远远高于补救性化疗的完全反应率。
肿瘤免疫疗法作用机制
免疫系统不仅负责防御微生物侵犯,而且能从肌体内清除改变了的宿主成分,机体存在着抗肿瘤免疫机制。当免疫监视功能由于免疫系统自身或肿瘤细胞原因被削弱时,便为肿瘤的发生提供了有利条件。
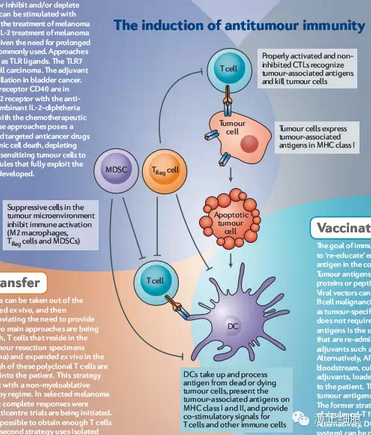
免疫系统识别与杀伤肿瘤细胞程序如下图所示包括:肿瘤细胞产生特异性抗原;树突细胞吞噬凋亡肿瘤,将肿瘤抗原呈递给T细胞;未受抑制并且激活的T细胞通过肿瘤特异性抗原识别并杀死肿瘤。其中免疫调节T细胞(TReg cell)通过抑制T细胞或解除抑制来调节T细胞活性,避免T细胞对体内正常细胞产生杀伤作用。
肿瘤免疫疗法即通过加强免疫系统在以上各个步骤中对肿瘤细胞的识别与杀伤能力。
肿瘤免疫疗法分类
根据不同机理疗法应用的时间先后排序,主要包括非特异性免疫刺激、免疫检验点单抗、过继细胞回输、单克隆T细胞受体疗法、CD47单抗等、肿瘤疫苗等。
1.非特异性免疫刺激:此类疗法的机理是通过刺激T细胞或抗原呈递细胞来加强抗原呈递过程,此外抑制免疫调节T细胞也能够增强T细胞活性。此类疗法70年代兴起但由于治疗时间长、毒性和治疗肿瘤范围限制导致应用受限。
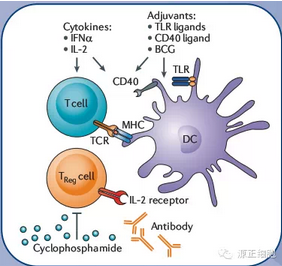
通过刺激T细胞来增强抗原呈递的药物包括:白细胞介素-2(IL-2)、干扰素α(IFNα)应用于黑色素瘤和肾癌。
通过刺激抗原呈递细胞来增强抗原呈递的药物包括:Toll样受体配体咪喹莫特用于治疗基底细胞癌,卡介苗(细菌制剂)用于膀胱癌局部灌注。
通过抑制免疫调节T细胞来增强抗原呈递的药物包括:结合免疫调节T细胞IL-2受体α链的CD25单抗。免疫抑制剂达利珠单抗Daclizumab(罗氏,2007),地尼白介素-2( Eisai ,2008)用于治疗皮肤性T细胞白血病及卵巢癌,环磷酰胺治疗肿瘤及自身免疫疾病。
2.免疫检验点单抗:
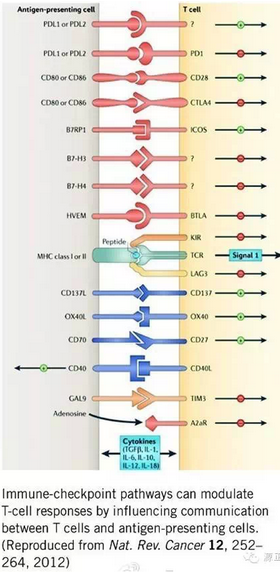
20世纪末随着对抗原呈递过程研究的深入,研究表明主动免疫治疗是激活自身的免疫系统T细胞或抗原呈递细胞来识别杀伤肿瘤细胞,T细胞的激活需要两个信号:一是MHC-多肽的信号,另一个是共刺激分子的信号,主要有正向共刺激因子CD27、CD28和CD137通路,此外为保证T细胞不被过度刺激,还有调节T细胞不被过度刺激的共刺激分子,主要有CTLA4通路和PD1/PDL1通路,这种抑制性的通路也会被肿瘤劫持用来对抗免疫系统。通过结合正向共刺激因子的激动剂,或结合负向共刺激因子的抑制剂都可以达到提高对肿瘤的免疫杀伤作用。
已经上市的有负向共刺激因子抑制剂CTLA4单抗Ipilimumab(BMS,2011),Ⅲ期临床表明25%的恶性黑色素瘤患者生存期超过2年,成为黑色素瘤治疗领域重大突破。
PD1/PDL1单抗比CTLA4单抗有更强的抗肿瘤作用。在研PD1 单抗有BMS的Nivolumab、Merck的Lambrolizumab、Cure Tech的Pidilizumab和GSK的AMP-224,在研PDL1单抗有罗氏的MPDL3280A和阿斯利康MEDI-4736。初步临床结果对晚期并且没有分子标记物指导的肿瘤患者有效率从13-38%不等。初步临床试验研究表明,接受百时美施贵宝免疫检验点单抗nivolumab治疗后,出现了令人印象深刻的长期生存数据,有62%的患者在1年后仍存活,43%的患者在2年后仍存活。
正向共刺激因子的激动剂有Celldex在研的CD27激动剂CDX1127,初步临床显示疗效显著,与PD1单抗联合治疗潜力巨大。在研正向共刺激因子的激动剂还有AZ的OX40抑制剂。
免疫检验点单抗会出现“延迟效应”,由于一些患者用药一段时间后才出现缓解,BMS和学界提出了延迟效应的概念,并且提出了一个新的肿瘤治疗疗效的评价标准——免疫相关的疗效评价。
同时也会出现与T细胞的过度激活和扩增有关的不良反应,一些患者的器官会发生临床上可观测到的自身免疫损伤。
免疫检验点单抗面临的挑战是,其仅能解除已经位于肿瘤边缘的T细胞的束缚或加强呈递,不能促使T细胞攻击肿瘤,一些病人并不免疫反应。
3.过继细胞回输:过继细胞疗法(ACT)主要包括肿瘤浸润淋巴细胞疗法(TIL)、T细胞受体疗法(TCR)和嵌合抗原受体修饰的T细胞疗法(CAR)。其中TCR和CAR分别通过识别抗原-MHC复合物和抗原能够特异性杀伤各类肿瘤细胞。
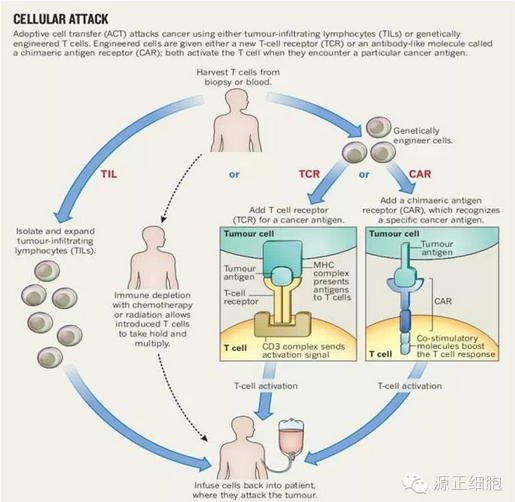
肿瘤浸润淋巴细胞疗法(TIL):从病人体内取出肿瘤组织,分离出其中的T细胞加入IL-2后扩增T细胞,然后回输体内扩大免疫应答,多联合化疗使用。只在转移性黑色素瘤上有效(40%长期缓解),因为在转移性黑色素瘤抗癌淋巴细胞会进入肿瘤内,因此比较容易分离,但很难从血液中收集其他非实体瘤的抗肿瘤T细胞。还有其他问题如体外培养细胞需要导致患者需要等待4-6周才能开始治疗、特异性抗癌T细胞体外培养扩增不太容易、治疗费用昂贵、扩增的抗癌T细胞也会被內源免疫系统抑制。Lion Bio在研相关产品。国内也有众多企业和医院合作开展TIL疗法。
T细胞受体疗法(TCR):提取患者外周血中的普通T细胞,通过病毒载体引入新的基因,使其表达能够识别癌细胞抗原的TCR以及一些免疫因子,从而激活引导T细胞寻找杀死癌细胞。优点是可以获得各类肿瘤抗原特异性受体从而治疗各种肿瘤,缺点是会攻击带有与肿瘤相同抗原的正常细胞,并且插入的TCR与体内MHC特异性结合难度大,导致实际肿瘤特异性结合能力不强。在研企业有Adaptimmune。
嵌合抗原受体修饰的T细胞疗法(CAR),CAR疗法与TCR疗法原理相似,只是将识别癌细胞的TCR换成类似于抗体的抗原受体,在受体另一端嵌合激活T细胞的元件,并在嵌合蛋白中引入多个共刺激分子,使得T细胞的生存能力、增殖能力、记忆效应增强,从而激活引导T细胞寻找杀死癌细胞。从发表的小规模临床数据来看,有些CAR疗法完全缓解率高达60%,并且都是其他治疗无效的患者。CAR似乎没有剂量效应,能够在体内产生扩增效应,有报道表明CAR在体内可以扩增千倍以上,但是一些无效的患者可能由于免疫功能减弱导致体内没有扩增。副作用也是攻击带有相同肿瘤抗原的正常细胞,引起细胞因子风暴,产生溶瘤症。后续的改进包括寻找正常细胞没有的肿瘤特异性抗原,加入嵌合共刺激受体能结合两种抗原的TCR以减少对正常细胞损害,加入不同共刺激因子作用不同肿瘤,和免疫检验点单抗或TCR联用,改进细胞培养技术。
有超过20项CAR疗法的临床试验正在进行,主要通过癌细胞表面的CD19识别,应用于成人急性B淋巴细胞白血病治疗,包括Novartis与Carl June,纪念斯隆-凯特琳癌症中心Michel Sadelain与Juno Therapeutics,Rosenberg与Kite Pharma,Buebird与Celgene等
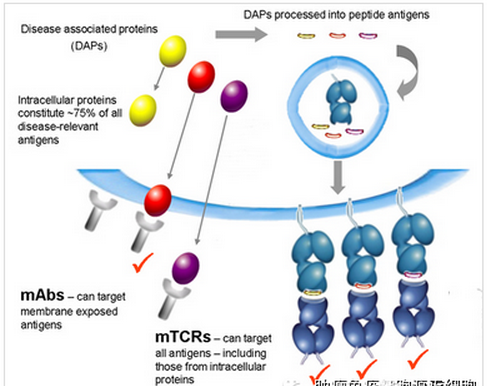
4.单克隆T细胞受体疗法:英国公司Immunocore开发单克隆T细胞受体疗法(mTCR),将能够识别肿瘤细胞表面和细胞内的mTCR与能够激活T细胞的anti-CD3 scFv连接到一起,病人输入这种mTCR药物后就能激活、引导T细胞寻找、杀死癌细胞。优点是不需要基因修饰T细胞,不用进行体外细胞培养,相比单抗能结合细胞内的大量肿瘤抗原。目前Genentech、GSK、AZ已与Immunocore结成战略同盟。
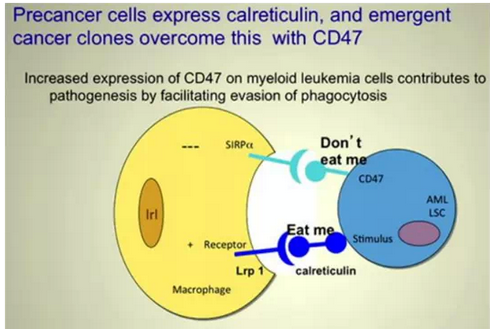
5.CD47单抗——阻断吞噬细胞“别吃我”通路:CD47单抗通过解除肿瘤对吞噬细胞的逃避作用,增强吞噬细胞对肿瘤的杀伤作用,临床前试验显示与肿瘤特异性单抗联用治疗效果明显。
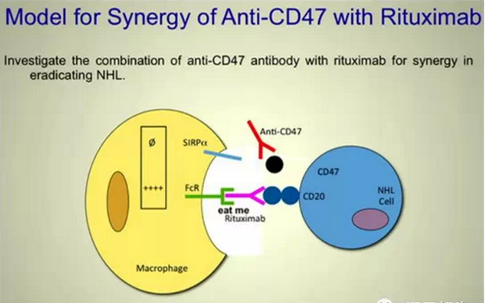
CD47广泛表达于不同组织细胞表面,如造血细胞(红细胞、淋巴细胞、血小板等)、非造血细胞(胎盘、肝和脑细胞等)及肿瘤细胞。原癌细胞同时表达促进吞噬细胞吞噬的钙网蛋白和抑制吞噬的CD47,两者处于动态平衡;病理状态下, CD47表达增加,抑制钙网蛋白介导的吞噬作用,使肿瘤细胞逃脱免疫监视。利用抗CD47抗体抑制或阻断CD47的信号路径,将是非常有效的肿瘤免疫治疗新途径。小鼠模型实验发现,抗CD47抗体能减轻淋巴瘤负担,提高存活率;如果和利妥昔单抗一起使用,则能治愈淋巴瘤。
6.肿瘤疫苗
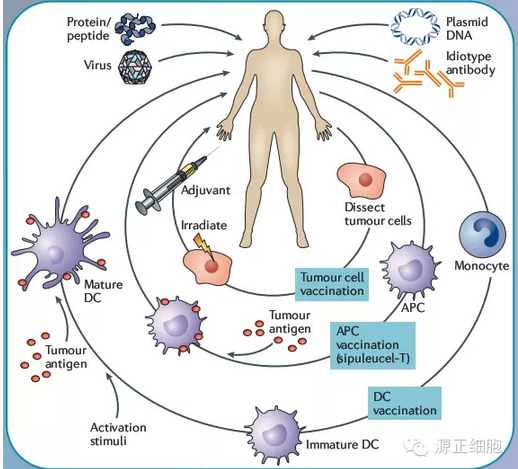
肿瘤疫苗作用机理是,在呈递细胞存在下通过肿瘤抗原刺激体内T细胞从而“驯化”其对肿瘤产生免疫杀伤作用,肿瘤抗原的形式包括蛋白、多肽、质粒DNA或病毒编码产物(病毒也有直接的溶瘤作用),特异性的抗体也可以作为某些B细胞恶性肿瘤的疫苗。此类疫苗都需要添加佐剂包括细胞集落刺激因子或Toll样受体配体。在研疫苗包括Biovest的非霍奇金淋巴瘤疫苗、GSK的非小细胞肺癌疫苗等,研发难度大。此外通过辐射灭活的肿瘤细胞也可以作为相应的肿瘤疫苗,俄罗斯2008年批准Antigenics的肾细胞癌疫苗。
另外一种方法是提取病人的抗原呈递细胞,在细胞因子或佐剂存在下装载肿瘤抗原到APC,回输体内。缺点是此类个性化定制的疫苗制作过程复杂费用高持久有效性差。FDA批准Sipuleucel-T(Dendreon,2010)用于治疗前列腺癌。
Gardasil(MSD,2008) HPV疫苗是第一个获准上市的用来预防由HPV 6、11、16和18型引起的宫颈癌和生殖器官癌前病变的癌症疫苗。严格来说HPV疫苗算不上癌症疫苗,只是一种病毒疫苗,这种抗癌机制推广不到其他肿瘤适应症。
肿瘤免疫疗法在研及上市药物
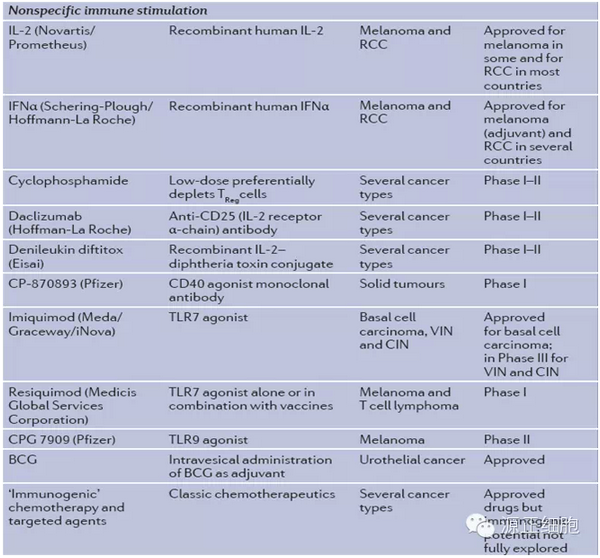
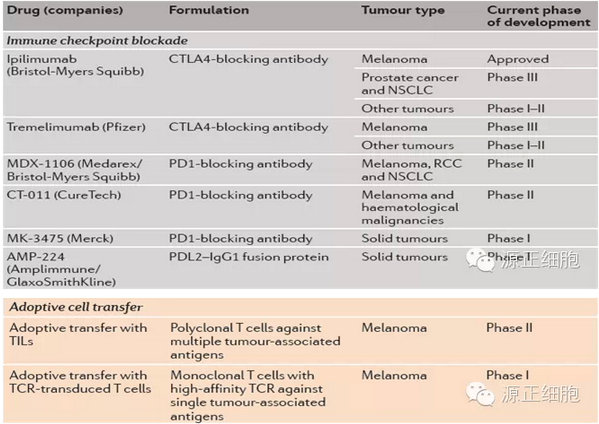
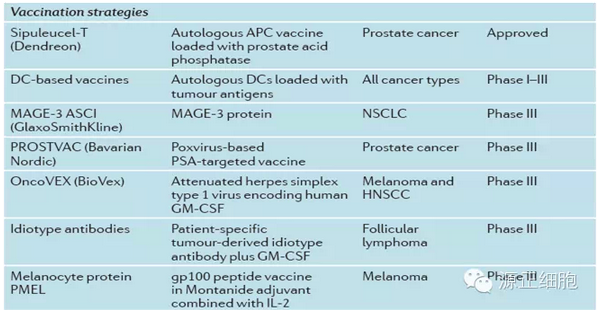
目前在研肿瘤免疫疗法药物集中于免疫检验点单抗、T细胞受体疗法和嵌合抗原受体修饰的T细胞疗法、单克隆T细胞受体疗法、CD47单抗等、肿瘤疫苗等。已上市及部分在研药物如下表所示。
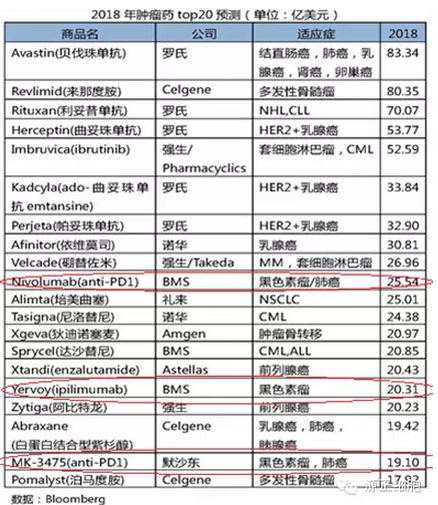
肿瘤免疫疗法药物市场预测
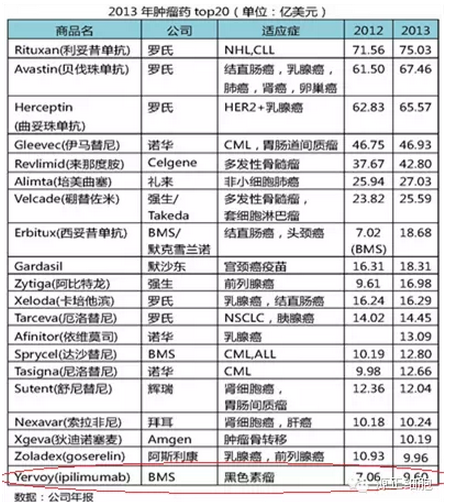
彭博预计2018年肿瘤药前二十药物中有3个免疫疗法药物,包括BMS黑色素瘤药物PD1单抗Nivolumab、CTLA4单抗Ipilimumab和默克的黑色素瘤肺癌药物PD1单抗MK-3475,2013年数据只有2011年上市的Ipilimumab。
花旗银行预测,未来十年癌症免疫治疗药物用于60%的晚期癌症患者,有可能会成为潜在的最大药物类别,2023年销售额将超过350亿美元。
肿瘤免疫疗法市场收购与合作
近两年各大药企纷纷进入肿瘤免疫疗法领域,在以下列举的近期国外交易中,可以看出主要集中在免疫检验点单抗、嵌合抗原受体修饰的T细胞疗法及单克隆T细胞受体疗法。
14年4月10日,GSK跟随AZ、Pfizer、JNJ与MD Anderson癌症研究中心将合作开发anti-CTLA-4抑制剂追赶目前领先的Merck、Roche和BMS,后三家公司专注在PD-1和PD-L1上。
14年3月19日,MSD宣布自家的PD-1单抗(MK-3475)要和3家公司的药物合用:Pfizer的PF-05082566以及axitinib;Incyte 的INCB24360;Amgen的talimogene laherparepvec。
14年3月17日,BMS同意支付给Five Prime 3.5亿美元获得后者两个免疫检验点单抗类药物,费用包括2000万美元的前期款,950万美元的研究费,并以2100万美元获得后者4.9%普通股,以及3亿美元的里程金,还有个位数至两位数的销售提成。BMS获得合作获得药物全球权益。
14年2月17日,诺华公司最近宣布收购美国的CoStim医药公司以获得相关技术进一步发展其PD-1靶向疗法。
14年2月17日,Servier宣布将与法国公司Cellectis合作开发UCART19以及另外5个同类项目,这些项目是对抗白血病和淋巴瘤的CAR疗法。Servie将支付1000万美元前期款以及每个项目1.4亿美元里程金。
14年2月13日,Pierre Fabre获得除印度外全球所有地区独家开发和销售Aurigene的癌症免疫治疗候选药AUNP-12的权益,机理是通过多肽阻断免疫检验点通路。Aurigene将获得一笔前期款和里程金。
14年2月3日,MSD与ABLYNX合作开发免疫检验点单抗相关药物。
14年1月14日,Juno Therapeutics与纪念斯隆-凯特琳癌症中心等合作开发CAR疗法。
14年1月8日,AZ跟随Genentech、GSK与Immunocore达成合作协议,利用mTCR技术平台共同开发TCR类抗癌药物。阿斯利康就每个项目需支付$2000万预付款+$3亿里程金+销售分成。
13年8月26日,AZ 收购一家专注于早期癌症免疫药物研发的公司Amplimmune,收购价为2.25亿美元的前期款加上2.75亿美元的潜在里程金,后者研发免疫检验点单抗,拥有尤其出名的IMT-C平台和一款临床前的单抗药物AMP-514。
13年2月14日,Jounce Therapeutics完成4700万美元A轮融资开发免疫检验点单抗。
肿瘤免疫疗法国内研发进展
目前查到的有,中信国健的CTLA4-Ig融合蛋白2005年进入临床,百济神州的PD1、PD-L1单抗在临床前阶段,香雪制药在研T细胞受体疗法,深圳源正细胞在研嵌合抗原受体修饰的T细胞疗法、多抗原负载的MASCT及Smart-T细胞疗法已进入临床应用,并开展了多中心的临床实验;此外301医院在开展多项嵌合抗原受体修饰的T细胞疗法临床试验。







