今年年初美国最大的抗体药物偶联物制造公司Seattle Genetics 斥资20亿美元买下Immunomedics旗下正在研发的抗体药物偶联物IMMU-132。同时Seattle Genetics公司的股价下跌了4%,因为外界认为这是Seattle Genetics的一次风险较大的豪赌。Seattle Genetics虽然财大气粗,但并不是人傻钱多,IMMU-132令人振奋的二期临床数据以及IMMU-132的前景才是Seattle Genetics豪赌的底牌。

IMMU-132在对69名多种治疗方案(平均接受过5种治疗方案)无效的晚期三阴性乳腺癌患者的二期临床数据中。2名患者肿瘤完全消除,19名患者肿瘤明显缩小,客观反应率达30%,并且疾病控制率高达69.5%,这意味着有69.5%的患者减轻了肿瘤的负担。最重要的是这种药物从用药到起效的平均时间仅需1.9个月,极大增强了患者的依从性。尽管是多种治疗方案无效的患者,在使用sacituzumab govitecan (IMMU- 132)过程中,无进展生存期也长达6个月。总生存期达16.6个月。在治疗过程中所有患者中都没有致死性的不良反应出现(1)。

IMMU-132靶向肿瘤细胞(红色)而对正常细胞
(蓝色)无影响(绘图by王爽)
有趣的是,4名患者在接受PD-1检查点抑制剂时仅对1人稍有作用,而另外3人全部对sacituzumab govitecan (IMMU- 132)敏感。因此在这些令人振奋的临床数据之下,FDA授予其突破性药物,以加速其上市。
同时在对小细胞肺癌的临床二期试验中,对49名晚期难治性小细胞肺癌患者进行治疗过程中,7名患者肿瘤组织明显缩小,21名患者病情得到控制。客观反应率为14%,临床获益率为35%。中位无进展生存期3.7个月,中位总生存期7个月,6名患者的总生存期达1年至2年多。并且无论是对一线化疗敏感还是不敏感的患者,它都有效(2)。
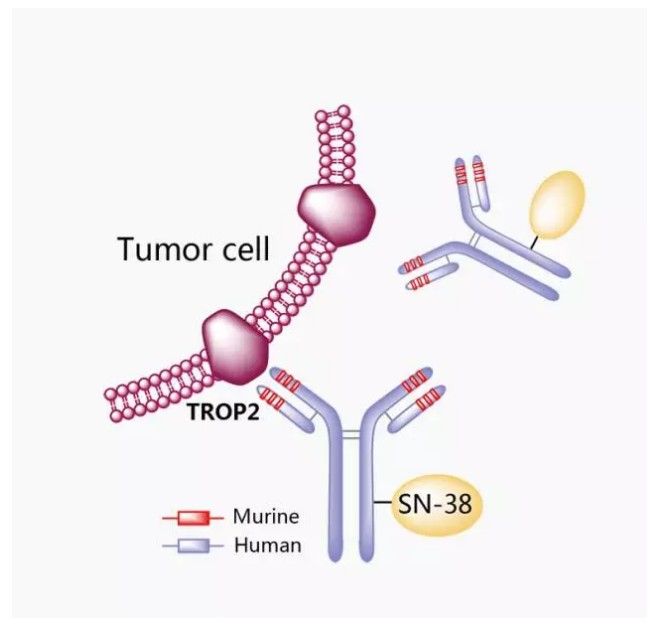
抗体药物偶联物靶向肿瘤细胞
也许对小细胞肺癌的临床数据并不是太好。但是,这已经比2007年FDA批准用于小细胞肺癌治疗的拓扑替康临床数据要好,而且拓扑替康之后再无用于小细胞肺癌的新药上市。同时这已经接近我们之前写过的另一家公司Stemcentrx正在研发的抗体药物偶联物Rova-T对小细胞肺癌的二期临床数据。而且正是Rova-T一次性给Stemcentrx带来了58亿美元的资金。所以Seattle Genetics的这次豪赌还是很有机会的。

每8位妇女中就有一人会患乳腺癌
实际上乳腺癌是目前是全世界导致妇女死亡的第一大癌症,尽管在过去几十年里对乳腺癌患者的健康管理取得了很大的进步,乳腺癌仍具有很高的死亡率,仅2012年就有521900人死于乳腺癌。而三阴性乳腺癌(Triple-Negative Breast Cancer)则是乳腺癌中,复发率最高,最容易转移,致死率最高的也是最难治的一种癌症,占所有乳腺癌的15%-20%(3)。
三阴性乳腺癌,即乳腺癌患者缺乏孕激素受体,孕激素受体以及人类表皮因子生长受体2这三种受体。与普通乳腺癌相比三阴性乳腺癌更具危险性(4)。
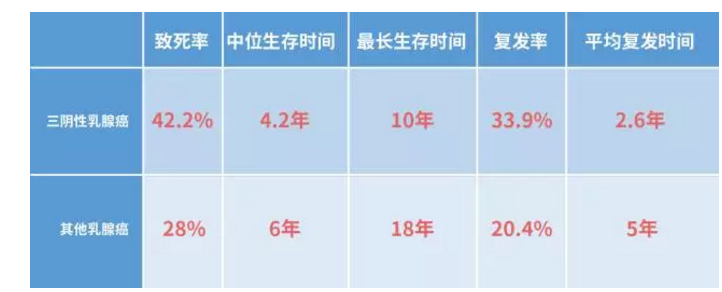
三阴性乳腺癌与普通乳腺癌特征对比
同时小细胞肺癌也是肺癌中最难治的一种,发病率占所有肺癌15%左右,导致的死亡占到所有肺癌的25%以上,一旦确诊,5年存活率小于5%(5)。而且小细胞肺癌已经近40年没有新的疗法出现了,所有的靶向药物都没有取得成功(6)。目前治疗复发性小细胞肺癌的药物,近年来上市的只有GSK在2007年获得FDA批准的化学药物拓扑替康。
拓扑替康注射剂
IMMU-132在对这两种临床最难治的恶性肿瘤的二期临床实验中取得的突破性进展无疑是Seattle Genetics看好IMMU-132并花20亿美元买下它的根本原因,那么sacituzumab govitecan (IMMU- 132)为什么这么厉害呢?连PD-1抑制剂都搞不定的三阴性乳腺癌患者,无药可用的晚期小细胞肺癌患者,它都能能搞定。
其实sacituzumab govitecan (IMMU- 132)就是一个普通的抗体加化疗药物结合的偶联物,由人源化的RS7抗体和细胞毒性药物SN-38组成。SN-38是常用的肿瘤化疗药物伊立替康(CPT-11)在体内的活性代谢物,是一种DNA拓扑异构酶1的抑制剂,让癌细胞这种增殖比较快的细胞不能进行DNA复制从而抑制癌细胞增殖。但是人体本身也有很多的细胞处于不断的增殖过程中,例如骨髓造血干细胞,小肠黏膜上皮细胞等。因此它也会抑制正常的细胞,会对人体造成重大的损伤甚至致死,这限制了其高剂量的使用。 低浓度CPT-11会杀伤少量癌细胞,但肿瘤细胞也有自己的修复机制,修复受损的癌细胞,从而逆转CPT-11对癌细胞的抑制,因此CPT-11对许多癌症患者效果有限。
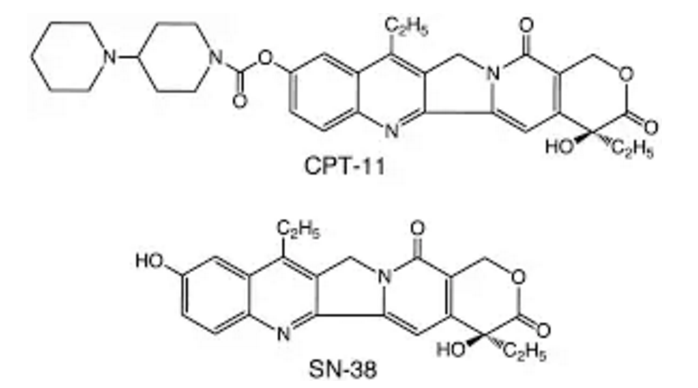
伊立替康和SN-38的结构
但是当SN-38和人源化的RS7抗体合作之后,就大不一样了。人源化的RS7抗体就像导弹的制导装置,牵着SN-38往TROP-2受体上面跑,而且TROP-2受体主要表达在癌细胞上,人体正常组织很少表达,例如三阴性乳腺癌患者的TROP-2受体表达率高达90%。因此SN-38大量聚集在肿瘤组织,抑制癌细胞的增殖,还不会伤害机体的健康组织。即使癌细胞有自我修复机制,但是高剂量的SN-38轮番轰炸让癌细胞根本忙不过来(7)。
由于TROP-2受体在其他许多癌症例如实体瘤等其他癌症中也大量表达。因此sacituzumab govitecan (IMMU- 132)对其他许多癌症也有一定效果,并在进行临床实验中。
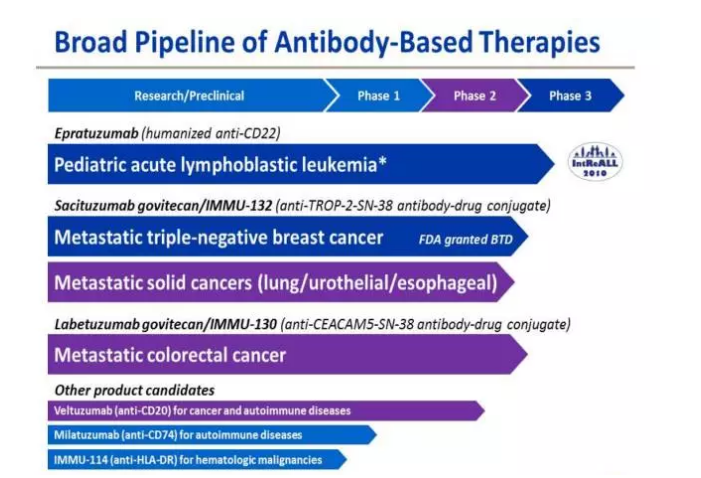
IMMU-132的临床研究进展
在Seattle Genetics 财大气粗的环境下,sacituzumab govitecan (IMMU- 132)上市进程也会加快,预计将在一年之内上市。这也为大量三阴性乳腺癌患者以及小细胞肺癌患者带来新的治疗希望。
参考文献:
1. Bardia A, Mayer I A, Diamond J R, et al. Efficacy and Safety of Anti-Trop-2 Antibody Drug Conjugate Sacituzumab Govitecan (IMMU-132) in Heavily Pretreated Patients With Metastatic Triple-Negative Breast Cancer[J]. Journal of Clinical Oncology, 2017: JCO. 2016.70. 8297.
2. Jhanelle E. Gray, Rebecca S. Heist,et al. Phase 2 study of sacituzumab govitecan (IMMU-132), an anti-Trop-2/SN-38 antibody-drug conjugate (ADC), in patients with pretreated metastatic small-cell lung cancer (mSCLC). In: Proceedings of the 107th Annual Meeting of the American Association for Cancer Research; 2017 Apr 1-5; Washington, DC. Philadelphia (PA):AACR; 2017. Abstract CT155.
3. Torre L A, Bray F, Siegel R L, et al. Global cancer statistics, 2012[J]. CA: a cancer journal for clinicians, 2015, 65(2): 87-108.
4. Dent R, Trudeau M, Pritchard K I, et al. Triple-negative breast cancer: clinical features and patterns of recurrence[J]. Clinical cancer research, 2007, 13(15): 4429-4434.
5. Joshi, M., (2013). Small-Cell Lung Cancer: An Update on Targeted Therapies. Impact of Genetic Targets on Cancer Therapy. W. S. El-Deiry. New York, NY, Springer New York: 385-404.
6. Rudin, C. M., (2016). Rovalpituzumab tesirine, a DLL3-targeted antibody-drug conjugate, in recurrent small-cell lung cancer: a first-in-human, first-in-class, open-label, phase 1 study. The Lancet Oncology 18(1): 42-51.
7. Goldenberg D M, Cardillo T M, Govindan S V, et al. Trop-2 is a novel target for solid cancer therapy with sacituzumab govitecan (IMMU-132), an antibody-drug conjugate (ADC)[J]. Oncotarget, 2015, 6(26): 22496.







