为了增强化疗药物的效果,斯坦福大学副教授Heike E. Daldrup-Link实验室的研究人员计划利用金属纳米粒子将化疗药物运输到肿瘤细胞内,他们还给这个方法取了很有内涵的名字,「特洛伊木马」。

Heike E. Daldrup-Link副教授
为了提高研究效率,Daldrup-Link选择了ferumoxytol(纳米氧化铁)作为化疗药物载体,ferumoxytol已经被FDA批准用于治疗成年人缺铁性贫血。
为了验证设想,研究人员做了三组对照试验:一组小鼠注射「特洛伊木马」,一组小鼠注射没有装载化疗药物的金属纳米粒子,最后一组小鼠注射溶剂。就在研究人员对「特洛伊木马」的疗效充满期待的时候,意外出现了:只注射金属纳米粒子的小组肿瘤抑制效果最好。
「在大部分的研究中金属纳米粒子都是被当做运输药物的工具或者放疗的造影剂,」Daldrup-Link说,「金属纳米粒子本身的抗癌作用被掩盖,除非我们单独观察它的作用。」
是金属纳米粒子本身就可以毒杀肿瘤细胞吗?他们将金属纳米粒子加到体外培养的癌细胞中,发现癌细胞的死亡率并没有显著变化。这就意味着金属纳米粒子抑制肿瘤生长是个间接过程。那么金属纳米粒子究竟是如何起作用的,它激活了人体的哪个「机关」?
在查阅了大量的研究文献之后,Daldrup-Link发现,纳米金属粒子可以吸引肺泡巨噬细胞(1)。经过体外和体内的大量研究,Daldrup-Link证明,的确是金属纳米粒子激活了巨噬细胞,促进巨噬细胞攻击癌细胞,最终表现出抑癌效果。这一重要研究成果9月底刊登在著名期刊《自然纳米科技》上(2)。
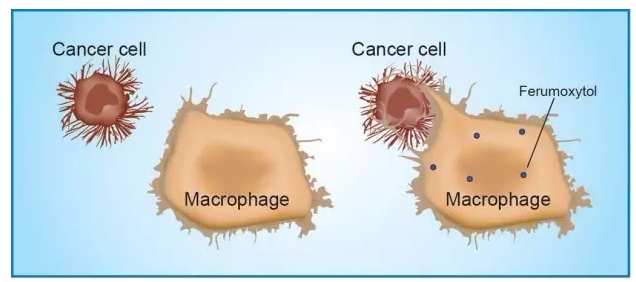
体内有金属纳米粒子ferumoxytol之后,巨噬细胞攻击癌细胞
「这个研究结果实在是太让我们意外了,金属纳米粒子居然促进巨噬细胞攻击癌细胞。」Daldrup-Link说。
很早之前科学家就发现,肿瘤中的巨噬细胞不仅阻止T细胞等攻击肿瘤细胞,还会分泌生长因子滋养肿瘤细胞,促进肿瘤血管的生成,导致癌细胞转移扩散(3)。另外,在今年3月16日,加州大学旧金山分校Matthew F. Krummel的研究团队在《自然》杂志上在线发表了一项骇人的研究成果(4):在血管中吞下癌细胞碎片的巨噬细胞会被癌细胞碎片控制,变成任由癌细胞碎片摆布的「僵尸」,「僵尸」巨噬细胞会离开毛细血管,进入肺组织深处,为后续癌细胞的转移创造有利的生存条件。
由此看来,Daldrup-Link的研究的确让人兴奋。毕竟一直以来,研究人员都把巨噬细胞当做肿瘤生长和转移的「帮凶」。没想到已经被FDA批准的治疗贫血的药物可以用来激活巨噬细胞,治疗癌症。
为了进一步验证金属纳米粒子的抑癌效果,研究人员在乳腺癌模式小鼠和非小细胞肺癌模式小鼠身上做了深入的研究。在乳腺癌小鼠模型实验中,研究人员使用FDA批准用于治疗缺铁性贫血的剂量,可以有效的抑制肿瘤的生长,而且每次用药的有效性可以持续三周。在非小细胞肺癌的转移实验中,使用ferumoxytol的小鼠,转移灶数量显著降低。
Daldrup-Link认为,从小鼠实验结果来看,ferumoxytol在临床的应用非常广泛。对于手术治疗的患者而言,为了扑灭体内剩余的癌细胞,一般需要化疗;然而化疗有一定的副作用,因此患者一般需要等到身体恢复到一定的程度之后,才能接受化疗。没有副作用的金属纳米粒子很好的规避了这个问题。
尽管目前Daldrup-Link的研究都是在模式小鼠身上完成的,但是由于ferumoxytol是FDA已经批准的药物,因此ferumoxytol治疗癌症的临床试验可以快速进入临床研究。Daldrup-Link也表示,「我们认为,我们的这一发现同样适用于人类。」
巨噬细胞作为人体非特异性免疫的一员,由于其与肿瘤关系「暧昧」,研究人员一直没有将其作为免疫治疗的重点研究对象。Daldrup-Link的研究,将巨噬细胞拖回正轨,为免疫治疗又贡献了一份力量。
巨噬细胞
「免疫肿瘤学的关注焦点基本都集中在T细胞身上,」成立于2015年的肿瘤免疫治疗公司Forty Seven的首席商务官Craig Gibbs在接受《自然》杂志采访时表示(5),在一些肿瘤中,巨噬细胞占到了肿瘤总重量的一半。「巨噬细胞含量越高的肿瘤预后越差,这就说明巨噬细胞在肿瘤的发生和发展中起到非常重要的作用。」
T细胞和巨噬细胞分属两个不同的免疫体系。T细胞是特异性免疫系统的代表,免疫效果强烈,且特异性强。近年来给人们治愈癌症带来信心的CTLA4抗体,PD-1/PD-L1抗体,以及CAR-T和TCR-T,都是依赖于T细胞。而以巨噬细胞为代表的非特异性免疫系统虽然覆盖面广,但是特异性差,且相对温和。
虽然基于T细胞的免疫治疗取得了不错的成绩,但是由于T细胞自身特点的限制,CAR-T在实体瘤上表现乏力,用于治疗实体瘤的PD-1/PD-L1抗体大部分患者都不响应,这些也是医学界不得不面对的事实。免疫治疗领域急需新的发展方向。巨噬细胞的研究进展,给免疫治疗打开了另一扇窗。这也是Daldrup-Link等的研究受到广泛关注的原因。
当然,Daldrup-Link教授在巨噬细胞上的研究进展只是近来「巨噬细胞热」的一个方面。
近年来,巨噬细胞与肿瘤关系「暧昧」的原因逐渐清晰,研究人员也开始思考如何根据这种「暧昧」的关系设计新的抗体药物。
斯坦福大学Irving L. Weissman教授在2009年一期《细胞》杂志上背对背刊登了两篇文章(6; 7),揭示了巨噬细胞「帮助」肿瘤细胞生长的背后原因。6年之后,Weissman教授又揭示了巨噬细胞决定是否吞噬肿瘤细胞的关键机制(8; 9)。研究人员的不懈努力,让巨噬细胞得以「沉冤昭雪」,成为免疫治疗领域的又一员悍将。在基于T细胞的免疫治疗开始疲软的现状下,资本也将目光投向了基于巨噬细胞的免疫治疗。
今年2月24日,成立于2015年的肿瘤免疫治疗公司Forty Seven获得Google等领投的7500万美元A轮融资;半年后成立于2006年的另一家肿瘤免疫治疗公司Tioma Therapeutics,经历10年的默默无闻,获得GSK和Roche等领投的8600万美元A轮融资。这两家公司均专注于巨噬细胞抗体药物免疫治疗的研究,并且已经从合作的高校获取药物研发的专利权。
另一个制药巨头Celgene也在开展巨噬细胞免疫治疗研究,它的抗体药物CC-90002在动物实验中表现出色,对所有的肿瘤类型都有效果。据统计,目前至少有三个抗体药物进入临床试验。
相较于Forty Seven等公司开发的免疫抑制剂,Daldrup-Link教授发现的金属纳米粒子,具有副作用极小,且已经获批用于人体等优势。或许Daldrup-Link教授的研究成果会更快的转化到临床应用中。
相关资料:
【1】Warheit DB, Hartsky MA. 1993. Role of alveolar macrophage chemotaxis and phagocytosis in pulmonary clearance responses to inhaled particles: Comparisons among rodent species. Microscopy Research and Technique 26:412-22
【2】Zanganeh S, Hutter G, Spitler R, Lenkov O, Mahmoudi M, et al. 2016. Iron oxide nanoparticles inhibit tumour growth by inducing pro-inflammatory macrophage polarization in tumour tissues. Nat Nano advance online publication
【3】Biswas SK, Mantovani A. 2010. Macrophage plasticity and interaction with lymphocyte subsets: cancer as a paradigm. Nat Immunol 11:889-96
【4】Headley MB, Bins A, Nip A, Roberts EW, Looney MR, et al. 2016. Visualization of immediate immune responses to pioneer metastatic cells in the lung. Nature 531:513-7
【5】Morrison C. 2016. Immuno-oncologists eye up macrophage targets. Nat Rev Drug Discov 15:373-4
【6】Jaiswal S, Jamieson CHM, Pang WW, Park CY, Chao MP, et al. 2009. CD47 Is Upregulated on Circulating Hematopoietic Stem Cells and Leukemia Cells to Avoid Phagocytosis. Cell 138:271-85
【7】Majeti R, Chao MP, Alizadeh AA, Pang WW, Jaiswal S, et al. 2009. CD47 Is an Adverse Prognostic Factor and Therapeutic Antibody Target on Human Acute Myeloid Leukemia Stem Cells. Cell 138:286-99
【8】Feng M, Chen JY, Weissman-Tsukamoto R, Volkmer J-P, Ho PY, et al. 2015. Macrophages eat cancer cells using their own calreticulin as a guide: Roles of TLR and Btk. Proceedings of the National Academy of Sciences 112:2145-50
【9】Vonderheide RH. 2015. CD47 blockade as another immune checkpoint therapy for cancer. Nat Med 21:1122-3







