在CRISPR诞生之前,“基因编辑”一词仅存在于科研人员的世界里;在CRISPR诞生之后,“编辑生命”似乎变得触手可及,于是才会有今天人尽皆知的局面。近期临床和实验室的研究进展再次表明,基因编辑斗得过癌症和艾滋,还要去治疗失明。
基因编辑这种“上得了厅堂,下得了厨房”的能力,依赖于于它强大而稳定的“关闭”、“恢复”和“切换”三大技能。
“关闭”一个基因,打开生命之门
2015年11月5日,Waseem Qasim对外宣布,他们利用Cellectis公司经ZFNs基因编辑技术改造的UCART19细胞株,成功缓解了Layla的不治之症–急性淋巴细胞性白血病(ALL)。
NBCNEWS的报道
急性淋巴细胞性白血病的主要特征为,免疫淋巴细胞在骨髓内异常增生,导致人体造血功能紊乱,以及大量器官被侵犯。一般情况下,可以通过放化疗以及骨髓移植,有效的杀死异常增殖的免疫淋巴细胞,最终达到缓解或者治愈的目的。据统计,Layla这个年龄(1岁左右)患上急性淋巴细胞性白血病的治愈率为25%,但是Layla显然属于那不幸的75%,她在接受放化疗以及骨髓移植之后,病情仍旧没有得到缓解。Layla显然被传统的治疗手段“抛弃”了。就在这种情形下,Layla的父母决定让Layla尝试基因编辑疗法,尽管这种治疗急性淋巴细胞性白血病的方法只在小白鼠身上用过。
幸运的是Layla最终转危为安。因此才有了前几天“基因编辑技术成功治愈白血病女孩”的文章席卷朋友圈。但是,Cellectis公司的Qasim却谨慎地说,“对白血病患者来说,这种治疗方法并不是长久之计,实际上它(基因编辑)更像是‘缓兵之计’,在找到合适的配型之前,这种方法起到‘桥梁’的作用”。
Qasim在言辞间分明在告诉我们,“缓解Layla病情的不止基因编辑”。还有传说中的CAR-T技术(Chimeric Antigen Receptor T-Cell Immunotherapy,嵌合抗原受体T细胞免疫疗法)。
Cellectis公司基于ZFNs基因编辑的CAR-T技术
Layla的医生发现,在异常增殖的免疫淋巴细胞表面有CD19蛋白,这个蛋白可以被CAR19蛋白识别,但是没能找到携带CAR19蛋白的合适供体。最终,Layla的医生跟Qasim取得联系,Qasim开发的UCART19细胞(有CAR19蛋白)成为Layla唯一的希望。UCART19细胞尽管具备杀灭Layla体内恶性细胞的能力,但是也不是Layla合适的配型。
UCART19细胞的厉害之处在于,Qasim利用ZFNs基因编辑技术“关闭”了导致排异反应的关键基因,这样一来UCART19就可以安全输入Layla体内。让人感到惊喜的是,UCART19将Layla体内恶性增殖细胞消灭干净了。至此UCART19的任务全部完成,Layla已经完成了新一轮的骨髓移植(此时有没有CAR19蛋白已经不重要了)。目前看来Layla已经“痊愈”了,但只有经过一两年时间的考验之后,我才敢去掉那个引号。
“恢复”受损基因,才能重见光明
2015年11月3日,Katrine Bosley在剑桥大学召开的EmTech大会上宣布,实验室数据表明,CRISPR基因编辑技术可以用于治疗Leber congenital amaurosis(LCA;利伯先天性黑朦病,一种遗传性视力衰退疾病),Editas将在2017年开展CRISPR基因编辑人体实验。

相比于ZFNs基因编辑技术“治愈”了Layla的白血病,可能会发生于2017年的CRISPR基因编辑人体实验显得暗淡无光。但我却为Editas的CRISPR基因编辑技术感到心潮澎湃。我们先来看看Editas是打算如何做的。
LCA是一种罕见遗传病,研究表明有20多种基因变异会导致LCA,例如RPE65和CEP290等。传统的基因治疗十分热衷于研究LCA,因为这些变异与LCA关系明确,直接通过病毒载体导入正常基因(比如正常的RPE65)即可。但是,一旦遇到跟病毒载体一样大的基因(比如CEP290)缺陷,传统的基因治疗就束手无策了。
在所有的LCA病例中,CEP290基因缺陷导致的LCA大概占20%,Editas采用的方法是,利用CRISPR基因编辑技术,直接删除CEP290基因变异位点左右共1000个碱基。Editas实验室的研究表明,删除CEP290基因的那1000个碱基之后,CEP290基因的表达恢复正常。CEP290基因变异的患者视力可能恢复正常。
Katrine Bosley详解CRISPR基因编辑技术治疗LCA过程
Editas宣布的2017年人体实验激动人心之处在于,这有可能是首次人体(in vivo)基因编辑试验。这项研究成功的意义在于,将CRISPR基因编辑“工具”装载到病毒体内,再把病毒注射到患处,CRISPR可以自行对患病部位进行基因改造。那么以后治疗Layla那样的白血病,不用分离T细胞了,直接将改造好的病毒注射到骨髓,就直接将基因异常的骨髓修复了,或者是直接整合目标基因加强其战斗力。这样一来,很多大手术就会变成微创手术,带来的好处是难以估量的。
在不同人种之间,自由“切换”
2014年3月12日,宾夕法尼亚大学Pablo Tebas教授团队在新英格兰医学杂志撰文称,他们利用Sangamo BioSciences开发的ZFNs基因编辑技术,显著提高了艾滋病患者对艾滋病毒的抵抗能力。
这篇发表于2014年的文章,研究从2009年就开始了,直到2012年才结束。是基因编辑技术首次应用于临床。目前Sangamo BioSciences基于ZFNs技术治疗艾滋病的方法已经进入临床II期试验。
之所以能够使用基因编辑技术治疗艾滋病,是因为发现免疫细胞表面的CCR5蛋白是HIV进入免疫细胞的“入口”。而少数北欧人由于CCR5基因“变异”,具备天然的HIV抵抗力(为什么是他们?)。
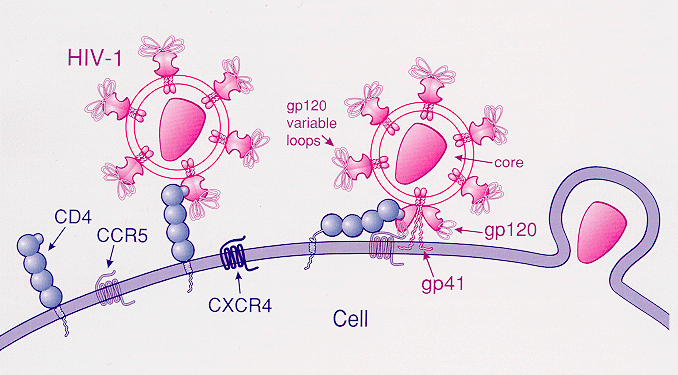
HIV在细胞表面的“入口”CCR5蛋白
这个“变异”对于艾滋病患者来说真的很重要,因此研究人员做了很多的研究。有研究表明,北欧人体内的CCR5基因“变异”不是CCR5基因突变的结果,而是在自然界中伴随着原始高加索人种的出现而出现的,这种“变异”所表现出来的性状因适应自然环境而保留了下来。自此,我不得不佩服大自然的神奇。也许在世界的任何一个角落里,造物主都会安放着一个保护人类的重要基因,避免人类因一种疾病的爆发而灭绝。
有了造物主释放的重要信息,研究人员就动脑子了,“要不把患者的CCR5基因都改成高加索人种那种类型吧”!Tebas团队做的就是这件事。在体外(ex vivo)利用ZFNs基因编辑技术定点改造免疫细胞的CCR5基因。让我们静候Sangamo临床II期的好消息。
纵观上述三项研究,你会发现我一直在强调一个事情:体外(ex vivo)和体内(in vivo)。体外基因编辑就是在实验室里修改目标细胞的基因信息,即使效率低下,仍旧可以通过大量的实验筛选出改造成功的细胞,接下来只需要扩大培养,在输入体内即可。而体内编辑是整个编辑的过程在体内进行,这就编辑过程是高效的;另外,携带编辑工具的病毒载体一旦注入人体,控制性就变差了,因此对编辑过程的安全性要求非常高。但是正如我在讲述CRISPR基因编辑技术所言,一旦能过做到精确高效的编辑,以后很多疾病的治疗都变得非常简单了。
尽管老牌的ZFNs基因编辑技术已经在癌症和艾滋病的治疗上崭露头角,但是ZFNs能做的事情,对CRISPR来讲是“小菜一碟”。今年Editas已经与CAR-T新贵Juno开展合作,相信他们很快会在免疫治疗领域取得大突破。体内(in vivo)基因编辑应该才是Editas们的终极梦想。







