刚刚结束的第59届美国临床肿瘤学会(ASCO)年会以及第28届欧洲血液学会(EHA)年会上,来自罗特西普的COMMANDS研究结果以重磅之姿呈现,继BELIEVE研究证实β-地中海贫血患者获益于罗特西普治疗后,再次证实较低危骨髓增生异常肿瘤(即,骨髓增生异常综合征,简称MDS)患者亦可获益于罗特西普一线治疗,使得治疗需求一直未能得到满足的较低危MDS患者有了新的治疗选择。【肿瘤资讯】特别采访了浙江大学附属第一医院血液科执行主任佟红艳教授,请她详细介绍COMMANDS研究以及该研究展示出的罗特西普一线治疗较低危MDS的优势,同时分析了罗特西普对未来临床实践可能产生的影响。

浙江大学医学院附属第一医院血液科执行主任,骨髓增生异常综合征中心主任,淋巴瘤中心主任
浙江省血液病医学临床研究中心副主任
浙江大学医学院诊断教研室主任
浙江省卫生领军人才
浙江省高层次创新人才
浙江省新世纪151人才
浙江省杰出青年人才项目获得者
英国Royal Free Hospital 高级访问学者
社会兼职:
中华医学会血液学分会红细胞学组委员
中国女医师协会临床肿瘤血液淋巴专业委员会常务委员及MDS/MPN学组组长
中国抗癌协会血液肿瘤专业委员会MDS/MPN工作组副组长
中国老年医学会血液分会常务委员及MDS工作委员会副主任委员
浙江省医师协会血液科医师分会委员会MDS/MPN学组组长
浙江省抗癌协会血液淋巴专业委员会副主任委员
浙江省医学会临床试验与伦理分会副主任委员
浙江省医学会血液学分会副主任委员
主持国家自然科学基金面上项目5项,省部级重点项目、省杰青项目等7项;以第一或通讯作者发表在Haematologica,European Journal of Cancer,J Infect等SCI期刊50余篇;以第一完成人获省科技进步二等奖2项,主参国家科技进步二等奖1项、省科技进步一、二等奖6项。
横空出世 填补未满足的临床需求
MDS是造血干细胞的克隆性疾病。中国MDS的发病率约为1.5/10万[1],其中77%[2,3]属于较低危类型。佟红艳教授表示,较低危MDS患者的主要临床表现是慢性贫血,输血依赖是这类患者面临的最严峻问题,因为相较于非输血依赖患者,其合并症(心血管事件、呼吸困难、感染等)发生率更高,死亡风险增加超过50%,心血管疾病是主要死亡原因[4-7]。
较低危MDS患者的治疗目标[8-10]是减少输血依赖,提升生活质量,改善生存并延迟向急性髓系白血病转化。红细胞生成刺激剂(ESA)是目前较为公认的治疗较低危MDS贫血的标准一线药物,但其疗效和持续时间有限,仅三分之一患者存在治疗应答,且中位应答持续时间仅6-18个月[11-13]。
佟红艳教授认为,ESA治疗无效患者的进一步治疗选择极为有限,长期输血并祛铁治疗虽然可部分解决这一难题,但血源紧张导致无法按需输血,输血增加感染风险等问题导致患者依从性差,这些无法彻底解决的问题,导致贫血纠正不理想,进而严重影响患者生活质量与预后[10,14],因此亟需更有效且疗效更持久的治疗药物以改善目前窘境。罗特西普的问世以及COMMANDS研究结果[15,16]的公布,无疑为较低危MDS患者的贫血治疗提供了新的武器。
COMMANDS研究证实罗特西普高效持久,普适安全
COMMANDS研究是一项开放标签、随机III期研究,纳入的是输血依赖且未接受过ESA治疗的IRSS-R定义的极低危、低危及中危MDS患者,旨在比较罗特西普和ESA促红素治疗的疗效和安全性。研究的主要终点是前24周内,摆脱红细胞输注(RBC-TI)≥12周同时平均血红蛋白(Hb)增加≥1.5 g/dL的患者比例;关键次要终点包括前24周内获得血液学改善-红系应答(HI-E)≥8周、RBC-TI 24周和RBC-TI≥12周的患者比例。
减少输血依赖,提升血红蛋白,疗效有力
COMMANDS研究[15]中罗特西普组可评估患者147例,促红素组可评估患者154例,中位治疗持续时间分别为41.6周和27周。治疗的前24周内,罗特西普和促红素组分别有86例(58.5%)和48例(31.2%)患者达到主要终点,即RBC-TI≥12周同时平均Hb增加≥1.5g/dL(P<0.0001)。
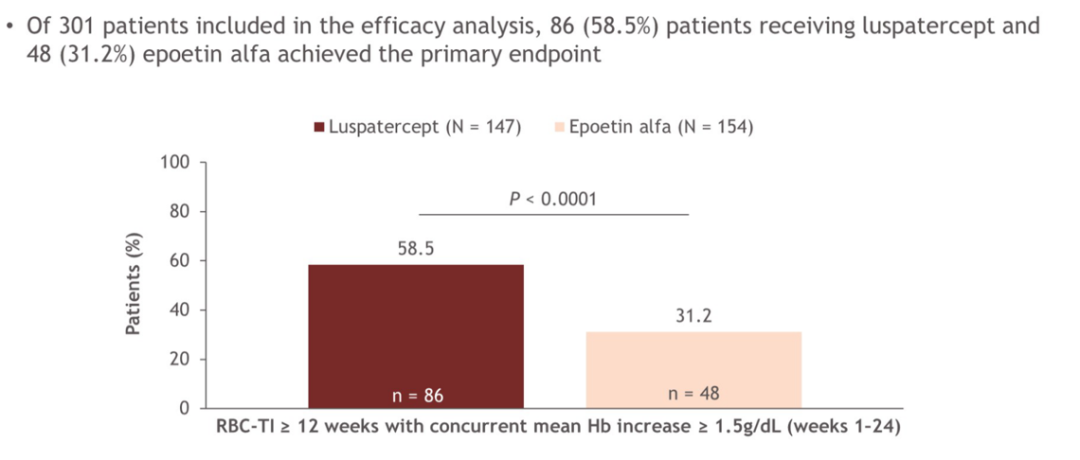
佟红艳教授对这一结果给予了高度肯定,因为罗特西普治疗组减少输血依赖且平均Hb增加≥1.5g/dL的患者比例几乎是促红素组的2倍,充分体现了罗特西普治疗较低危MDS贫血的良好疗效。更难能可贵的是,COMMANDS研究[15]的主要终点为复合终点,Hb增加≥1.5g/dL这一标准使得RBC-TI≥12周的结果更为客观,显著增加了可信度,因为血红蛋白水平能更可靠的实时反映治疗结果,而输血依赖则受较多客观因素影响,如个体对贫血耐受性、输血可及性等。
摆脱输血依赖,改善红系反应,疗效持久
COMMANDS研究[15]的次要终点分析显示,罗特西普和促红素组前24周内RBC-TI 24周的患者分别为70例(47.6%)和45例(29.2%)(P = 0.0006),RBC-TI≥12周的患者分别为98例(66.7%)和71例(46.1%)(P = 0.0002),HI-E ≥ 8周的患者分别为109例(74.1%)和79 例(51.3%)(P< 0.0001),尤其突出的是罗特西普组RBC-TI≥12周患者的中位应答持续时间为126.6周,而促红素组仅为77周。
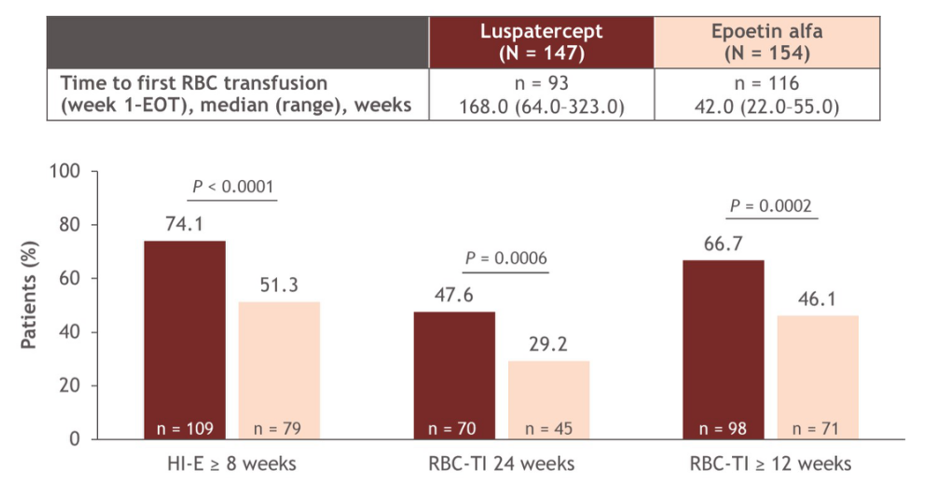
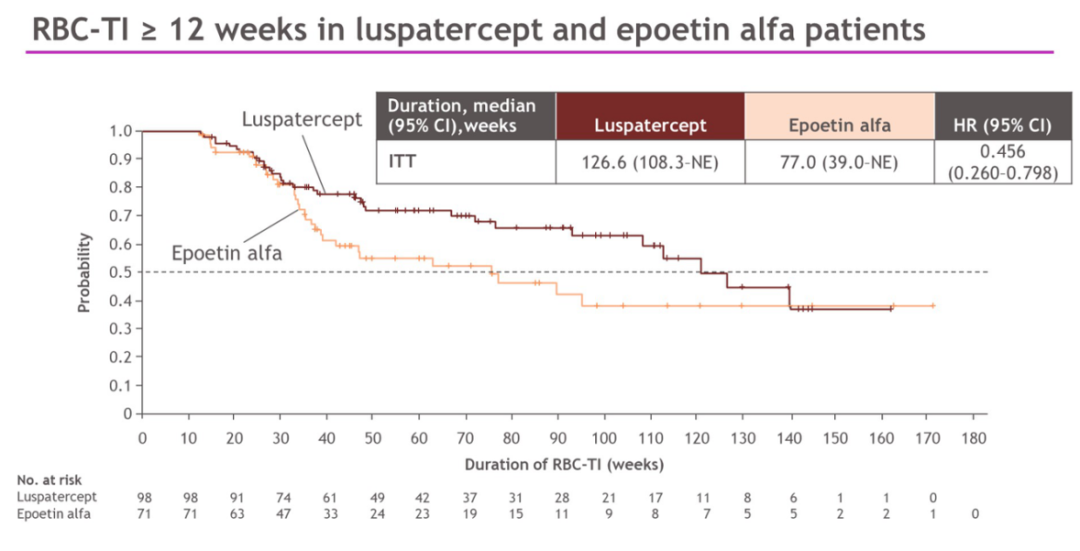
佟红艳教授说,II期PACE-MDS研究[17]就已发现,罗特西普能够有效治疗较低危MDS的贫血,而COMMANDS研究则进一步证实,不但更多的较低危MDS贫血患者可以获益于罗特西普治疗,而且中位治疗应答持续时间长达2年半,远远超过了目前标准一线治疗促红素的中位应答持续时间的1年半,这对于减轻输血带来的各种负担,持续改善患者生活质量具有非常积极的意义。
无论突变类型,罗特西普获益可能性更高
COMMANDS研究[15,16]的进一步分析还显示,无论基线促红素水平、基线输血负荷大小,罗特西普治疗均有更高获益可能。且对于SF3B1、ASXL1、TET2、DNMT3A等常见的MDS基因突变,罗特西普治疗结果均优于促红素,临床获益的可能性更高。
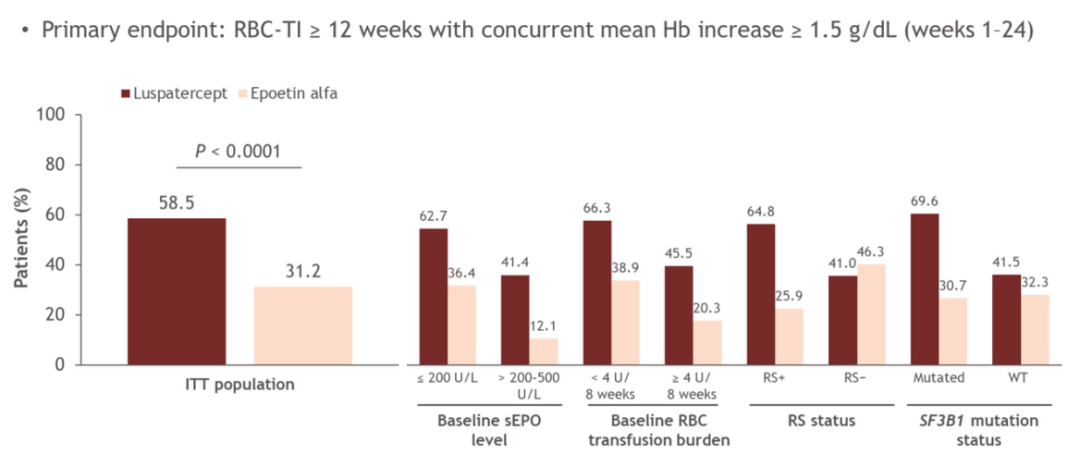
佟红艳教授表示,继MEDALIST研究[18]证实伴环状铁粒幼红细胞的MDS(MDS-RS)患者获益于罗特西普治疗后,COMMANDS研究[15,16]更进一步证实,较低危MDS接受罗特西普治疗的获益优于促红素,包括临床相关亚组。这是一个令人鼓舞的结果,意味着罗特西普的适用人群非常广泛,能使更多较低危MDS贫血患者获益,提升生活质量,改善预后。
安全性良好,与既往一致
截至COMMANDS研究数据分析时,罗特西普中位治疗持续时间41.6周,未出现新的安全性信号,临床相关各亚组显示出一致的安全性特征。罗特西普和促红素治疗组的贫血、血小板减少和中性粒细胞减少发生率分别为9.6%(17)和9.7%(17)、6.2%(11)和1.7%(3)、5.1%(9)和7.4%(13),疲劳、腹泻和外周水肿发生率分别为14.6%(26)和6.8%(12)、14.6%(26)和11.4%(20)、12.9%(23)和6.8%(12)。
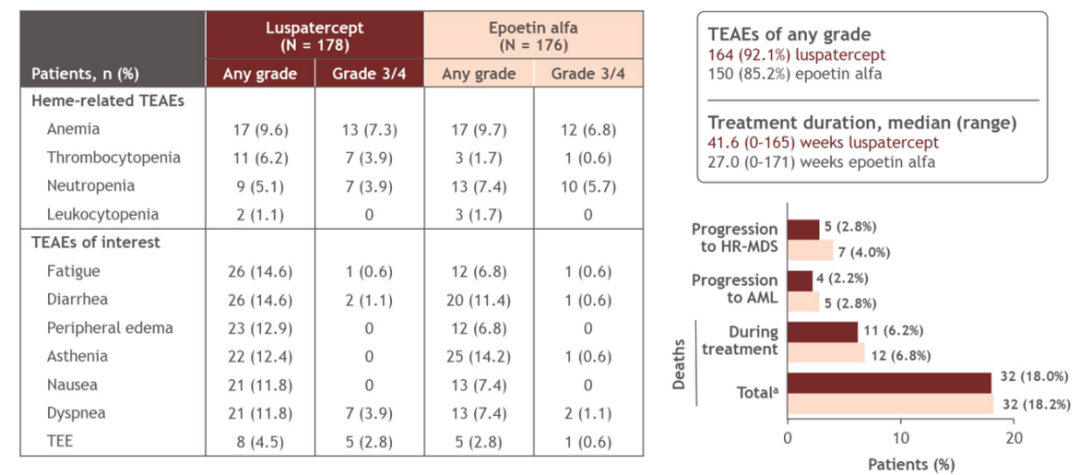
佟红艳教授认为,药物评价应包括两方面内容,第一是疗效,第二是安全性与耐受性。COMMANDS研究[15,16]不但显示了罗特西普的良好疗效,同时也再次验证了既往研究中体现出来的良好安全性,不良事件发生率与促红素持平,未出现新的安全性事件。临床实践中罗特西普相关不良事件发生率与临床研究中类似,且均能较好处理。
改变临床实践,期待惠及更多患者
佟红艳教授对未来罗特西普适用范围的扩展报以极大信心,她认为COMMANDS研究最重要的意义在于通过罗特西普与促红素头对头研究,明确了罗特西普治疗较低危MDS贫血显著优于促红素,为罗特西普进入一线治疗提供了有力证据,为临床实践增添了信心,罗特西普有望以其更有效、更持久的疗效和良好的安全性改变现有标准治疗。
目前,罗特西普的补充生物制品许可申请正在接受美国食品药品监督管理局的优先审评,用于治疗可能需要红细胞输注且未接受过ESA治疗的极低危至中危MDS成人患者的贫血。目前罗特西普在中国获批的适应症是β-地中海贫血,期待能早日在中国获批治疗较低危MDS的适应证,造福中国患者。
1. Wang W, Wang H, Wang XQ, Lin GW. First report of incidence of adult myelodysplastic syndrome in China. Ann Hematol. 2012;91(8):1321-1322. doi:10.1007/s00277-011-1389-7
2.Greenberg PL, Tuechler H, Schanz J, et al. Revised international prognostic scoring system for myelodysplastic syndromes. Blood. 2012;120(12):2454-2465. doi:10.1182/blood-2012-03-420489
3.Henry DH, Glaspy J, Harrup R, et al. Roxadustat for the treatment of anemia in patients with lower-risk myelodysplastic syndrome: Open-label, dose-selection, lead-in stage of a phase 3 study. Am J Hematol. 2022;97(2):174-184. doi:10.1002/ajh.26397
4.Sekeres MA, Taylor J. Diagnosis and Treatment of Myelodysplastic Syndromes: A Review. JAMA. 2022;328(9):872-880. doi:10.1001/jama.2022.14578
5. Malcovati L, Della Porta MG, Strupp C, et al. Impact of the degree of anemia on the outcome of patients with myelodysplastic syndrome and its integration into the WHO classification-based Prognostic Scoring System (WPSS). Haematologica. 2011;96(10):1433-1440. doi:10.3324/haematol.2011.044602
6. Braga Lemos M, Rodrigues SR, Schroeder T, Kulasekararaj AG, Matos JE, Tang D. Association between red blood cell transfusion dependence and burden in patients with myelodysplastic syndromes: A systematic literature review and meta-analysis. Eur J Haematol. 2021;107(1):3-23. doi:10.1111/ejh.13619
7.Goldberg SL, Chen E, Corral M, et al. Incidence and clinical complications of myelodysplastic syndromes among United States Medicare beneficiaries. J Clin Oncol. 2010;28(17):2847-2852. doi:10.1200/JCO.2009.25.2395
8.Garcia-Manero G. Myelodysplastic syndromes: 2015 Update on diagnosis, risk-stratification and management. Am J Hematol. 2015;90(9):831-841. doi:10.1002/ajh.24102
9.Germing U, Oliva EN, Hiwase D, Almeida A. Treatment of Anemia in Transfusion-Dependent and Non-Transfusion-Dependent Lower-Risk MDS: Current and Emerging Strategies. Hemasphere. 2019;3(6):e314. Published 2019 Oct 30. doi:10.1097/HS9.0000000000000314
10.Cogle CR, Reddy SR, Chang E, et al. Early treatment initiation in lower-risk myelodysplastic syndromes produces an earlier and higher rate of transfusion independence. Leuk Res. 2017;60:123-128. doi:10.1016/j.leukres.2017.07.008
11. Platzbecker U, Symeonidis A, Oliva EN, et al. A phase 3 randomized placebo-controlled trial of darbepoetin alfa in patients with anemia and lower-risk myelodysplastic syndromes. Leukemia. 2017;31(9):1944-1950. doi:10.1038/leu.2017.192
12. Fenaux P, Platzbecker U, Ades L. How we manage adults with myelodysplastic syndrome. Br J Haematol. 2020;189(6):1016-1027. doi:10.1111/bjh.16206
13. Fenaux P, Santini V, Spiriti MAA, et al. A phase 3 randomized, placebo-controlled study assessing the efficacy and safety of epoetin-α in anemic patients with low-risk MDS. Leukemia. 2018;32(12):2648-2658. doi:10.1038/s41375-018-0118-9
14.Oliva EN, Platzbecker U, Fenaux P, et al. Targeting health-related quality of life in patients with myelodysplastic syndromes - Current knowledge and lessons to be learned. Blood Rev. 2021;50:100851. doi:10.1016/j.blre.2021.100851
15.Guillermo Garcia-Manero, Uwe Platzbecker, Valeria Santini, et al. Efficacy and safety results from the COMMANDS trial: A phase 3 study evaluating luspatercept vs epoetin alfa in erythropoiesis-stimulating agent (ESA)-naive transfusion-dependent (TD) patients (pts) with lower-risk myelodysplastic syndromes (LR-MDS). Journal of Clinical Oncology. 2023 41:16_suppl, 7003
16.Porta MGD, Platzbecker U, Santini V, et al. LUSPATERCEPT VERSUS EPOETIN ALFA FOR TREATMENT (TX) OF ANEMIA IN ESA-NAIVE LOWER-RISK MYELODYSPLASTIC SYNDROMES (LR-MDS) PATIENTS (PTS) REQUIRING RBC TRANSFUSIONS: DATA FROM THE PHASE 3 COMMANDS STUDY. EHA 2023 Abstract: S102
17.Platzbecker U, Götze KS, Kiewe P, et al. Long-Term Efficacy and Safety of Luspatercept for Anemia Treatment in Patients With Lower-Risk Myelodysplastic Syndromes: The Phase II PACE-MDS Study. J Clin Oncol. 2022;40(33):3800-3807. doi:10.1200/JCO.21.02476
18.Fenaux P, Platzbecker U, Mufti GJ, et al. Luspatercept in Patients with Lower-Risk Myelodysplastic Syndromes. N Engl J Med. 2020;382(2):140-151. doi:10.1056/NEJMoa1908892