摘要:mRNA疫苗技术可用于帮助摧毁癌细胞,十年内人类或许可以打赢癌症攻坚战。在全球mRNA肿瘤疫苗领域,BioNTech和Moderna正在展开激烈竞争。在新冠疫苗需求降温后,两家公司近一年来股价都出现重挫,股价跌幅近50%。12月13日,业界传来重磅消息:制药巨头Merck与Moderna联合研发的个体化癌症mRNA疫苗,在临床上可将晚期黑色素瘤患者术后复发或死亡风险降低44%。当日Moderna股价走高,暴涨超过20%。这是mRNA疫苗首次在随机临床试验当中展现治疗黑色素瘤的效力。
2021年《麻省理工科技评论》“全球十大突破性技术”名单之首即为mRNA疫苗。BioNTech联合创始人Ugur Sahin夫妇曾表示:“mRNA癌症疫苗的上市可能要等到2030年左右。”mRNA新冠疫苗已经证明了通过将遗传基因编码输送至人体,能够让细胞产生抗体,从而激活人体的免疫反应。那么,同样的原理也应该能够在对抗肿瘤方面被验证,通过接种癌症疫苗,人体将能够启动免疫系统,从而攻击肿瘤细胞。
对抗恶性肿瘤最强大的武器是人体免疫系统。然而,癌症通常会“欺骗”我们的免疫系统,但适当的治疗可以“武装/唤醒”我们的免疫系统来抵抗肿瘤。癌症疫苗接种的目的便是激活宿主免疫系统,诱导免疫系统靶向癌细胞,从而摧毁肿瘤细胞。在mRNA肿瘤疫苗领域,BioNTech正在研发针对直肠癌、黑色素瘤和其他癌症的mRNA疗法。Moderna则联手Merck开发并销售一种个性化精准治疗癌症疫苗。这种疫苗基于Moderna的mRNA技术,并与默沙东的明星肿瘤疗法 Keytruda(K药)联用,治疗高危黑色素瘤患者。
联手Merck,Moderna将mRNA技术应用于癌症治疗
Merck与Moderna在2016年建立“战略合作伙伴关系”后,一直在共同进行癌症试验。2022年10月12日,Merck与Moderna签订2.5亿美元合作协议,对个性化癌症疫苗(Personalized Cancer Vaccine,PCV)mRNA-4157/V940进行联合开发和商业化。12月13日,Moderna官网发布公告:个体化癌症疫苗mRNA-4157/V940与PD-1抑制剂Keytruda的组合疗法,在临床2b期试验当中显示,与Keytruda单药治疗相比,可以显著降低III、IV期黑色素瘤患者在肿瘤完全切除后的复发或死亡风险达44%!

图1 Moderna官网公告(图源:Moderna官网)
mRNA-4157/V940癌症疫苗包含编码34种新抗原的单一合成mRNA分子,这些新抗原是根据每位患者肿瘤独特的DNA序列突变特征通过演算法所设计而成。当将此癌症疫苗注射入体内时,这些RNA所携带的新抗原序列会被翻译成蛋白质,并通过体内的抗原呈递,刺激产生T细胞抗肿瘤反应。自获得肿瘤样本至对病患进行治疗,约需花费45天的时间。在该疗法中,每三周注射九剂mRNA-4157/V940疫苗,每三周注射一疗程Keytruda。
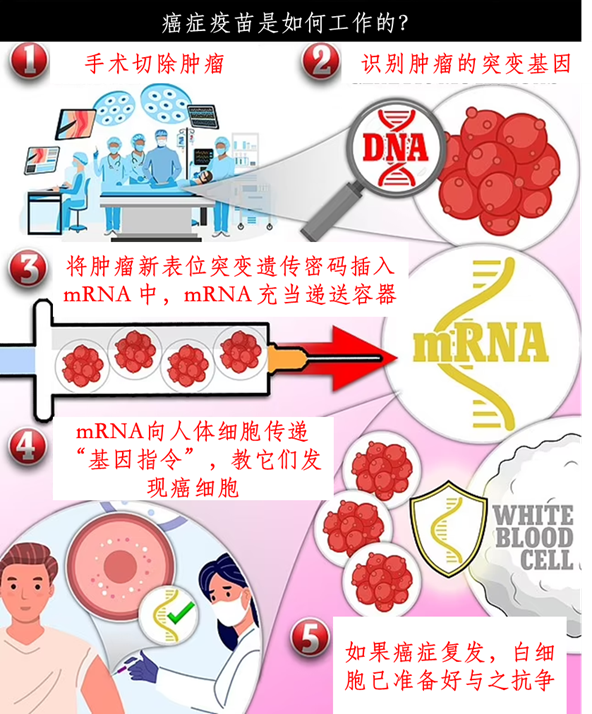
图2 癌症疫苗的作用过程(图源:生物探索编辑团队&[1])
公布的KEYNOTE-942/mRNA-4157-P201试验,是一项开放标签的临床2b期试验,共有157位患者入组。数据分析显示,与Keytruda单药治疗相比,癌症疫苗与Keytruda在III、IV期黑色素瘤患者进行肿瘤完全切除后,可在统计上显著并具临床意义地改善试验主要终点无复发生存期。此组合疗法可降低患者复发或死亡风险达44%(HR:0.56,95% CI:0.31-1.08,单侧P值=0.0266)。安全性方面也与过去试验一致,在组合疗法与Keytruda单药治疗组中所见产生严重治疗相关不良反应比率分别为14.4%与10%。
如果该疗法获得批准,费用可能会非常昂贵。正在试验的类似癌症疫苗每针成本约为10万美元(69.6万人民币)。Moderna称:“这种疫苗与新冠mRNA疫苗使用了相同的技术,因此其安全性已经经过一定程度的验证。此项临床结果是mRNA疫苗应用的巨大进步,将开启mRNA疫苗治疗癌症的新范式。我们计划于明年启动在黑色素瘤患者的临床3期试验,并将此疗法扩展应用至其他肿瘤类型。”
新生抗原癌症疫苗,都是谁在布局?
起初,癌症疫苗并不成功,在看到高度的不良反应和低疗效后,人们对这项技术的热情和兴趣下降。然而,随着测序技术、创新的输送系统、生物信息数据处理技术和疫苗佐剂的发展,癌症疫苗有越来越突出的机会深入到市场中。2021年,癌症疫苗的市场规模估计为107.2亿美元,2022年已达到164.7亿美元。癌症疫苗已开始形成一个独立的产业分支。目前,癌症疫苗的研发主要有五种平台:新生抗原平台、溶瘤病毒平台、肿瘤相关抗原平台、抗原精华平台和全细胞平台。
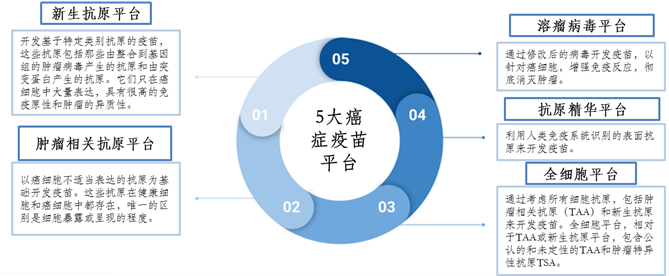
图3 5大癌症疫苗平台(图源:生物探索编辑团队&[2])
Moderna所应用的便是癌症疫苗新生抗原平台。新生抗原是基于特定类别抗原的疫苗,包括整合到基因组中的肿瘤病毒产生的抗原和突变蛋白产生的抗原。这些抗原仅在癌细胞中大量表达,具有高免疫原性和肿瘤异质性。目前,已经发现了相当数量的新生抗原,它们是肿瘤细胞所特有的,不受免疫耐受机制的影响。
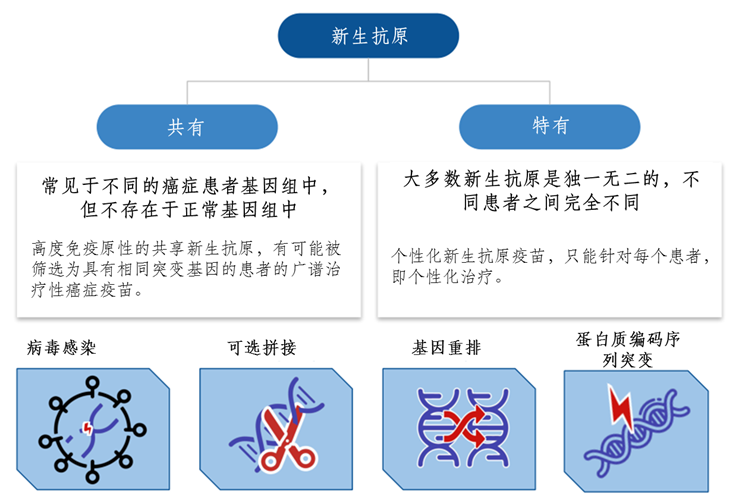
图4 新生抗原简介(图源:生物探索编辑团队&[2])
目前还没有批准的新生抗原癌症疫苗。根据ClinicalTrials.gov的搜索结果,有190个在研新生抗原,但是没有一个进入三期临床(不考虑HPV-疫苗)。与2021年第三季度的搜索结果相比,2022年多了30项新生抗原研究,这表明市场对癌症疫苗平台的兴趣有了巨大的增长。

图5 全球新生抗原研发公司现状(图源:生物探索编辑团队&[2])
新生抗原疗法的研究起步相对较晚,仍处于实验室阶段。Genocea Biosciences GEN-009疫苗试验(NCT03633110)目前正在进行I期/IIa期临床试验。NCT03633110的目的是评估GEN-009个体化疫苗用于治疗实体瘤患者的安全性、耐受性、免疫原性和抗肿瘤活性。目前为止的结果表明,已经接种了40剂疫苗,没有发生剂量限制性毒性,接种过疫苗的患者没有复发。GEN-009的预计完成日期为2022年12月,是当前个性化新生抗原疗效最佳的癌症疫苗。
BioNTech和Moderna是开发基于新生抗原癌症疫苗的领导者。BioNTech有六种癌症疫苗正在开发中,均共享新生抗原(FixVac平台)和与Genentech共同拥有两种基于个体化方法(iNeST平台);Achilles Therapeutics是一家生物制药公司,开发针对克隆新生抗原的精确T细胞疗法。目前,该公司有两项处于I/IIa期临床试验的疫苗:用于治疗晚期非小细胞肺癌的Chiron和用于治疗黑色素瘤的Thetis,评估新抗原反应性T细胞的安全性和临床活性;Transgene完成了个体化新抗原疫苗TG4050在卵巢癌和头颈癌中的I期临床试验研究。这种癌症疫苗基于Transgene的myvac®平台,并由先进的人工智能功能提供支持。Granite和Slate是由Gritstone Oncology开发的两种癌症疫苗。这两种药物目前都处于I/IIa期临床试验阶段,用于治疗不同类型的实体肿瘤。
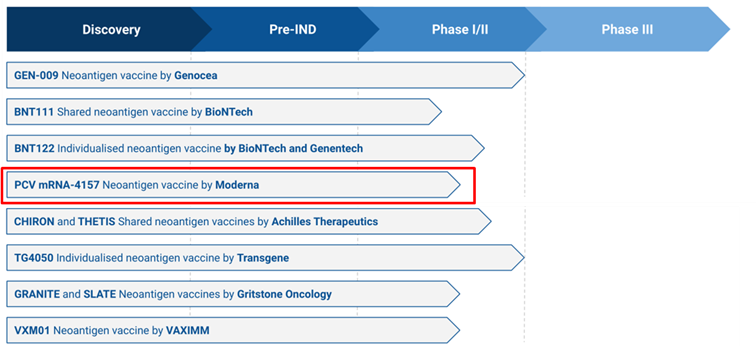
图6 正在研发的新生抗原癌症疫苗(图源:Deep-pharma)
新生抗原疫苗开发的第一个阶段颇为复杂和耗时。即使基因组和转录组测序技术正在积极发展,但数据的生物信息学处理仍然极具挑战。因此,新生抗原平台的复杂性与测序成本、速度、数据存储和分析等问题相重合。然而,随着数字化、人工智能、机器人和数据存储技术的广泛引入,这些问题即使不能几乎完全消除,至少也会减少。

图7 新抗原癌症疫苗开发的分步方案(图源:生物探索编辑团队&[2])
Merck与Moderna的mRNA-4157/V940与PD-1抑制剂Keytruda的组合疗法具有较好的发展前景。针对肿瘤细胞免疫逃逸问题开发出了PD-1抑制剂,其能够激活T细胞活性、诱导免疫原性因子的分泌。这就解决了新生抗原疫苗难以激活T细胞的免疫反应的问题。因此,两者的联合使用将成为新生抗原疫苗应用的新策略。树突状细胞疫苗与免疫检查点抑制剂联合使用,在治疗实体瘤和血液瘤方面均表现出了明显的临床优势。
参考资料:
[1]https://www.dailymail.co.uk/health/article-11533153/New-paradigm-moment-mRNA-cancer-vaccine-slashes-risk-tumor-relapse-death.html
[2]https://www.deep-pharma.tech/epigenetic-drugs-q2-2022





