目前,全球范围内正在进行大规模的新冠疫苗接种,这为缓解新冠疫情的流行趋势带来了希望。但由于新冠病毒关键变种来势汹汹,其疫苗的保护效力也受到了挑战。
近日,以色列特拉维夫大学研究团队对以色列疫苗接种人群进行了调查,以此来评估mRNA疫苗BNT162b2的保护效力。该研究成果以 Evidence for increased breakthrough rates of SARS-CoV-2 variants of concern in BNT162b2-mRNA-vaccinated individuals 为题目发表在了 Nature 上。研究提出,在特定时间窗口内,mRNA疫苗BNT162b2对两种新冠病毒变种的保护有效性有所降低,因此,应该更严格地进行病毒变异追踪,增加疫苗接种以防止病毒变种的传播。

https://doi.org/10.1038/s41591-021-01413-7
研究显示,在临床试验中,mRNA疫苗BNT162b2在预防新冠症状性疾病方面有95%的有效性,在以色列的现实环境中也展现了同样高的保护效力。但是,随着新冠变种病毒的不断增加,越来越多的证据显示这些变种可能会削弱新冠疫苗的保护效力,因此,检测它们能否击破新冠疫苗对人体的免疫防御作用迫在眉睫。
在该项研究中,研究人员对以色列Clalit健康服务中心有症状或无症状、已进行疫苗接种但仍然感染了新冠病毒的人群进行了调查,并将研究对象分为三组,第1组为在第一次给药后14天和第二次给药后6天之间进行PCR检测呈阳性的疫苗接种者,第2组为在第二次接种疫苗后7天内进行PCR检测呈阳性的疫苗接种者,最后一组为对照组,采用相同数量的、与两组研究对象基本同时期显示PCR检测阳性的未接种疫苗人群。最终收集了813个鼻咽拭子样本进行了病毒基因组测序,其中包括149对第2组-对照组、247对第1组-对照组和其他未成功测序的样本。
所有样本进行基因测序后,只有B.1.1.7 与 B.1.351两种新冠病毒变种出现在样本中,其中,B.1.1.7是以色列最主要的病毒变种,而B.1.351仅占所有样本的1.6%。研究人员假设,B.1.1.7可能具有轻微的疫苗抗性,而与之相比,B.1.351的疫苗抗性则会更高一些。结果显示,第2组病例与未接种疫苗的对照组相比,其B.1.351感染的比例明显更高,大约一半的第2组病例在第二次给药后7-13天检测呈阳性,大约一半在第二次给药后14天或更长时间内检测呈阳性。而在第1组中,其病例中B.1.1.7的感染率与对照组相比起来明显更高。
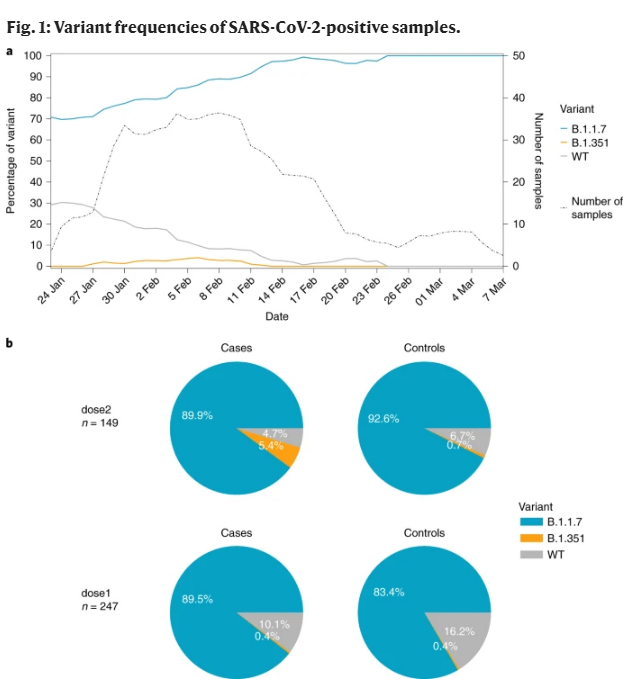
样本中的新冠变种病毒分布情况

疫苗接种后一段时间内新冠变种病毒感染分布,其中前三列为第1组,后三列为第2组
这些结果证明,在两个特定时间窗口内,会有疫苗突破性感染事件发生,同时其变种病毒比例有所增加。鉴于此结果,研究人员表示,目前的研究可能表明,在第一次接种后的最初几周内,mRNA疫苗BNT162b2对预防B.1.1.7变种感染的效力较低。此外,由于一些国家选择将第一针和第二针mRNA疫苗BNT162b2之间的间隔从建议的3周增加到更长的时间,因此应该更加严格地去评估这种延迟是否会影响仅接受第一剂疫苗的群体对新冠病毒变种的免疫防御效力。但同时因为新冠变种病毒在以色列出现的时间差、以及样本较少等因素交织在一起的复杂性,该研究结果需要被更加理性客观地看待。
目前,全球共有两款mRNA疫苗问世,其中德国BioNTech与辉瑞合作研发的BNT162b2已被纳入世界卫生组织紧急使用清单,另一款则为美国Moderna公司研发的mRNA-1273,两者在临床试验中的有效性均超过了90%。在国内,复星医药与德国BioNTech SE共同开发的mRNA疫苗BNT162b2已在待审批状态,可于8月份实现国产化,年产疫苗或将达10亿计。
此外,已进入临床试验阶段的国产mRNA疫苗还包括由沃森生物、苏州艾博和军事科学院军事医学研究院共同研制的ARCoV疫苗、斯微生物可预防多种变异毒株的新冠疫苗以及丽凡达生物自主研发的疫苗,让我们期待更多具有高保护效力的新冠疫苗上市,为抵抗新冠病毒变种做好更充足的准备!
参考资料:
[1]https://www.nature.com/articles/s41591-021-01413-7







