作为血液系统恶性肿瘤之一,白血病严重威胁了人类的健康。虽然常规化学疗法取得了进步,但许多患者仍然面临棘手的问题,包括严重的毒性反应和对化学疗法的不敏感性。最近,免疫疗法已成为治疗白血病的新突破。尽管在许多方案中都进行了多次疫苗接种,但其效果仍未达到预期水平。
对此,10月12日,来自中国科学院过程工程研究所和南方医科大学珠江医院的研究人员开发了一种治疗性疫苗,可将抗原表位肽和PD-1抗体共封装在自愈微胶囊中,以精确治疗白血病。在新型疫苗中,表位肽和PD-1抗体可通过微胶囊独特的自我修复功能,轻松、温和、高效地装载到聚乳酸微胶囊中。相关研究成果发表于《Nature Biomedical Engineering》上。

https://doi.org/10.1038/s41551-020-00624-6
具体而言,为了构建这种疫苗,研究人员使用聚乳酸(FDA批准的材料)合成具有巨大多孔结构的微球(千兆孔微球),从而能够以扩散方式有效地加载混合表位肽和PD-1抗体。由于在温和条件下,微球表层的毛孔具有独特的愈合特性,因此可以将抗原表位肽和PD-1抗体有效地作为货物共包封在最终的微胶囊中。
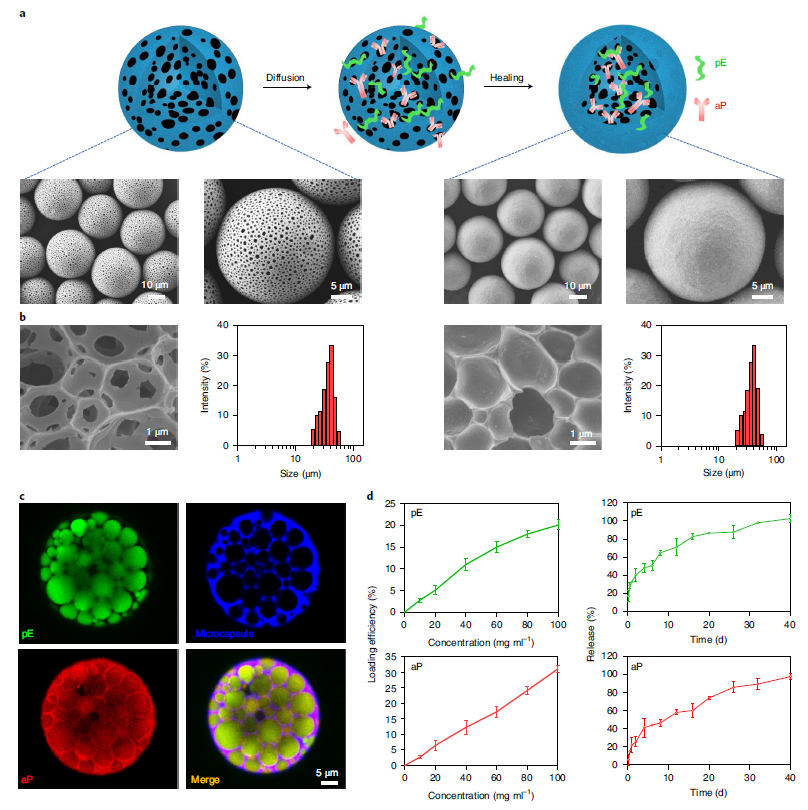
自愈微胶囊的制备与表征
在小鼠实验中,单次给药后,在疫苗接种部位产生的有利趋化因子和细胞因子募集了抗原呈递细胞并使其活化。同时,微胶囊的逐渐降解导致两种被包裹货物的持续释放。相应地,表位肽可被募集的抗原呈递细胞有效吸收,而PD-1抗体则被转运至淋巴进行T细胞调节。通过这些功能的配合,研究人员在特异性细胞毒性淋巴细胞的激活方面取得了实质性的改善。
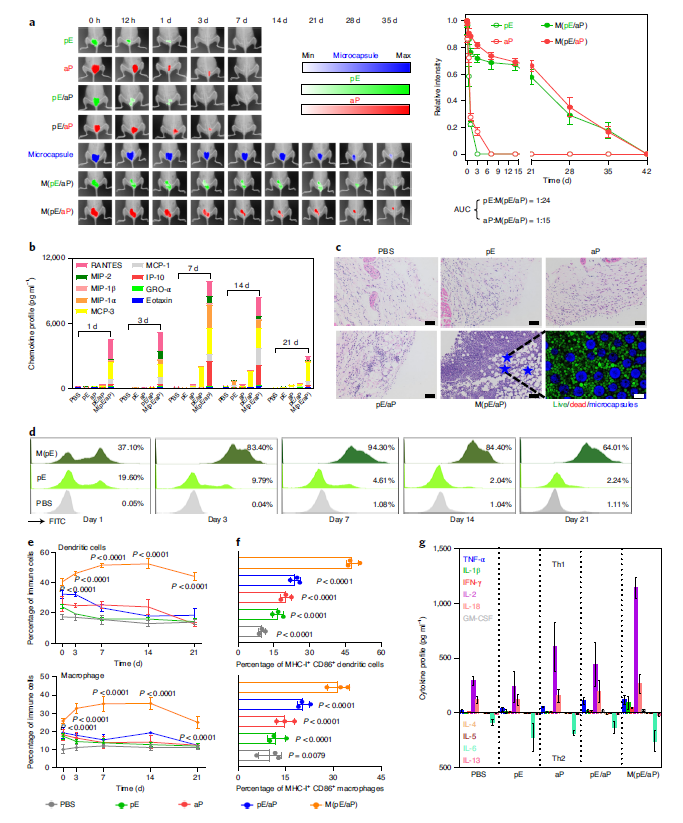
通过持续的抗原释放和注射部位抗原呈递细胞募集的协调,抗原呈递细胞的反应得以增强
研究人员还验证了在不同模型中使用各种表位肽的新型疫苗的可用性,例如鼠类白血病,人源化细胞系白血病异种移植物(CDX)和患者源性白血病异种移植物(PDX)模型。在所有白血病治疗模型中,基于微胶囊的制剂均表现出优于ISA佐剂(商业化佐剂)的性能,系统地抑制了白血病,且几乎没有异常。其高性能和安全性使该疫苗可以作为一种有前景的免疫疗法在临床上治疗白血病。
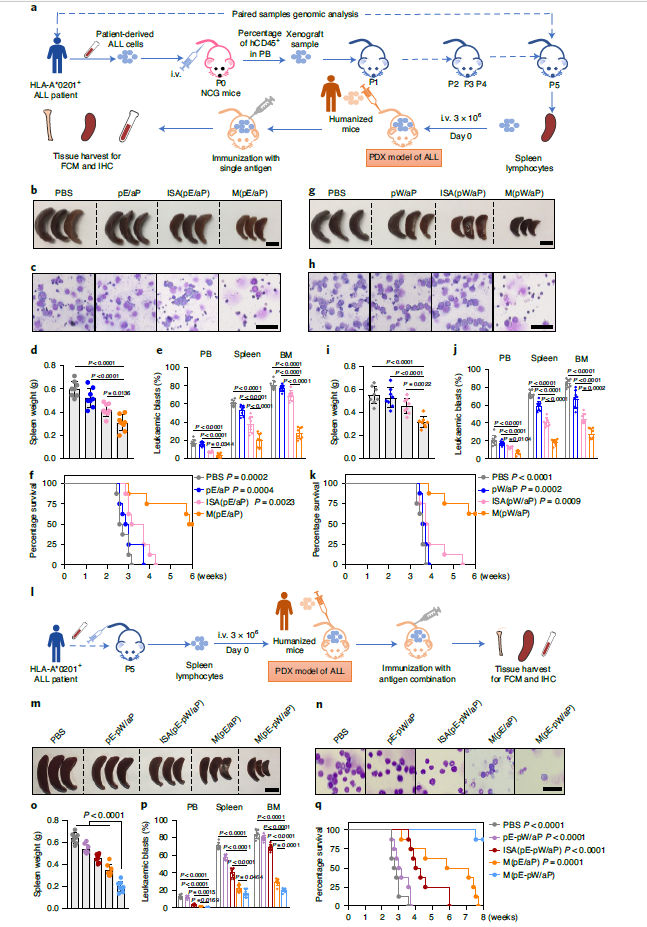
PBMCs-PDX模型中有效的抗白血病活性
研究人员强调,基于FDA批准的聚乳酸材料的优点,制备疫苗制剂的便利性,疫苗成分的多样性以及出色的治疗效果,这种基于微胶囊的疫苗具有很大的临床转化潜力。
《Nature Biomedical Engineering》的一位同行评审员将该研究描述为“全面的新平台”。审稿人还强调,这项工作是“令人兴奋和令人信服的”。
参考文献:
[2] Scientists develop new precisetherapeutic leukemia vaccine







