本文转载自 医麦客
近日,葛兰素史克公司(GlaxoSmith Kline,GSK)推行的Strimvelis疗法在上市近一年后迎来了第一位使用患者,这名欧洲儿童是继使用首个基因药物Glybera患者之后接受商业基因疗法的第二人。
2016年5月,全球制药巨头葛兰素史克公司(GlaxoSmithKline,GSK)的基因疗法Strimvelis被欧盟批准上市,此基因治疗是世界上第一个被批准上市用于儿童缺陷基因修复的疗法,针对ADA-SCID患者,是基因治疗走向市场的里程碑事件。
Strimvelis是继UniQure公司的脂蛋白酶缺乏症(LPLD)基因疗法Glybera之后的第二个被欧盟批准上市的基因治疗方法。(值得一提的是,就在上个月,UniQure公司宣布其在10月份Glybera的销售许可证到期之前不再重新申请销售许可,第一个上市的基因药物因上市四年只有一人使用而退出市场。)
这周二,葛兰素史克公司的新闻发言人Anna Padula表示,他们在今年3月份接收了第一名患者,这距离Strimvelis于2016年5月被批准在欧洲销售已经有一年时间了。
上市近一年,Strimvelis终于迎来了第一位患者,那么未来Strimvelis的商业化之路能否顺利前行呢?作为走向市场为数不多的新的基因治疗方法之一,Strimvelis的商业命运正受到密切关注,包括美国的Spark Therapeutics公司也计划在今年申请其治疗失明的基因疗法上市。
众所周知,基因药物开发的费用不菲,但评估基因治疗药物的潜在价值比较困难,因此定价、支付是个难题。
基因疗法费用高昂,保险公司是否愿意为患者买单,即使将来保险公司愿意买单,将会采取何种支付模式,是否应该与治疗的效果相关联,诸如此类问题都还没有解决方案。Glybera更是一针百万,被称为最贵基因药物。
同样,Strimvelis的定价和费用的支付,也不是一件简单的事情。很长一段时间内,该公司都未公布Strimvelis的售价。直到2016年8月,葛兰素史克公司宣布Strimvelis的售价为59.4万欧元(650000美元)。
650000美元的基因治疗费用太高了吗?

ADA-SCID患者—David Vetter在一间塑料房间里生活了12年,1984年死于骨髓移植的并发症
Strimvelis作为一种体外基因疗法,与CAR-T类似是在体外引入缺失DNA然后把细胞回输到患者体内。理论上只需要治疗一次,而且葛兰素史克表示付费可以采取分期付款模式并保证无效退款。相比较传统的干细胞移植和一年价格高达400000美元的酶替代疗法,其实Strimvelis并不算太贵,而且该疗法可以对病人DNA的一次性修复达到终身治愈的效果。
事实上,就商业利润而言,Strimvelis的上市对葛兰素史克公司是微不足道的。欧洲平均每年仅有15个ADA-SCID患者,收入800万-900万美元,相对于葛兰素史克公司几百亿美元的年销售额实在是不值一提。
但是公司看重的其实是如何借鉴罕见病的模式,更为精准地针对常见病开展基因治疗,一旦进入基因治疗领域黄金时间,自然就会盈利。
所以葛大爷有钱就是任性!
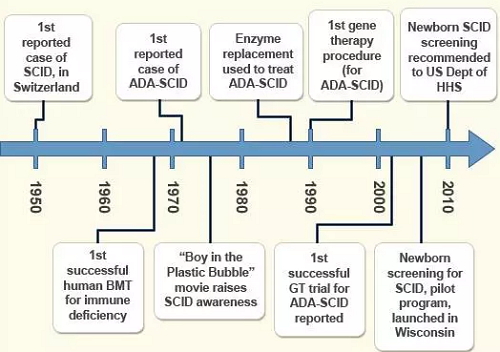
ADA-SCID基因治疗历史轨迹(来源:adagen)
ADA-SCID基因治疗最初由OSR和FondazioneTelethon通过San Raffaele Telethon Institute for Gene Therapy (SR-Tiget)联合开发,并与葛兰素史克公司开展战略合作以及由MOLMED推进研发。
Fondazione Telethon的首席科学官Lucia Monaco表示,Strimvelis需要“专业化的治疗环境”。

意大利米兰的Ospedale San Raffaele治疗中心
这就是为什么葛兰素史克一开始就把治疗场所设置于位于米兰的Ospedale San Raffaele。该公司表示,这样欧盟28个国家的儿童可以利用跨境医疗条款接受Strimvelis治疗,由母国支付昂贵的治疗费用。但这也是Strimvelis上市一年才有一位患者的原因,在欧洲只有意大利一个治疗中心、而且手续相对繁琐。这对于患者来说并不方便
而且事实上,一些ADA-SCID患者并没有寻求葛兰素史克的基因治疗,而是选择加入提供替代疗法的医院的临床试验。位于伦敦中心的大奥蒙德街医院(Great Ormond Street Hospital)也正在进行一项不同的ADA-SCID基因治疗研究。关注遗传性免疫缺陷疾病的慈善组织的主管Susan Walsh表示:“大奥蒙德街医院的临床研究取得了很好的成功,这意味着患者可以就近接受治疗,而不需要飞去意大利。”
对于美国和加拿大的患者,加州大学洛杉矶分校同样有ADA-SCID的临床试验。这项疗法已获得伦敦的Orchard Therapeutics许可,这家公司是由葛兰素史克公司前高管所创立的。
但万事开头难, Strimvelis为此也等了一年。GSK的Strimvelis项目领导人Jonathan Appleby说:葛兰素史克正在致力于研究低温冷冻和运输患者细胞的可行方法,这样公司就可以在欧洲各地提供Strimvelis。病人就不用前往米兰去治疗了。他表示,公司希望在未来两年内能够实现这种想法。
现如今,基因疗法算是已经通过了概念验证,取得了可观的结果。但是从科研到实业,注定是一条坎坷的道路。但至少,我们真的找到了重新编辑基因的入口,逆转了某些本来毫无胜算的赌局。重新编写生命信息也许就在明天,而明天我们就是诅咒的终结者。
纵使基因疗法商业化道阻且长,且不论能否获得商业上的成功,但是医学上的成功为其他基因治疗药物奠定了基础,在基因治疗药物的万里长征路上,我们的决定必须面向未来。
关于ADA-SCID
ADA-SCID为腺苷脱氨酶缺陷所致重症联合免疫缺陷症,这种罕见的疾病使新生儿几乎完全丧失抗病毒、细菌、霉菌的能力。有些患者只能生活在无菌环境中,所以也叫bubble boydisease。在Strimvelis上市前这类患者用干细胞移植和酶替代疗法控制。但不是每个患者都能找到匹配的捐献者。
关于Strimvelis
这款叫做Strimvelis的基因药物,利用病毒补全患ADA-SCID的儿童骨髓里缺失的基因,以治疗重度联合免疫缺陷症。Strimvelis疗法是从患者的骨髓中取出干细胞,通过转导将一个正常拷贝的ADA基因导入干细胞,然后采取静脉输注将干细胞重新导入患者体内,之后一部分干细胞会归巢至骨髓。该疗法已在18个患儿身上实施,最早一例是在15年前。目前这18例接受Strimvelis治疗的ADA-SCID患者仍然存活。一项关键性研究显示,所有儿科ADA-SCID患者接受Strimvelis治疗后3年的存活率达100%。Strimvelis只需给药一次,而且不依赖于第三方捐献者,不存在因排斥引发的免疫不相容风险。(eMedClub)
参考资料:
A Year After Approval, Gene-Therapy Cure Gets Its First Customer