导读:梅奥诊所的研究人员“以毒攻毒”治疗皮肤癌,他们以经过基因改造的水泡性口炎病毒为媒介,将源自黑素瘤癌细胞的广谱基因直接传送至皮肤癌肿瘤,在小鼠实验中得到了良好的结论。
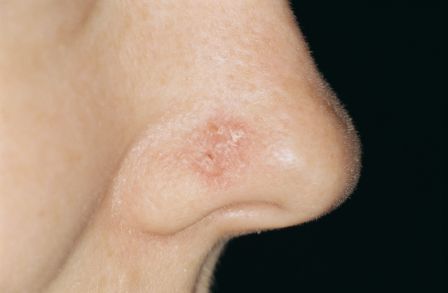
据美国物理学家组织网3月19日报道,美国梅奥诊所的研究人员利用从黑素瘤和狂犬病近似病毒中获取的人类组合DNA(脱氧核糖核酸),训练小鼠免疫系统从内部根除了皮肤癌。这种癌症免疫疗法可利用经基因方法改造过的水泡性口炎病毒,将源自黑素瘤癌细胞的广谱基因直接传送至肿瘤。初步研究结果表明,60%受到肿瘤困扰的小鼠可在3个月内痊愈,副作用也可降至最低水平。相关研究结果发表在本周出版的《自然·生物技术》杂志上。
该中心分子医学部的理查德·威尔博士表示:“我们相信这种新技术能帮助确认完整的全新抗原编码基因序列,这对于刺激免疫系统抗击癌症十分重要。特别是,我们已发现部分蛋白质需一起表达才能形成最有效的肿瘤抑制机制。通过使用疫苗同时打击多种蛋白,我们希望能同时治疗原发肿瘤并防止其复发。”
研究人员解释说,免疫系统基于“搜索摧毁”平台发挥功能,并可微调自身能力,以确定水泡性口炎病毒等病毒入侵。从全部肿瘤DNA频谱构建癌症疫苗的部分请求,表明肿瘤能够适应来自健康免疫系统的反复攻击,并显示出免疫系统可识别的较少抗原或路标。
癌症可以学会隐藏在正常的免疫系统之中,但却无法逃过经过水泡性口炎病毒和广谱DNA训练过的免疫系统。威尔表示,没人知道免疫系统能在肿瘤细胞中辨识出多少抗原,通过利用高度免疫原性的病毒表达这些蛋白,能增加免疫系统对它们的识别度。免疫系统会认为病毒正在向内侵入,而这些病毒表达了应该被消灭的癌症相关抗原。
由于研究人员无法隔离出足够的多样化肿瘤细胞抗原集合,许多有关免疫疗法的研究已经放缓。而采用新技术,肿瘤能够变异并重建自己,而无需担忧免疫系统的干扰。
在黑素瘤疫苗研制成功之前,该中心还制成了抗击肝癌的实验性疫苗。未来研究人员还将致力于研发类似疫苗以对抗更具侵略性的癌症,如肺癌、脑癌和胰腺癌等。

 Using virally expressed melanoma cDNA libraries to identify tumor-associated antigens that cure melanoma
Using virally expressed melanoma cDNA libraries to identify tumor-associated antigens that cure melanoma
Jose Pulido, Timothy Kottke, Jill Thompson, Feorillo Galivo, Phonphimon Wongthida, Rosa Maria Diaz, Diana Rommelfanger, Elizabeth Ilett, Larry Pease, Hardev Pandha, Kevin Harrington, Peter Selby, Alan Melcher & Richard Vile
Multiple intravenous injections of a cDNA library, derived from human melanoma cell lines and expressed using the highly immunogenic vector vesicular stomatitis virus (VSV), cured mice with established melanoma tumors. Successful tumor eradication was associated with the ability of mouse lymphoid cells to mount a tumor-specific CD4+ interleukin (IL)-17 recall response in vitro. We used this characteristic IL-17 response to screen the VSV-cDNA library and identified three different VSV-cDNA virus clones that, when used in combination but not alone, achieved the same efficacy against tumors as the complete parental virus library. VSV-expressed cDNA libraries can therefore be used to identify tumor rejection antigens that can cooperate to induce anti-tumor responses. This technology should be applicable to antigen discovery for other cancers, as well as for other diseases in which immune reactivity against more than one target antigen contributes to disease pathology.
文献链接:https://www.nature.com/nbt/journal/vaop/ncurrent/full/nbt.2157.html







