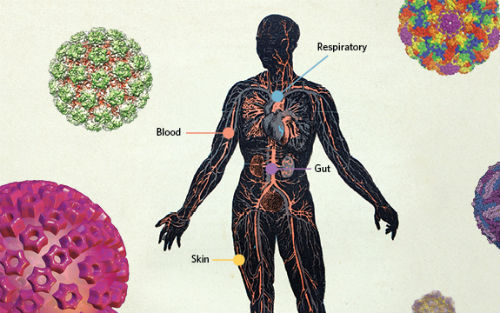
科学家们将寄居于人类体内或者表面的病毒统称为“人类病毒组”(human virome)。它们不仅仅会入侵人体细胞,还会对其他微生物造成影响,,例如细菌。得益于基因组学的发展,我们已经发现了很多之前从未发现的病毒种类,它们存在于皮肤、肠道、肺部、血液……
值得注意的是,很多病毒并不会立即引发病变,它们保持“潜伏”特性,直至感染者免疫力下降。它们看似“无害”,但是解析未知病毒的致病机理和共生模式,有利于我们判断对病毒采取不同的态度(防御或者忽视)。
如何发现新病毒?
病毒宏基因组学是当下鉴定新病毒、监控病毒变异的有效手段,它直接针对病毒遗传物质进行研究,避开了传统的病毒分离步骤。除了与已知病毒的基因组数据类似之外,更具有挑战的是那些基因组并不能匹配成功的未知病毒。
对于这些未知,研究人员将病毒基因组编译成蛋白芯片,以此筛查类似的病毒蛋白序列。因为相比于基因组,蛋白序列的变异速率相对较慢,所以匹配率更高。
借助宏基因组方法,科学家们已经鉴定了13个已知的人类多瘤病毒,并发现它们与免疫抑制移植神经、肾损伤、艾滋病以及皮肤癌有关。多瘤病毒多在儿童期入侵,它们不会立即发作,而是安静潜伏等待免疫系统“懈怠”,再伺机猖狂。多瘤病毒是人类致病性病毒家族的典型“分子”,例如一些人乳头状瘤病毒会潜伏在健康成年皮肤上,而另一些特定的乳头状瘤病毒却会导致宫颈癌。
人乳头状瘤病毒
指环病毒属(anelloviruses)是一类很少被研究的病毒,被称为是最常见的人类感染病毒。几乎100%的成年人血液中都会检测到这一类病毒。(文献3)指环病毒会在婴儿期就入侵人体,多数成员会进入血液引起持续的病毒血症。因为家族内各病毒种类的遗传背景差异较大,所以指环病毒能够感染不同的组织,导致不同的结果。与人乳头状瘤病毒一样,仅仅只有一部分指环病毒会引发疾病。
病毒长期的潜伏是否会对健康造成威胁还有待研究。目前并没有直接证据表明,指环病毒是有害的。它们的普遍性、慢性感染的特征意味着这些病毒与我们是共同进化的。科学家们最新在啮齿类动物和猴子模型上发现了指环病毒,这意味着我们可以借助动物模型对其致病性进行研究。
除了血源性病毒,科学家在健康人群的呼吸道和粪便样本中同样发现了很多病毒,特别是儿童,例如越来越多的指环病毒、小病毒(parvoviruses)、细小核糖核酸病毒(picornaviruses)、picobirnaviruses等。这些新病毒的挖掘意味着,即便再健康,我们身体内也会潜伏有一些慢性感染病毒。
如何评估病毒的致病性?
我们通常较为关注的是实际正在或者将要造成广泛流行负担的病毒,例如HIV、HCV以及Zika病毒。考虑到大多数感染者并没有表现出病症,所以科学家们需要首先确定它们是否存在致病性以及致病能力。
为此,早在19世纪末,德国医生和微生物学家Robert Koch建立了一套体系,并沿用至今。这一体系涉及4个标准:第一,病原体仅仅存在于患者人群中;第二,能够从患者身上分离;第三,接种该病毒会引发疾病;第四,可以从接种患者体内再次分离出病毒。
但是,检测病毒致病性并不容易。首先,许多病毒并不能被提取和体外培养。此外,考虑到无法在健康人体上进行接种试验,科学家们需要采用动物模型,例如恒河猴、小鼠,但是很多病毒仅仅感染人类。另外,研究人员可以将病变组织(患有肝炎的肝脏、脑炎的大脑)作为样本,一旦检测到病毒,则可以作为其致病性的直接证据。考虑到病变组织有限,所以一般以血液样本为主。
病例对照研究(case-control study)也可以用于病毒致病性研究,通过比较患者和未患病者之间的病毒检测率,分析病毒与该并的关联性。但是该方法需要控制影响两组对象的其他变量保持一致,例如年龄、地理位置、性别、社会经济地位等。
大多数病毒并不表现出绝对的致病性或者无害性,它们会针对不同的个体、不同的免疫状态反映出不同的结果。病毒致病的概率越小,越需要扩大病例对照研究量。
病毒也有好的一面
初生婴儿呼吸道、胃肠道受病毒感染很常见,且一般不会引发病症,这主要得益于通过胎盘以及母乳吸收的抗体。这样的减毒感染会建成天然的疫苗屏障,用于抵御成长期可能接触到的更加致病的相关病毒。
共生病毒也可以为防御其他病原体入侵,例如,GBV-C(一种与HCV病毒属于同一家系的病毒)、Zika病毒和登革热病毒已经被发现能够减缓艾滋病病毒感染的病症。(文献6)研究表明,艾滋病患者感染GBV-C病毒后,其存活期会明显延长。科学家们推测,这是因为GBV-C抑制HIV复制。
病毒感染的另一个潜在好处是它“热衷”于分裂快速的细胞。这也是科学家们研发溶瘤病毒对抗癌症的基础,通过改造病毒使其特异性地感染肿瘤细胞,并在肿瘤内溶瘤性复制使其裂解,实现免疫治疗作用。

约8%人类基因组来源于逆转录病毒
逆转录病毒一旦进入宿主细胞,会将其遗传物质插入宿主基因组中,并利用细胞中的物质和能力以及宿主DNA复制、转录和翻译能力进行扩增繁殖。其中,有一些病毒基因会被人类基因组“捕获”,从而负责宿主相关生理过程。
内源性逆转录病毒表达的蛋白可以与细胞受体结合,从而保护其他外源性病原体的入侵。一些内源性逆转录病毒的膜融合活动对于宿主某些生理功能不可或缺。例如,一些内源性逆转录病毒表面的包膜蛋白有利于促进滋养层细胞与胎盘中调节母体与胎儿实现营养、氧气交换的细胞结构融合。
近期,有研究团队证实,病毒蛋白合胞素(syncytin)除了促进胎盘发育之外,还有利于肌肉纤维形成过程中成肌细胞的融合,参与肌肉的形成。
人类病毒组的研究意义
对血液、咽拭子标本以及粪便等样本的检测有利于更好地预防和控制传染病流行。快速鉴别致病病原体可以减少不必要的抗生素使用,从而减缓耐药性病菌的产生和扩散。
同时,基因测序、大数据分析等技术的更迭有助于病毒组信息库逐步扩大和完善。基因组分析可以用于衡量不同区域的病毒流行情况。这些信息有利于确定致病病毒,从而确保疫苗等防御手段的快速跟进。对人类病毒组的研究有利于弄清楚病毒致病的机理、模式,从而预估病毒大流行的趋势,实现早期防御。
备注:文章参考自“Viruses of the Human Body”。







