“重磅炸弹”药物能够畅销的首要条件针对某一疾病具有良好的治疗作用且副作用小,能够得到处方医生和患者的认可,是治疗某一疾病的标准治疗药物。

如你所知,越来越多的疾病在等待着“新药”的拯救,这不仅仅是数量上的增加,还意味着更快的速度,更好的质量和更低的花费。然而,根据美国制药工业研究协会(PhRMA)的统计数据:每5000个测试的潜在新药中,仅有5个能够进入临床试验,仅有1个会被批准用于人类。2015年,科学杂志上发表了120万篇医学研究论文,但是只有396种潜在研究药物被提交给美国监管部门申请进行人体试验。
为什么?尽管新药研发也常常受金融和监管政策影响,但金融(全球药企每年在R&D上花费500亿美元)和政策(2014年FDA批准了77%申报)并不是主要原因。
那主要原因是什么?真正的原因是由于我们并没有期望中的新药,尤其是大多数药物在人体试验中达不到期望值。早期的时候,我们将这种高失败率归咎于创新性不够,而事实上是由于在研药物pipeline存在一个“死亡之谷”(Valley of Death)。受诸多因素影响,许多基础科学发现并没能完成这个跨越。每年,都有成百上千的潜在药物消失在“死亡之谷”。
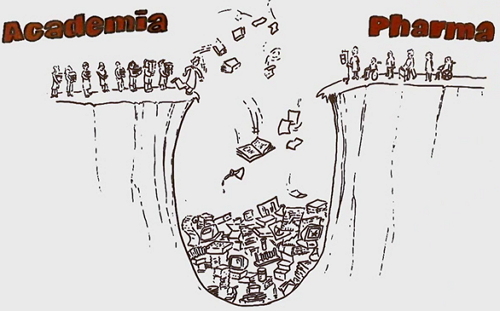
“死亡之谷”(Valley of Death),是科学家对基础科学发现与行业决定将想法转化为临床药物的这段时间的称呼。即全球科研院校的科学家通过开展基础研究实验来确定细胞是如何工作的,细胞是如何生长失控的已经细胞是如何过早死亡的。在这个过程中,他们会发现一些有潜力的新药靶标。
这些研究通常是针对基因而言,当移除某个基因来阻止肿瘤的形成或保护阿尔茨海默氏症患者的神经元退化(最差情况下:细胞在培养皿中生长,较好的试验:在老鼠身上)。而后他们在期刊上发表成果,作为其传统学术意义上的科研贡献。
毫无疑问,正是这些关键工作增加了我们对人类生物学的理解,以及解释疾病出现的原因;当然,并不是所有的科学发现都具有成为突破性药物的潜力,极少数的基础研究能产生直接的治疗方法。
与此同时,在药物的pipeline上,制药工业研究人员一直是从化合物的药理学和毒理学方面进行研究,而不是基因方面。制药工业研究人员正在寻找新颖的化合物(潜在的药物前体),并通过动物模型和其他途径证明其是有效的和安全的,即在药物还未被确认为一种新疗法之前,市场已经投入几十亿美元。
死亡之谷
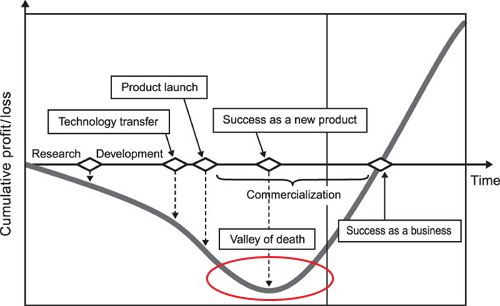
“死亡之谷”
如上所述,你看到了“科研界”和“制药界”之间的断层了吗?遗传操作是一种用来理解基础生物学的有力工具,但并不是治疗疾病的可行手段。在医药研究人员看来,化合物是最有效和最便宜的方法。
被“死亡之谷”隔断的科研界和产业界是一道难以跨越的鸿沟,即使想在上面“架桥”也非常困难。
山谷的一侧,极少数的科学家具有产业化所需的专业技能和资源,他们的科研成果仅能被认定为药物的潜在分子靶点,至于到底能否通过病理学试验和药物筛选,成为具有活力且可在人体进行临床试验的靶标很难确定;山谷的另一侧,是制药公司的迟疑,他们犹豫到底要不要在某个并不确定能为人类所用的靶点上豪赌数十亿美元。
因此,“死亡之谷”的问题显而易见,即双方皆在博弈,且双方好像都在等待别人来找到一个方法来以达到未来最好的选择。
通往“死亡之谷”的学术桥梁
有一种方法可以成为跨越药物发现“死亡之谷”的桥梁,这不仅在理论上而且在实践中得到了证实。 一些大学和非营利研究机构创造了学术药物发现和开发中心,旨在将基础研究成果转化为潜在的临床产品。一般情况下,传统的学术界并不适合这种工作。
这些中心不仅配备了药物化学、药理学、高通量筛选、药物代谢、生物信息学等方面的全职专家(通常是有药企工作经历的科研人员),而且装备先进,自动化程度极高,且在外面的制药公司很罕见。例如斯坦福大学和企业建立的合作机构SPARK 项目是致力于让学校的科研工作者大胆研发并实现其商业价值。
越来越多的类似孵化器的机构出现,不过其能否引领创新型的疗法值得商榷。数据显示,大约一百个学术机构中只有大约六家可能让制药公司感兴趣。虽然这些机构拥有先进的基础设施和疾病专家、学术研究人员和临床医生等人才,但他们缺乏药物发现的专业知识或培训。
然后,这些创新药物研发团队寻求与制药公司的早期资金合作,以援助他们沿着“死亡之谷”方向开发出具有潜力的pipeline。在这个途径里,学术界和产业界将在“死亡之谷”的中间会面,共同分享风险和回报。此外,政府在跨越“死亡之谷”的桥梁中也扮演重要角色。
推荐阅读: