1986年,世界上首个单克隆抗体药物——用于治疗器官移植出现的排斥反应的抗cd3单抗OKT3获得美国FDA的上市批准,由此拉开了单抗药物发展的序幕。如今,单抗已成为现代生物制药的重要组成部分,更是制药企业争相布局的“金矿产业”。
经过不到三十年的快速发展,单抗药物在肿瘤、自身免疫病、心血管疾病等领域取得了很好的成绩。随着获批抗体药物数量的增加,抗体市场规模也在不断扩大。1997年全球单抗药物销售额仅达3.7亿美元,而2007年销售额增长到了220亿美元,2013年这个数字已达到620亿。
据了解,目前全国有100多家企业在做单抗,除了中信国健、赛金生物、百泰生物、海正药业等一些老牌企业外,近几年还涌现出了很多新兴企业,包括丽珠单抗、信达生物、百济神州、嘉和生物以及布局生物药领域的恒瑞医药等。
以下是部分相关公司近期大事记一览:
恒瑞医药
9月3日,恒瑞医药发布公告称,公司与美国Incyte公司在美国达成协议,将具有自主知识产权的用于肿瘤免疫治疗的PD-1单克隆抗体(代号“SHR1210”)项目有偿许可给美国Incyte公司。Incyte公司将获得除中国大陆、香港、澳门和台湾地区以外的全球独家临床开发和市场销售的权利。
根据协议,Incyte公司将向恒瑞支付首付款2500万美元,另外还包括不超过9000万美元的上市里程碑付款、1.5亿美元的临床优效里程碑付款以及不超过5.3亿美元的销售业绩里程碑付款。此外,SHR1210在国外上市后,恒瑞按照约定比例从其年销售额中提成。
信达生物
10月12日,被业内的人比喻成“含着金汤匙”出生的信达生物再创记录。公司与礼来达成三个肿瘤免疫治疗双特异性抗体药物的全球开发合作协议,里程碑付款总金额超过10亿美元,成为迄今为止中国新药国际合作项目的所涉金额最大的一桩。
此前,信达与礼来曾经达成新药合作开发的战略合作协议,由礼来提供一个品种,信达提供两个品种,共同开发。首付5600万美元,其中一个项目的里程碑付款就达4亿美元。
而此番新合作协议,主角是三个新型双特异性肿瘤免疫治疗抗体,其中信达生物将合作主导中国市场的开发、生产和销售,礼来将合作主导国外市场的开发、生产和销售。据悉,三个抗体均使用来自于信达生物自主研发的PD-1单抗,是目前最有前景的新型双特异性肿瘤免疫治疗抗体。
嘉和生物
10月14日,沃生生物发布公告称,其控股子公司嘉和生物研发的单抗产品“注射用重组抗HER-2人源化单克隆抗体(曲妥珠单抗类似药)”和“注射用重组抗TNF-alpha人鼠嵌合单克隆抗体(英夫利昔单抗类似药)”均已获得CFDA颁发的临床批件,现正在开展临床研究工作。
为加快上述两个单抗产品的研发及产业化进程,嘉和生物设立了全资子公司玉溪嘉和生物技术有限公司(下称“玉溪嘉和”),由玉溪嘉和作为实施主体投资建设“治疗性单克隆抗体药物产业化项目”。项目建设工期计划为2年,总投资为25114.94万元;计划建成年产36万支曲妥珠单抗类似药和40万支英夫利昔单抗类似药的生产线,合计实现年产76万支单克隆抗体药物的生产规模。
百济神州
6月5日,百济神州(BeiGene)宣布其针对晚期肿瘤治疗的BGB-A317临床一期试验已经入组了第一位患者。BGB-A317是一个高选择性的强效的全人源的抗PD-1的单克隆抗体候选药物。
10月16日,百济神州向美国证交会(SEC)提交了筹集高达1亿美元的首次公开募股(IPO)申请,计划以BGNE作为股票代码登陆纳斯达克市场。公开资料显示,百济神州先后在于去年11月和今年5月完成两轮融资,价格分别为4.5亿人民币和6亿人民币;如果此次IPO成功,将极大推进百济神州临床试验的进程。
CFDA批准上市的10种国内单抗
目前,我国抗体药物开发市场正处于高速发展的时期;在过去的3-5年内,国内陆续有创新的抗体药物上市或者进入后期临床阶段,这些突破性的成果一步步推动着我国抗体产业的发展。然而,国内单抗的市场规模还较小,具有成熟的抗体工业体系和规模化生产能力的企业为数不多。
由于国内单抗等生物药物的全面研发起步较晚,截至目前年底,CFDA批准上市的国产单克隆抗体药物数量仅有10种,占国内上市单抗药物总数不到一半,销售额仅占全部生物技术药物的1.7%,远低于全球34%的水平,市场占有率不高。下表是已获CFDA批准的国产单克隆抗体:
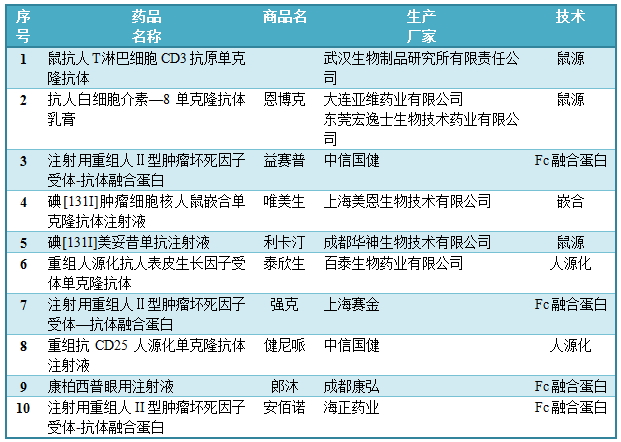
数据来源:沃森生物公司研究报告(2015-10-15)
国内的10个产品中,4个是鼠源型,1个嵌合型和2个人源化单抗,另有4个Fc融合蛋白类药物,而国外市场上人源和全人源化单抗药品约占90%。而目前真正实现产业化的抗体药物只有上海中信国健药业有限公司的益赛普、健尼哌以及百泰生物药液有限公司的泰欣生。
目前,外资单抗药品目前仍是国内市场的主导产品,但因其价格昂贵,国内大多数患者消费不起单抗等生物药物的治疗。近几年,越来越多的国内企业通过自主研发或者合作开发的方式发展单克隆抗体产品;其中,以上提到的一些企业也取得了非常突出的成果。这些消息对国内的患者来说都是巨大的福音。
1. 注射用抗人T细胞CD3鼠单抗
生产厂家:武汉生物制品研究所有限责任公司
国药准字S19990012、获批时间2010-09-30
适应症:肾脏移植、器官移植病人之急性排斥反应的治疗和预防。
药理作用:鼠源性抗人T淋巴细胞CD3抗原单克隆抗体,具有免疫抑制作用,可逆转对移植器官的排斥反应,其作用机理可能是阻断急性同种异体排斥反应中起主要作用的T细胞功能。体外试验结果表明,该药可作用于存在人类T细胞膜上并与其抗原识别结构相结合的CD3分子,从而影响该分子传递活化信号的功能,导致细胞因子释放,并因此阻断效应细胞的增殖和功能;体内试验结果表明,该药可与大部分外周血液和组织中的T细胞发生反应,但尚未发现该药可与其他血液成分或人体其他组织发生反应。
2. 抗人白介素-8鼠单抗乳膏(恩博克)
生产厂家:大连亚维药业有限公司、东莞宏逸士生物技术药业有限公司
2003-04-17,CFDA批准了东莞宏逸士生物技术药业有限公司抗人白细胞介素-8单克隆抗体乳膏(国药试字S20010004)
2010-08-30,CFDA批准了大连亚维药业有限公司抗人白介素-8鼠单抗乳膏(国药准字S20030093)
适应症:用于寻常型银屑病、亚急性湿疹的治疗
药理作用:白细胞介素-8对中性粒细胞具有趋化作用。据文献报道,银屑病病灶皮肤中的白细胞介素-8浓度高于正常水平,推测其可能是银屑病病灶早期形成的因素之一。动物试验结果提示,该药的作用机理可能是通过中和局部组织中的白细胞介素-8,降低中性粒细胞的聚集,从而减轻皮肤炎症的反应。单克隆抗体能有效地中和银屑病皮损组织中过量的白细胞介素-8,从而阻止嗜中性粒细胞对皮肤的浸润,抑制表皮角质化细胞的异常增生,消除炎症,达到治疗银屑病的目的。
3.注射用重组人Ⅱ型肿瘤坏死因子受体-抗体融合蛋白(益赛普)
生产厂家:上海中信国健药业股份有限公司
国药准字S20050058(12.5mg/瓶)、国药准字S20050059(25mg/瓶),获批时间为2015-01-27
适应症:1.中度及重度活动性类风湿关节炎;2. 18岁及18岁以上成人中度至重度斑块状银屑病;3.活动性强直性脊柱炎。
药理作用:已知肿瘤坏死因子(TNF-a)是类风湿性关节炎、银屑病、强直性脊柱炎等病理过程中的一个主要炎性介质,其参与调控的炎症反应可导致关节的病理改变。该药的作用机制为竞争性地与血中TNF-a结合,阻断它和细胞表面TNF受体结合,降低其活性。
4.碘[131I]肿瘤细胞核人鼠嵌合单克隆抗体注射液(唯美生)
生产厂家:上海美恩生物技术有限公司
国药准字S20060061,获批时间为2006-08-31
适应症:适用于放化疗不能控制或复发的晚期肺癌的放射免疫治疗
药理作用:该药是一种用于实体瘤放射免疫治疗的131I标记的人鼠嵌合型单抗,该单抗靶向作用于肿瘤坏死区中变性、坏死细胞的细胞核,将其荷载的放射性131I输送到实体瘤坏死部位,通过其局部放射性而对实体瘤组织细胞产生杀伤作用。
5. 碘[131I]美妥昔单抗注射液(利卡汀)
生产厂家:成都华神生物技术有限公司
国药准字S20060064,获批时间为2011-05-18
适应症:不能手术切除或术后复发的原发性肝癌,以及不适宜作动脉导管化学栓塞(TACE)或经TACE治疗后无效、复发的晚期肝癌患者。
药理作用:该药是一种用于导向放射治疗肝癌的碘[131I]标记的新型单抗。美妥昔单抗—HAb18 F(ab’)2可与分布在肝癌细胞膜蛋白中的HAb18G抗原结合,将其荷载的放射性碘[131I]输送到肿瘤部位,从而产生抗肿瘤作用。
6. 尼妥珠单抗注射液(泰欣生)
生产厂家:百泰生物药业有限公司
国药准字S20080001,获批时间为2012-12-25
适应症:适用于与放疗联合治疗表皮生长因子受体 (EGFR) 表达阳性的III/IV期鼻咽癌。
药理作用:EGFR是一种跨膜糖蛋白,分子量为170KD,其胞内区具有特殊的酪氨酸激酶活性。体内和体外研究显示,尼妥珠单抗可阻断EGFR与其配体的结合,并对EGFR过度表达的肿瘤具有抗血管生成、抗细胞增殖和促凋亡作用。
7. 注射用重组人Ⅱ型肿瘤坏死因子受体—抗体融合蛋白(强克)
生产厂家:上海赛金生物医药有限公司
国药准字S20110004,获批时间为2011-04-11
适应症:适用于中度及重度强直性脊柱炎患者。
药理作用:重组人Ⅱ型肿瘤坏死因子受体-抗体融合蛋白是一个二聚体的融合蛋白,包含人75KDa肿瘤坏死因子受体(TNFR)(p75)的细胞膜外配体结合部分与人IgG1的Fc片段,包含934个氨基酸,表观分子量约为150K道尔顿(KDa)。
TNF是机体自然产生的一种细胞因子,参与正常的炎症和免疫反应。在强直性脊柱炎关节病变的炎症反应中,TNF起着重要的作用。TNF存在55KDa蛋白(p55)和75KDa蛋白(p75)两类受体,它们均以单体的形式存在于细胞表面。TNF的生物学活性取决于它与细胞表面两类受体分子的结合。重组人Ⅱ型肿瘤坏死因子受体-抗体融合蛋白的作用机制是竞争性地与TNF结合,阻止TNF与细胞表面TNF受体的结合,抑制TNF的生物学活性。
8. 重组抗CD25人源化单克隆抗体注射液(健尼哌)
生产厂家:上海中信国健药业股份有限公司
国药准字S20110001,获批时间为2011-01-12
适应症:适用于预防肾移植后急性排斥反应的发生,可与含钙调素抑制剂和皮质类固醇激素的免疫抑制方案联用。
药理作用:该药是一种重组人源化抗Tac单克隆抗体,属于lgG1/k型抗体。作为白细胞介素-2受体拮抗剂,它与IL-2竞争,高特异性结合IL-2受体复合物(在激活的T细胞表面表达,而非静止的T细胞)的a-亚单位(Tac抗原),从而抑制IL-2生物活性。使用本品可抑制IL-2介导的淋巴细胞激活,亦即抑制了移植排斥反应过程中细胞免疫的关键通路。
9. 康柏西普眼用注射液(朗沐)
生产厂家:成都康弘生物科技有限公司
国药准字S20130012,获批时间为2013-11-27
适应症:用于治疗湿性年龄相关性黄斑变性(AMD)
药理作用:该药是一种VEGF受体与人免疫球蛋白Fc段基因重组的融合蛋白,通过结合血管内皮生长因子VEGF,竞争性抑制VEGF与受体结合并阻止VEGF家族受体的激活,从而抑制内皮细胞增殖和血管新生,达到治疗湿性年龄相关性黄斑变性的目的。
10. 注射用重组人II型肿瘤坏死因子受体-抗体融合蛋白(安佰诺)
生产厂家:浙江海正药业股份有限公司
国药准字S20150005(12.5mg/瓶)、国药准字S20150006(25mg/瓶),获批时间为2015-04-09
适应症:中度-至重度活动性类风湿关节炎、活动性强直性脊柱炎 和18 岁及 18 岁以上成人中度及重度斑块状银屑病
药理作用:已知肿瘤坏死因子(TNF-a)是类风湿性关节炎、银屑病、强直性脊柱炎等病理过程中的一个主要炎性介质,其参与调控的炎症反应可导致关节的病理改变。该药是一种通过中和肿瘤坏死因子体内生物学活性而发挥治疗作用的生物制剂。
特别备注:
1. 东莞宏逸士生物技术药业有限公司抗人白细胞介素-8单克隆抗体乳膏(国药试字S20010004)、上海美恩生物技术有限公司碘[131I]肿瘤细胞核人鼠嵌合单克隆抗体注射液(国药准字S20060061),信息来自网络,未在CFDA官网查到。
2. 本文表格以及部分信息参考自沃森生物公司研究报告:《沃森生物:玉溪嘉和生物技术有限公司治疗性单抗药物产业化项目可行性研究报告》







