近期,《JCI Insight》期刊发表一篇文章揭示,一类辅助T细胞——Th17细胞可以作为肿瘤过继细胞治疗的新选择,因为它们保留有类似于干细胞的特性,且体外长期培养扩增过程不会损耗它们的抗肿瘤活性。
这一研究由南卡罗莱纳医科大学(MUSC)的科研团队完成。通常,肿瘤过继细胞治疗选用的细胞毒性T细胞(CTL)在体外扩大培养过程中,抗肿瘤活性会大大受损。而这一研究首次证实,Th17细胞具有持久性,有望成为过继免疫疗法的又一利器。
肿瘤过继细胞治疗
肿瘤过继细胞治疗(adoptive cell therapy,ACT)是指向患者输入在体外培养扩增或激活、具有抗肿瘤活性的的免疫细胞,借助它们直接杀死或者激活机体免疫系统消灭肿瘤细胞,最终实现治疗肿瘤的目的。
从最早的淋巴因子激活的杀伤细胞(LAK,第一代)、细胞因子诱导的杀伤性细胞(CIK,第二代)、肿瘤浸润性淋巴细胞(TIL,第三代)到细胞毒性T淋巴细胞(CTL,第四代)、嵌合抗原受体T细胞(CAR-T,第五代),过继细胞治疗经历了几代更迭,是癌症免疫治疗的热门研究领域。
这种疗法包括提取、活化、扩大免疫细胞,以便它们能够在患者体内引发持久的抗肿瘤反应。然而,免疫细胞体外扩增需要提前数月进行,以便获得足够量的杀手T细胞,从而确保过继免疫治疗有效。此外,细胞毒性T细胞常常因为体外扩增在临床试验中失效。如何解决这些问题,一直是科学家们努力的方向。

文章一作Jacob S. Bowers和通讯作者Chrystal M. Paulos
Th17细胞
南卡罗莱纳医科大学的,微生物学和免疫学副教授Chrystal M. Paulos带领团队首次证明,一类T细胞亚群——Th17细胞能够抵抗体外扩增过程的退化。他们发现,Th17细胞具有长期有效的高抗肿瘤活性。
Paulos表示:“不同于CD8 +T细胞或者Th1细胞,我们发现Th17细胞可以扩增至大样本,且不会折损细胞质量。Th17细胞具有对数扩增的天然属性。这对于癌症免疫治疗而言,意味着新的替代细胞。”
考虑到Th17细胞具有类似于干细胞的属性,且在小鼠体内被证实具有持久的复制特性,研究团队推测,Th17细胞在体外经过长时间的扩增后,依然可以保留高效的抗肿瘤特性。他们经过一系列试验证实,不需要外界刺激,Th17细胞可以在体外持续扩增21天,最终生成的细胞数约为原有细胞的5000倍。
Th17细胞的“干细胞记忆”会保持完整。以患有黑色素瘤的小鼠为模型进行试验,研究人员发现,Th17细胞在体外培养扩增后输入小鼠体内,它们依然保留有活性,且能够在移植2周后消灭小鼠体内的肿瘤。这是CD8 +T细胞、Th1细胞所不能做到的。
此外,Th17细胞体外扩增14天后的抗肿瘤特性与扩增7天并无差别。“相同背景和时间下,CD8 +T细胞、Th1细胞的抗肿瘤活性会大大降低,而Th17细胞却依然保留有高效的能力。” Paulos强调,“某种程度上,Th17细胞的持久性与其抵抗细胞凋亡、衰老有关联。”
进一步研究表明,虽然一周时间的扩增并不足以生产出足够数量的Th17细胞,以便清除体积较大的肿瘤组织,但是2-3周的体外培养能够实现数量要求,从而有望根除肿瘤。
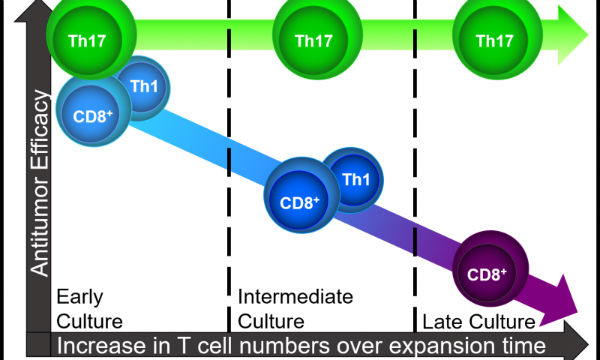
体外培养过程中,CD8 +T细胞、Th1细胞抗肿瘤活性逐步衰退,而Th17细胞却能够保留活性,从而确保有效的过继细胞治疗。
Paulos 表示:“我们想知道,长期的细胞培养是否能够对抗非常大体积的肿瘤组织(模拟晚期癌症)。研究表明,在短短2周内,我们能够获得足够多的Th17细胞,用于引发持久的免疫反应,从而根除肿瘤组织。动物实验证实,长时间体外扩增获得的Th17细胞能够治愈所有的患癌小鼠。而且,治疗100天后,我们人为移植肺肿瘤进入小鼠体内,结果发现其体内的Th17细胞能够提供多月的保护反应。”
数据显示,Th17细胞通过直接清除肿瘤本身,引发非常有效的抗肿瘤反应。在所有的试验中,Th17细胞都会引发机体抗肿瘤免疫反应,且强于CD8 +T细胞及其他CD4 +T细胞类群,例如Th1细胞。
参考资料:
Th17 cells could facilitate wider clinical use of adoptive immunotherapy







