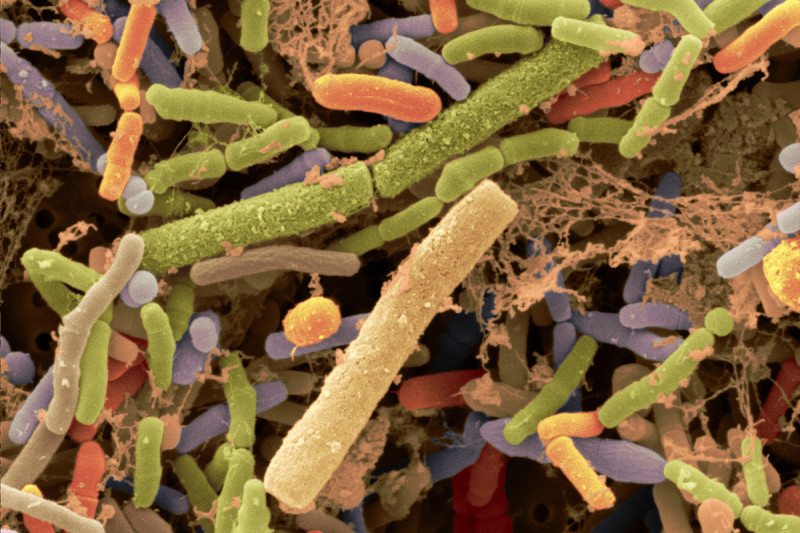
在寻求个性化治疗的过程中,许多研究都将焦点集中个体基因组的差异上。然而,越来越多的证据表明,个体对药物的反应不仅仅受到基因的影响,我们独特的微生物群落——那些生活在身体中的细菌和其他微生物群——是决定药效的关键。
研究人员现在已经有证据表明,健康人能够以不同的方式代谢某些药物,这取决于他们的微生物组成。这项研究结果于6月4日在新奥尔良召开的美国微生物学会会议上公布。
定居于人体中的细菌会“吃掉”它们周围的任何营养物质,无论是宿主饮食中的食物,还是所服用的药物。但是,如果微生物把一种药物代谢成无用的或有毒的化合物,那它们肆意进食就会给我们带来困扰。
纽约阿尔伯特爱因斯坦医学院的计算生物学家Leah Guthrie研究了一种常用于治疗结肠癌的药物——伊立替康的数据,在一些患者中,这种药会引起严重腹泻。以前在小鼠中的研究发现,一种名为β-葡萄糖醛酸酶的细菌酶可以修饰伊立替康和其他药物的化学结构。正常情况下,肝脏通过葡萄糖醛酸化过程给药物添加基团解毒。但是这种细菌酶会移除添加的基团,将药物分解成一种有毒化合物。
肠道菌群影响患者对药物毒素的吸收
为了了解个体的肠道菌群是否影响了他们对药物的代谢,Guthrie和她的同事收集了20个健康人的粪便样本。他们用伊立替康对样品进行处理,并测量样品中细菌与药物相互作用时产生的化合物。研究小组发现,其中4个样本含有高水平的伊立替康代谢毒素,但在样本中发现的细菌种类没有显著差异。
当研究人员分析粪便样本中合成的蛋白质时,他们发现那些有较多细菌代谢物的人包含生产更多β-葡萄糖醛酸酶的菌株。这些人体内将糖运输到细胞的蛋白质水平也明显较高,这表明他们更有可能吸收有毒化合物并产生胃肠道问题。
研究负责人、阿尔伯特爱因斯坦医学院的微生物学家Libusha Kelly说,研究人员正计划收集使用伊立替康的癌症患者的样本,以确定是否存在这种情况。
北卡罗来纳大学教堂山分校的结构生物学家Matthew Redinbo也在研究伊立替康,他认为这是了解肠道细菌酶与药物相互作用的一步很好的研究。Redinbo说:“我们最深入的探索就是观察肠道酶,并像人类的酶一样研究它们。”
Redinbo说,肝脏通过β-葡萄糖醛酸酶移除化学基团来处理许多患者使用的药物:这意味着微生物的影响是非常深远的。他在小鼠中的工作发现一些β-葡萄糖醛酸酶能对消炎药,包括布洛芬进行类似的修饰,这可会在长期用药时导致肠道毒性。
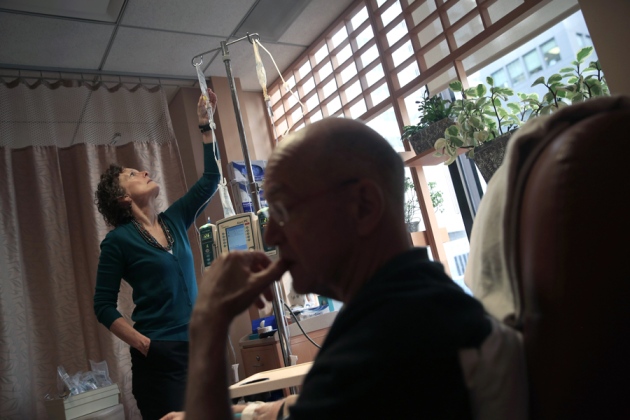
药物对一些疾病,如癌症的治疗效果往往存在个体差异。图片来源:Nature
肠道微生物对药物影响仍然存在许多未知
美国马萨诸塞州剑桥市哈佛大学的生物化学家Emily Balskus说,研究人员已经发现了几十种肠道细菌似乎可以修饰治疗药物,包括一些治疗帕金森病和焦虑的药物。细菌干扰也可能有助于解释为什么动物模型并不总能预测人类的药物毒性,因为动物的肠道微生物与人类不同。
不过,目前仍然还有许多问题存在。现在只有极少数破坏药物的酶被发现,并且现在还不清楚在人类人群中肠道细菌的差异有多大。
比如,6月2日发表在Science杂志上的一篇论文指出,用于阴道凝胶的抗艾滋病毒药物泰诺福韦,对那些阴道含有Gardnerella菌的女性无效。这种细菌很快将药物分解成非活性化合物,但是科学家们还不知道这个过程如何工作,或者是否可以阻止。
Balskus说,最终,临床医生也许能够筛选人们的微生物,来确定药物是否对他们有效。如果他们的肠道微生物群落看起来有点问题,医生可以开一些酶抑制剂,或者改变患者饮食从而为细菌提供替代的食物来源。一项研究表明,对小鼠进行饮食干预成功防止了肠道细菌降解一种名为digoxin的心脏病药物。
Redinbo想在人类身上尝试这项技术。他开办了一家生物公司,计划申请临床试验许可,在这项实验中,研究人员将给癌症患者β-葡萄糖醛酸酶抑制剂与伊立替康。
尽管如此,还需要更多的研究才能进一步了解细菌与药物之间的相互作用。因此,这种治疗方法要被医生使用还需要很长时间。
参考资料:







