
数字PCR是PCR领域最激动人心的创新之一,这一技术的诞生让绝对定量的梦想成为现实。与传统PCR不同,数字PCR是一种新的核酸检测和定量方法,直接检测目标序列的拷贝数。它不依赖于标准曲线和参照样本,因此比传统PCR更具灵敏度、特异性和精确性。
数字PCR技术在极微量核酸样本检测、复杂背景下稀有突变检测、表达量微小差异鉴定方面表现出很大的优势。
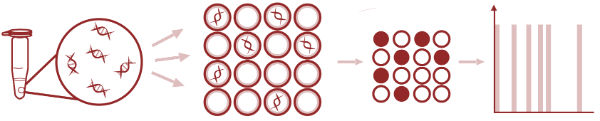
数字PCR的原理
DPCR产品获创新医疗器械特别审批
近期,生物探索在国家食品药品监督管理总局医疗器审评中心(CMDE)官网注意到“芯片式数字聚合酶链式反应(DPCR)分析系统”进入创新医疗器械特别审批程序。这意味着,这款数字PCR产品被率先纳入“绿色通道”。借此,我们采访了这款产品的研发负责人、南京科维思生物科技有限公司CEO王焱博士,请他为我们介绍了这一技术的创新点。

王焱博士表示:“首先,灵敏度高。每张芯片上有2万个微孔,可形成2万独立的PCR反应体系,检测灵敏度达到0.1%。其次,隔绝污染。借助于多色荧光系统和密封的芯片,dPCR系统可以很好地避免了污染物以及液滴系统中常见的DNA损失。最后,仪器操作简易,且配备有直观简单的读取、分析软件。”
“2015年11月,我们与Therno Fisher签署合作协议,构建芯片式数字PCR系统。随后一年,我们在Themo Fisher产品的基础上,申请了核心耗材的发明专利以便快速本地化,致力于构建中国乃至全球的第一款数字PCR技术平台。” 王焱博士回顾道。
DPCR+NGS,助力肿瘤液体活检
DPCR凭借其创新特色,可以与高通量测序(NGS)平台实现优势互补,有望成为支撑液体活检的重要平台之一。
2017年3月,阿斯利康宣布其第三代肺癌靶向药物泰瑞沙(甲磺酸奥希替尼片, AZD9291)获CFDA批准,很快在中国上市。泰瑞沙是一款靶向抗癌药物,适用于基因EGFR出现T790M突变的肺癌患者。作为在中国获批的首个第三代肺癌靶向药物,它的获批无疑给中国携带有EGFR T790M突变的非小细胞肺癌患者带来好消息。
据悉,阿斯利康比较了NGS、qPCR和DPCR的检测结果后认为,DPCR是AZ9291伴随诊断的首选。这是DPCR助力液体活检的典型案例,它有望成为癌症精准治疗的坚强后盾。
王焱博士表示:“DPCR以患者外周血为媒介取代组织活检,检测肿瘤相关的基因突变的存在,并动态监控其随病程进展及治疗过程发生的演变。结合生物信息分析技术,实现对肿瘤早期诊断、个性化治疗、治疗效及预后评估和监控等工作,从而为癌症病人的临床伴随诊断和个性化治疗提供有力的依据。目前,基于芯片式DPCR系统,我们已经完成五款肿瘤检测试剂的开发工作。”
最后,王焱博士展望道:“我们期待和更多IVD厂商合作,在这个新的技术平台共同研发新产品,共同向医院终端进行推广,为肿瘤患者延长生命。”







