为了保障医疗器械的安全、有效,鼓励医疗器械的研究与创新,促进医疗器械新技术的推广和应用,推动医疗器械产业发展,2014年2月7日,国家食品药品监督管理总局组织制定了《创新医疗器械特别审批程序(试行)》。该《程序》发布实施以来,全国各地的申请审批情况如何呢?
笔者汇总了《程序》发布以来全国各地进入创新医疗器械审批程序的产品和企业情况,从以下汇总表可以看出,创新医疗器械特别审批呈现以下几大特征:
一、生物、基因类医疗器械受宠
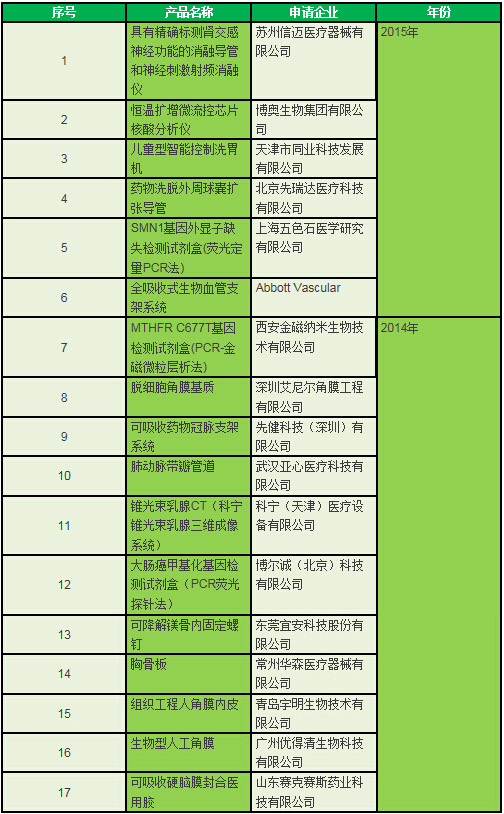
从进入创新医疗器械特别审批程序的产品种类来看,生物、基因类创新医疗器械受到管理层宠爱。如上海五色石医学研究有限公司申请的SMN1基因外显子缺失检测试剂盒;博奥生物集团有限公司申请的恒温扩增微流控芯片核酸分析仪;Abbott Vascular申请的全吸收式生物血管支架系统;西安金磁纳米生物技术有限公司申请的MTHFR C677T基因检测试剂盒;博尔诚(北京)科技有限公司申请的大肠癌甲基化基因检测试剂盒;广州优得清生物科技有限公司申请的生物型人工角膜;青岛宇明生物技术有限公司申请的组织工程人角膜内皮。这些产品占了全体过批创新医疗器械17种产品的大部分,占41.2%。
可见,选对医疗器械创新的切入口、顺应技术发展的趋势、符合社会消费需求、掌握产品核心技术知识产权,成为顺利通过创新医疗器械产品审批的四大窍门,也是从源头上确立竞争不败之地的根本策略!
二、较之2014年,2015年审批速度加快
自《程序》发布实施以来,共通过17项产品。其中,2014年全年共审批11项。2015年前3月,共通过创新医疗器械审批6项,这表明,国家对创新医疗器械的审批速度有所加快。这迎合了行业企业的期望,对产品快速上市生产销售是一大利好。
三、创新医疗器械来源地以沿海地区为主
从汇总表可以看出,申请创新医疗器械审批的厂家主要分布在北京、天津为主的环渤海经济区;上海、苏州为主的长三角经济区;深圳、东莞为主的珠三角经济区。其中,内陆省份通过创新医疗器械审批的厂家很少,只有西安、武汉分别各有一家。这种特征符合我国经济发展的现状,经济发达、技术进步的沿海地区成为我国创新医疗器械发展的主源地。
创新医疗器械产品审批汇总表
总之,《程序》的实施效果从以上分析即可得到总结。该《程序》顺应国家鼓励医疗器械的研究与创新要求,有利于发挥市场机制的作用,进一步促进医疗器械新技术的推广和应用。对于创新医疗器械,按照优先安排注册检验、技术审评、注册审批的原则,最大程度地提升我国医疗器械创新发展的速度。







